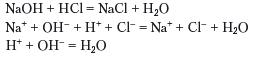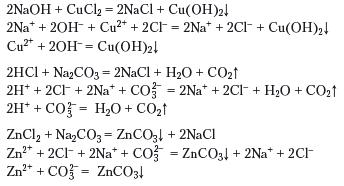|
|
|
| Строка 1: |
Строка 1: |
| - | '''[[Гіпермаркет Знань - перший в світі!|Гіпермаркет Знань]]>>[[Хімія|Хімія]]>>[[Хімія 10 клас|Хімія 10 клас]]>> Хімія: Найважливіші класи неорганічних сполук<metakeywords>Найважливіші класи неорганічних сполук</metakeywords>''' <br> | + | '''[[Гіпермаркет Знань - перший в світі!|Гіпермаркет Знань]]>>[[Хімія|Хімія]]>>[[Хімія 10 клас|Хімія 10 клас]]>> Найважливіші класи неорганічних сполук<metakeywords>Найважливіші класи неорганічних сполук</metakeywords>''' <br> |
| - |
| + | |
| | | | |
| - | <br> | + | <br> <br> '''Загальні відомості про [[Найважливіші_класи_неорганічних_сполук._Презентація|найважливіші класи неорганічних сполук]]'''<br>В основній школі ви вже вивчили такі класи [[Неорганічні_сполуки._Повні_уроки|неорганічних сполук]], як [[12._Оксиди,_їх_склад,_назви|оксиди]], [[13._Кислоти,_їх_склад,_назви|кислоти]], [[15._Основи,_їх_склад,_назви|основи]], [[14._Солі_(середні),_їх_склад,_назви|солі]].<br>► ''Пригадайте їх визначення й розподіліть наведені формули за класами сполук, назвіть речовини: ''[[Image:H1028.jpg|Формули. фото]]<br>Серед неорганічних сполук переважають представники саме цих класів. Хоча, окрім них, вам відомі амфотерні гідроксиди (алюміній гідроксид, цинк гідроксид та ін.), пероксиди (гідроген пе-роксид та ін.).<br>Речовини, формули яких ви віднесли до одного класу, подібні за складом, проте мають відмінності щодо [[Основні_фізичні_та_хімічні_властивості_неметалів|фізичних і хімічних властивостей]]. Це дає підстави для їх класифікації на окремі групи. Так, за агрегатним станом (фізична характеристика) оксиди поділяють на тверді (наприклад, фосфор(У) оксид), рідкі (наприклад, вода), газуваті (наприклад, карбон(ІУ) оксид).<br>''Наведіть власні приклади оксидів, що за звичайних умов перебувають у різному агрегатному стані.''<br>За здатністю розчинятися у воді кислоти, основи та солі поділяють на розчинні, малорозчинні й нерозчинні. Наприклад, сульфатна кислота добре розчинна, силікатна кислота — нерозчинна, купрум(ІІ) гідроксид — нерозчинна основа, натрій гідроксид -розчинна основа, або луг, кальцій гідроксид — малорозчинна основа, натрій хлорид — розчинна сіль, барій сульфат — нерозчинна сіль, кальцій сульфат — малорозчинна сіль. Потрібно пам'ятати, що абсолютно нерозчинних речовин не існує.<br>Розчинні основи утворюють мильні на дотик розчини, через що ці речовини дістали назву луги. Це: літій гідроксид, натрій гідроксид, калій гідроксид, кальцій гідроксид, барій гідроксид і деякі інші. Їх значно менше, аніж нерозчинних основ.<br>З-поміж різних класифікацій неорганічних речовин найуживанішою є класифікація за хімічними властивостями.<br>Оксиди. Вам відомо, що оксиди — бінарні сполуки елемента з Оксигеном, у яких він проявляє [[62._Ступінь_окиснення|ступінь окиснення ]]-2. Вони бувають солетвірні й несолетвірні. Солетвірні на підставі їх хімічних властивостей поділяють на основні, кислотні й амфотерні.<br>'''Основні оксиди''' — це оксиди, які взаємодіють із кислотами з утворенням солі та води.<br>До них належать лише оксиди металічних елементів зі ступенем окиснення +1, +2, рідше +3.<br>[[Image:H1029.jpg|350px|Основи. фото]] |
| - |
| + | |
| | | | |
| - | '''Загальні відомості про найважливіші класи неорганічних сполук'''<br>В основній школі ви вже вивчили такі класи неорганічних сполук, як оксиди, кислоти, основи, солі.<br>► Пригадайте їх визначення й розподіліть наведені формули за класами сполук, назвіть речовини: [[Image:H1028.jpg]]<br>Серед неорганічних сполук переважають представники саме цих класів. Хоча, окрім них, вам відомі амфотерні гідроксиди (алюміній гідроксид, цинк гідроксид та ін.), пероксиди (гідроген пе-роксид та ін.).<br>Речовини, формули яких ви віднесли до одного класу, подібні за складом, проте мають відмінності щодо фізичних і хімічних властивостей. Це дає підстави для їх класифікації на окремі групи. Так, за агрегатним станом (фізична характеристика) оксиди поділяють на тверді (наприклад, фосфор(У) оксид), рідкі (наприклад, вода), газуваті (наприклад, карбон(ІУ) оксид).<br>Наведіть власні приклади оксидів, що за звичайних умов перебувають у різному агрегатному стані.<br>За здатністю розчинятися у воді кислоти, основи та солі поділяють на розчинні, малорозчинні й нерозчинні. Наприклад, сульфатна кислота добре розчинна, силікатна кислота — нерозчинна, купрум(ІІ) гідроксид — нерозчинна основа, натрій гідроксид -розчинна основа, або луг, кальцій гідроксид — малорозчинна основа, натрій хлорид — розчинна сіль, барій сульфат — нерозчинна сіль, кальцій сульфат — малорозчинна сіль. Потрібно пам'ятати, що абсолютно нерозчинних речовин не існує.<br>Розчинні основи утворюють мильні на дотик розчини, через що ці речовини дістали назву луги. Це: літій гідроксид, натрій гідроксид, калій гідроксид, кальцій гідроксид, барій гідроксид і деякі інші. Їх значно менше, аніж нерозчинних основ.<br>З-поміж різних класифікацій неорганічних речовин найуживанішою є класифікація за хімічними властивостями.<br>Оксиди. Вам відомо, що оксиди — бінарні сполуки елемента з Оксигеном, у яких він проявляє ступінь окиснення -2. Вони бувають солетвірні й несолетвірні. Солетвірні на підставі їх хімічних властивостей поділяють на основні, кислотні й амфотерні.<br>'''Основні оксиди''' — це оксиди, які взаємодіють із кислотами з утворенням солі та води.<br>До них належать лише оксиди металічних елементів зі ступенем окиснення +1, +2, рідше +3.<br>[[Image:H1029.jpg]]<br>► Визначте ступінь окиснення атомів металічних елементів у наведених формулах. Яка закономірність простежується між їх ступенем окиснення в оксиді й основі?<br>Кислотні оксиди — це оксиди, які взаємодіють із лугами з утворенням солі та води.<br>До них належать усі солетвірні оксиди неметалічних елементів та оксиди деяких металічних елементів із високими ступенями окиснення (+5, +6, +7).<br>[[Image:H1030.jpg]]<br>Щодо кислотних оксидів і відповідних їм гідратів оксидів (ок-сигеновмісних кислот), то для них також справджується закономірність, виявлена для основ: атоми кислототвірних елементів у кислотному оксиді й відповідній йому кислоті мають однаковий ступінь окиснення.<br>► Напишіть формули сульфур(ІУ) оксиду і сульфур(УІ) оксиду та формули відповідних їм гідратів оксидів.<br>Амфотерні оксиди — оксиди, які утворюють сіль і воду при взаємодії як із кислотою, так і з лугом.<br>До них належить невелика кількість оксидів металічних елементів: <br> | + | ''Мал. 1. Основи''<br>''► Визначте ступінь окиснення атомів металічних елементів у наведених формулах. Яка закономірність простежується між їх ступенем окиснення в оксиді й основі?''<br>'''Кислотні оксиди''' — це оксиди, які взаємодіють із лугами з утворенням солі та води.<br>До них належать усі солетвірні оксиди неметалічних елементів та оксиди деяких металічних елементів із високими ступенями окиснення (+5, +6, +7).<br>[[Image:H1030.jpg|350px|Кислоти. фото]] |
| - |
| + | |
| | | | |
| - | [[Image:H1031.jpg]]<br>'''Кислоти. '''Кислоти належать до складних речовин, загальну формулу яких передає об'ємне зображення:<br>
| + | ''Мал. 2. Кислоти.''<br>Щодо кислотних оксидів і відповідних їм гідратів оксидів (ок-сигеновмісних кислот), то для них також справджується закономірність, виявлена для основ: атоми кислототвірних елементів у кислотному оксиді й відповідній йому кислоті мають однаковий ступінь окиснення.<br>''► Напишіть формули сульфур(ІУ) оксиду і сульфур(УІ) оксиду та формули відповідних їм гідратів оксидів.''<br>'''Амфотерні оксиди''' — оксиди, які утворюють сіль і воду при взаємодії як із кислотою, так і з лугом.<br>До них належить невелика кількість оксидів металічних елементів: <br> |
| - |
| + | |
| | | | |
| - | [[Image:H1032.jpg]]<br>У розчинах кислот наявні катіони Гідрогену, що зумовлюють загальні властивості кислот. Так, кислоти взаємодіють з: 1) індикаторами; 2) металами (розташованими в ряді активності до водню); 3) основними й амфотерними оксидами;4) основами й амфотерними гідроксидами; 5) солями інших кислот, якщо один із продуктів реакції випадає в осад або виділяється в газоподібному стані.<br>Наведіть приклади рівнянь реакцій, що ілюструють зазначені властивості кислот.<br>Катіони Гідрогену зумовлюють загальні, кислотні залишки — специфічні властивості кислот.<br>'''Основи.''' Основи належать до складних речовин, загальну формулу яких передає об'ємне зображення:<br> | + | [[Image:H1031.jpg|350px|Амфотерні гідроксиди. фото]] |
| - |
| + | |
| | | | |
| - | [[Image:H1033.jpg]]<br>Як вам відомо, серед основ сильними електролітами є луги. Наявність гідроксид-іонів зумовлює загальні властивості лугів: 1) дію на індикатори; 2) взаємодію з кислотними та амфотерними оксидами; 3) взаємодію з кислотами (реакція нейтралізації); 4) взаємодію з амфотерними гідроксидами; 5) взаємодію із солями, якщо один із продуктів реакції випадає в осад або виділяється в газоподібному стані.<br>Наведіть приклади рівнянь реакцій, що ілюструють зазначені загальні властивості лугів.<br>Для нерозчинних основ характерною є взаємодія: 1) з кислотними та амфотерними оксидами (при сплавлянні у твердому стані); 2) з кислотами; 3) розкладання під час нагрівання.<br>► Наведіть приклади рівнянь реакцій, що ілюструють зазначені загальні властивості нерозчинних основ.<br>'''Солі.''' Солі належать до складних речовин, загальну формулу яких передає об'ємне зображення:<br>
| + | ''Мал. 3. Амфотерні гідроксиди.'''''Кислоти. '''Кислоти належать до складних речовин, загальну формулу яких передає об'ємне зображення:<br> |
| - |
| + | |
| | | | |
| - | [[Image:H1034.jpg]]<br>Як бачимо, до складу солей, як і до складу основ, входять катіони металічних елементів, а інша складова частина солей — аніони кислотних залишків — властива також молекулам відповідних кислот. Таке поєднання йонів урізноманітнює хімічні властивості солей. Солі взаємодіють з: 1) металами, активнішими від металу, йони якого входять до складу солі (у розчині); 2) лугами (у розчині за умови утворення осаду); 3) іншою сіллю (у розчині за умови утворення осаду); 4) кислотами, що є сильнішими електролітами за кислоту, із сіллю якої проводять реакцію (за умови утворення осаду чи виділення газу); 5) розкладання солей деяких кислот (наприклад, карбонатів, нітратів) під час нагрівання.<br>► Наведіть приклади рівнянь реакцій, що ілюструють зазначені загальні властивості солей.<br>Номенклатура неорганічних сполук. Окрім правильного запису хімічних формул і рівнянь хімічних реакцій, не менш важливо правильно називати речовини. Ви вже обізнані із сучасною українською хімічною номенклатурою, повторити яку допоможе таблиця 1. При повторенні треба пам'ятати, що для оксидів, основ і солей існує загальне правило номенклатури.<br>'''Усі назви складаються із двох слів. Назву елемента, з атомів якого утворилася перша складова частина речовини, пишуть з малої літери в називному відмінку, а в разі прояву ним змінної валентності її без відступу зазначають після назви елемента в круглих дужках римською цифрою.'''<br> | + | <br> [[Image:H1032.jpg|350px|Кислоти. фото]] |
| - |
| + | |
| | | | |
| - | [[Image:H1035.jpg]]<br>Особливості перебігу хімічних реакцій неорганічних речовин у розчинах. Значна частина хімічних реакцій між неорганічними речовинами відбувається в розчині.<br>До якого б класу не належала неорганічна сполука, у водному розчині її хімічні властивості визначають йони, на які вона дисоціює.<br>На конкретних прикладах розглянемо цей висновок і повторимо, як пишуть повні й скорочені йонні рівняння реакцій.<br>'''Приклад 1.''' Реакція нейтралізації (взаємодія основи з кислотою):<br>
| + | ''Мал. 4. Кислоти.''<br>У розчинах кислот наявні катіони Гідрогену, що зумовлюють загальні властивості кислот. Так, кислоти взаємодіють з: 1) індикаторами; 2) [[Відео_до_уроку:_Багатоманітність_речовин._Прості_й_складні_речовини._Метали_й_неметали|металами]] (розташованими в ряді активності до водню); 3) основними й амфотерними оксидами;4) основами й амфотерними гідроксидами; 5) солями інших кислот, якщо один із продуктів реакції випадає в осад або виділяється в газоподібному стані.<br>Наведіть приклади рівнянь реакцій, що ілюструють зазначені властивості кислот.<br>Катіони Гідрогену зумовлюють загальні, кислотні залишки — специфічні властивості кислот.<br>'''Основи.''' Основи належать до складних речовин, загальну формулу яких передає об'ємне зображення:<br> [[Image:H1033.jpg|350px|Основи. фото]] |
| - |
| + | |
| | | | |
| - | [[Image:H1036.jpg]]<br>
| + | ''Мал. 5. Основи.''<br>Як вам відомо, серед основ сильними електролітами є луги. Наявність гідроксид-іонів зумовлює загальні властивості лугів: 1) дію на індикатори; 2) взаємодію з кислотними та амфотерними оксидами; 3) взаємодію з кислотами (реакція нейтралізації); 4) взаємодію з амфотерними гідроксидами; 5) взаємодію із солями, якщо один із продуктів реакції випадає в осад або виділяється в газоподібному стані.<br>Наведіть приклади рівнянь реакцій, що ілюструють зазначені загальні властивості лугів.<br>Для нерозчинних основ характерною є взаємодія: 1) з кислотними та амфотерними оксидами (при сплавлянні у твердому стані); 2) з кислотами; 3) розкладання під час нагрівання.<br>''► Наведіть приклади рівнянь реакцій, що ілюструють зазначені загальні властивості нерозчинних основ.''<br>'''Солі.''' Солі належать до складних речовин, загальну формулу яких передає об'ємне зображення:<br> |
| - |
| + | |
| | | | |
| - | ''' Приклад 2. '''Реакції йонного обміну основи, кислоти та солі із сіллю:
| + | <br> [[Image:H1034.jpg|350px|Солі. фото]] |
| - |
| + | |
| | | | |
| - | [[Image:H1037.jpg]] | + | ''Мал. 6. Солі.''<br>Як бачимо, до складу солей, як і до складу основ, входять катіони металічних елементів, а інша складова частина солей — аніони кислотних залишків — властива також молекулам відповідних кислот. Таке поєднання [[Атоми,_молекули,_йони._Хімічні_елементи,_їхні_назви_і_символи|йонів]] урізноманітнює хімічні властивості солей. Солі взаємодіють з: 1) металами, активнішими від металу, йони якого входять до складу солі (у розчині); 2) лугами (у розчині за умови утворення осаду); 3) іншою сіллю (у розчині за умови утворення осаду); 4) кислотами, що є сильнішими електролітами за кислоту, із сіллю якої проводять реакцію (за умови утворення осаду чи виділення газу); 5) розкладання солей деяких кислот (наприклад, карбонатів, нітратів) під час нагрівання.<br>''► Наведіть приклади рівнянь реакцій, що ілюструють зазначені загальні властивості солей.''<br>Номенклатура неорганічних сполук. Окрім правильного запису хімічних формул і рівнянь хімічних реакцій, не менш важливо правильно називати речовини. Ви вже обізнані із сучасною українською хімічною номенклатурою, повторити яку допоможе таблиця 1. При повторенні треба пам'ятати, що для оксидів, основ і солей існує загальне правило номенклатури.<br>'''Усі назви складаються із двох слів. Назву елемента, з атомів якого утворилася перша складова частина речовини, пишуть з малої літери в називному відмінку, а в разі прояву ним змінної валентності її без відступу зазначають після назви елемента в круглих дужках римською цифрою.'''<br> |
| - |
| + | |
| | | | |
| - | <br> | + | <br> [[Image:H1035.jpg|Номенклатура неорганічних сполук різних класів. фото]]<br>Особливості перебігу хімічних реакцій неорганічних речовин у розчинах. Значна частина хімічних реакцій між неорганічними речовинами відбувається в розчині.<br>До якого б класу не належала неорганічна сполука, у водному розчині її хімічні властивості визначають йони, на які вона дисоціює.<br>На конкретних прикладах розглянемо цей висновок і повторимо, як пишуть повні й скорочені йонні рівняння реакцій.<br>'''Приклад 1.''' Реакція нейтралізації (взаємодія основи з кислотою):<br> |
| - |
| + | |
| | | | |
| - | _______________________________________________________________________
| + | <br> [[Image:H1036.jpg|Реакція нейтралізації. фото]]<br> |
| - |
| + | |
| | | | |
| - | О. Г. Ярошенко, Біологія, 10 клас<br>Надаслано читачами інтернет-сайтів
| + | <br> ''' Приклад 2. '''Реакції йонного обміну основи, кислоти та солі із сіллю: |
| - |
| + | |
| | + | <br> [[Image:H1037.jpg|Реакція йонного обміну. фото]] |
| | | | |
| - | <br> | + | <br> <br> |
| - |
| + | |
| | | | |
| - | <br> <sub>Збірка конспектів уроків по всім класами, [[Гіпермаркет Знань - перший в світі!|домашня робота]], скачати реферати [[Хімія|з хімії]], книги та підручники згідно каленадарного плануванння [[Хімія 10 клас|з хімії для 10 класу]]</sub> | + | <br> _______________________________________________________________________ |
| - |
| + | |
| | + | <br> ''О. Г. Ярошенко, [[Хімія_10_клас|Хімія, 10 клас]]<br>Надаслано читачами інтернет-сайтів'' |
| | + | |
| | + | <br> <br> |
| | + | |
| | + | <br> <br> <sub>Збірка конспектів уроків по всім класами, [[Гіпермаркет Знань - перший в світі!|домашня робота]], скачати реферати [[Хімія|з хімії]], книги та підручники згідно каленадарного плануванння [[Хімія 10 клас|з хімії для 10 класу]]</sub> |
| | + | |
| | + | <br> |
| | | | |
| | '''<u>Зміст уроку</u>''' | | '''<u>Зміст уроку</u>''' |
| Строка 85: |
Строка 79: |
| | | | |
| | Если у вас есть исправления или предложения к данному уроку, [http://xvatit.com/index.php?do=feedback напишите нам]. | | Если у вас есть исправления или предложения к данному уроку, [http://xvatit.com/index.php?do=feedback напишите нам]. |
| - |
| |
| | | | |
| - | Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - [http://xvatit.com/forum/ Образовательный форум]. | + | <br> Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - [http://xvatit.com/forum/ Образовательный форум]. |
Версия 19:47, 13 августа 2012
Гіпермаркет Знань>>Хімія>>Хімія 10 клас>> Найважливіші класи неорганічних сполук
Загальні відомості про найважливіші класи неорганічних сполук
В основній школі ви вже вивчили такі класи неорганічних сполук, як оксиди, кислоти, основи, солі.
► Пригадайте їх визначення й розподіліть наведені формули за класами сполук, назвіть речовини: 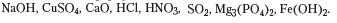
Серед неорганічних сполук переважають представники саме цих класів. Хоча, окрім них, вам відомі амфотерні гідроксиди (алюміній гідроксид, цинк гідроксид та ін.), пероксиди (гідроген пе-роксид та ін.).
Речовини, формули яких ви віднесли до одного класу, подібні за складом, проте мають відмінності щодо фізичних і хімічних властивостей. Це дає підстави для їх класифікації на окремі групи. Так, за агрегатним станом (фізична характеристика) оксиди поділяють на тверді (наприклад, фосфор(У) оксид), рідкі (наприклад, вода), газуваті (наприклад, карбон(ІУ) оксид).
Наведіть власні приклади оксидів, що за звичайних умов перебувають у різному агрегатному стані.
За здатністю розчинятися у воді кислоти, основи та солі поділяють на розчинні, малорозчинні й нерозчинні. Наприклад, сульфатна кислота добре розчинна, силікатна кислота — нерозчинна, купрум(ІІ) гідроксид — нерозчинна основа, натрій гідроксид -розчинна основа, або луг, кальцій гідроксид — малорозчинна основа, натрій хлорид — розчинна сіль, барій сульфат — нерозчинна сіль, кальцій сульфат — малорозчинна сіль. Потрібно пам'ятати, що абсолютно нерозчинних речовин не існує.
Розчинні основи утворюють мильні на дотик розчини, через що ці речовини дістали назву луги. Це: літій гідроксид, натрій гідроксид, калій гідроксид, кальцій гідроксид, барій гідроксид і деякі інші. Їх значно менше, аніж нерозчинних основ.
З-поміж різних класифікацій неорганічних речовин найуживанішою є класифікація за хімічними властивостями.
Оксиди. Вам відомо, що оксиди — бінарні сполуки елемента з Оксигеном, у яких він проявляє ступінь окиснення -2. Вони бувають солетвірні й несолетвірні. Солетвірні на підставі їх хімічних властивостей поділяють на основні, кислотні й амфотерні.
Основні оксиди — це оксиди, які взаємодіють із кислотами з утворенням солі та води.
До них належать лише оксиди металічних елементів зі ступенем окиснення +1, +2, рідше +3.

Мал. 1. Основи
► Визначте ступінь окиснення атомів металічних елементів у наведених формулах. Яка закономірність простежується між їх ступенем окиснення в оксиді й основі?
Кислотні оксиди — це оксиди, які взаємодіють із лугами з утворенням солі та води.
До них належать усі солетвірні оксиди неметалічних елементів та оксиди деяких металічних елементів із високими ступенями окиснення (+5, +6, +7).

Мал. 2. Кислоти.
Щодо кислотних оксидів і відповідних їм гідратів оксидів (ок-сигеновмісних кислот), то для них також справджується закономірність, виявлена для основ: атоми кислототвірних елементів у кислотному оксиді й відповідній йому кислоті мають однаковий ступінь окиснення.
► Напишіть формули сульфур(ІУ) оксиду і сульфур(УІ) оксиду та формули відповідних їм гідратів оксидів.
Амфотерні оксиди — оксиди, які утворюють сіль і воду при взаємодії як із кислотою, так і з лугом.
До них належить невелика кількість оксидів металічних елементів:

Мал. 3. Амфотерні гідроксиди.Кислоти. Кислоти належать до складних речовин, загальну формулу яких передає об'ємне зображення:
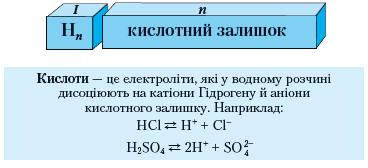
Мал. 4. Кислоти.
У розчинах кислот наявні катіони Гідрогену, що зумовлюють загальні властивості кислот. Так, кислоти взаємодіють з: 1) індикаторами; 2) металами (розташованими в ряді активності до водню); 3) основними й амфотерними оксидами;4) основами й амфотерними гідроксидами; 5) солями інших кислот, якщо один із продуктів реакції випадає в осад або виділяється в газоподібному стані.
Наведіть приклади рівнянь реакцій, що ілюструють зазначені властивості кислот.
Катіони Гідрогену зумовлюють загальні, кислотні залишки — специфічні властивості кислот.
Основи. Основи належать до складних речовин, загальну формулу яких передає об'ємне зображення:
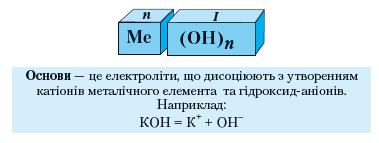
Мал. 5. Основи.
Як вам відомо, серед основ сильними електролітами є луги. Наявність гідроксид-іонів зумовлює загальні властивості лугів: 1) дію на індикатори; 2) взаємодію з кислотними та амфотерними оксидами; 3) взаємодію з кислотами (реакція нейтралізації); 4) взаємодію з амфотерними гідроксидами; 5) взаємодію із солями, якщо один із продуктів реакції випадає в осад або виділяється в газоподібному стані.
Наведіть приклади рівнянь реакцій, що ілюструють зазначені загальні властивості лугів.
Для нерозчинних основ характерною є взаємодія: 1) з кислотними та амфотерними оксидами (при сплавлянні у твердому стані); 2) з кислотами; 3) розкладання під час нагрівання.
► Наведіть приклади рівнянь реакцій, що ілюструють зазначені загальні властивості нерозчинних основ.
Солі. Солі належать до складних речовин, загальну формулу яких передає об'ємне зображення:

Мал. 6. Солі.
Як бачимо, до складу солей, як і до складу основ, входять катіони металічних елементів, а інша складова частина солей — аніони кислотних залишків — властива також молекулам відповідних кислот. Таке поєднання йонів урізноманітнює хімічні властивості солей. Солі взаємодіють з: 1) металами, активнішими від металу, йони якого входять до складу солі (у розчині); 2) лугами (у розчині за умови утворення осаду); 3) іншою сіллю (у розчині за умови утворення осаду); 4) кислотами, що є сильнішими електролітами за кислоту, із сіллю якої проводять реакцію (за умови утворення осаду чи виділення газу); 5) розкладання солей деяких кислот (наприклад, карбонатів, нітратів) під час нагрівання.
► Наведіть приклади рівнянь реакцій, що ілюструють зазначені загальні властивості солей.
Номенклатура неорганічних сполук. Окрім правильного запису хімічних формул і рівнянь хімічних реакцій, не менш важливо правильно називати речовини. Ви вже обізнані із сучасною українською хімічною номенклатурою, повторити яку допоможе таблиця 1. При повторенні треба пам'ятати, що для оксидів, основ і солей існує загальне правило номенклатури.
Усі назви складаються із двох слів. Назву елемента, з атомів якого утворилася перша складова частина речовини, пишуть з малої літери в називному відмінку, а в разі прояву ним змінної валентності її без відступу зазначають після назви елемента в круглих дужках римською цифрою.
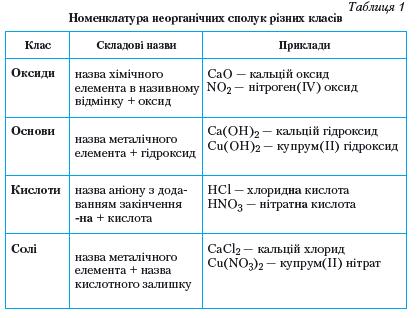
Особливості перебігу хімічних реакцій неорганічних речовин у розчинах. Значна частина хімічних реакцій між неорганічними речовинами відбувається в розчині.
До якого б класу не належала неорганічна сполука, у водному розчині її хімічні властивості визначають йони, на які вона дисоціює.
На конкретних прикладах розглянемо цей висновок і повторимо, як пишуть повні й скорочені йонні рівняння реакцій.
Приклад 1. Реакція нейтралізації (взаємодія основи з кислотою):
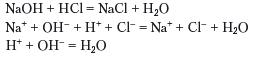
Приклад 2. Реакції йонного обміну основи, кислоти та солі із сіллю:
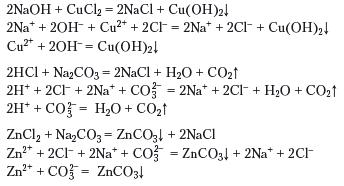
_______________________________________________________________________
О. Г. Ярошенко, Хімія, 10 клас
Надаслано читачами інтернет-сайтів
Збірка конспектів уроків по всім класами, домашня робота, скачати реферати з хімії, книги та підручники згідно каленадарного плануванння з хімії для 10 класу
Зміст уроку
 конспект уроку і опорний каркас конспект уроку і опорний каркас
 презентація уроку презентація уроку
 акселеративні методи та інтерактивні технології акселеративні методи та інтерактивні технології
 закриті вправи (тільки для використання вчителями) закриті вправи (тільки для використання вчителями)
 оцінювання
Практика оцінювання
Практика
 задачі та вправи,самоперевірка задачі та вправи,самоперевірка
 практикуми, лабораторні, кейси практикуми, лабораторні, кейси
 рівень складності задач: звичайний, високий, олімпійський рівень складності задач: звичайний, високий, олімпійський
 домашнє завдання
Ілюстрації домашнє завдання
Ілюстрації
 ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа
 реферати реферати
 фішки для допитливих фішки для допитливих
 шпаргалки шпаргалки
 гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення
 зовнішнє незалежне тестування (ЗНТ) зовнішнє незалежне тестування (ЗНТ)
 підручники основні і допоміжні підручники основні і допоміжні
 тематичні свята, девізи тематичні свята, девізи
 статті статті
 національні особливості національні особливості
 словник термінів словник термінів
 інше
Тільки для вчителів інше
Тільки для вчителів
 ідеальні уроки ідеальні уроки
 календарний план на рік календарний план на рік
 методичні рекомендації методичні рекомендації
 програми програми
 обговорення обговорення
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|