|
|
|
| (13 промежуточных версий не показаны.) | | Строка 1: |
Строка 1: |
| - | '''[[Гіпермаркет Знань - перший в світі|Гіпермаркет Знань]]>>[[Хімія|Хімія]]>>[[Хімія 11 клас|Хімія 11 клас]]>> Хімія: Теорія хімічної будови органічних сполук О. М. Бутлерова.''' | + | '''[[Гіпермаркет Знань - перший в світі!|Гіпермаркет Знань]]>>[[Хімія|Хімія]]>>[[Хімія 11 клас|Хімія 11 клас]]>> Хімія: Теорія хімічної будови органічних сполук О. М. Бутлерова.''' <metakeywords>хімія, хімія клас, 11 клас, уроки хімія, хімія</metakeywords> |
| | | | |
| - | '''Теорія хімічної будови.''' Поняття «хімічна будова» вперше ввів О. М. Бутлеров у 1861 р. Він зауважував, що властивості речовин визначаються не тільки їхнім складом (якісним і кількісним), як вважалося раніше, а й внутрішньою структурою молекул, тобто порядком з'єднання атомів один з одним, які входять до складу молекули. Цей порядок і є хімічною будовою молекули. У поняття «хімічна будова» О. М. Бутлеров включав також характер зв'язку атомів, їхній взаємний вплив один на одного. Наприклад, водень і кисень, утворивши воду, настільки змінилися від взаємного впливу, що вода вже не має властивостей ні водню, ні кисню, хоча й містить Гідроген і Оксиген, що входили до складу відповідно водню і кисню. У молекулі фенолу С6Н5ОН бензольне ядро впливає на властивості гідроксильної групи, посилюючи її кислотність (аналогія зі спиртами):
| + | '''Теорія хімічної будови.''' Поняття «хімічна будова» вперше ввів О. М. Бутлеров у 1861 р. Він зауважував, що властивості речовин визначаються не тільки їхнім складом (якісним і кількісним), як вважалося раніше, а й внутрішньою структурою молекул, тобто порядком з'єднання атомів один з одним, які входять до складу молекули. Цей порядок і є хімічною будовою молекули. У поняття «хімічна будова» О. М. [[Теория_строения_химических_соединений_А._М._Бутлерова|Бутлеров]] включав також характер зв'язку атомів, їхній взаємний вплив один на одного. Наприклад, водень і кисень, утворивши воду, настільки змінилися від взаємного впливу, що вода вже не має властивостей ні водню, ні кисню, хоча й містить Гідроген і Оксиген, що входили до складу відповідно водню і [[Практичні_роботи:_3._Добування_кисню_в_лабораторії_та_вивчення_його_властивостей|кисню]]. У молекулі фенолу С6Н5ОН бензольне ядро впливає на властивості гідроксильної групи, посилюючи її кислотність (аналогія зі спиртами): <br> |
| - | [[Файл:but1.jpg]]
| + | |
| - | <br> | + | |
| | | | |
| - | Гідроксильна група, у свою чергу, впливає на властивості бензольного ядра і полегшує заміщення в ньому атомів Гідрогену:
| + | <br> |
| | | | |
| - | <br> | + | [[Image:But1.jpg|300px|Перетворення фенолу]] <br> |
| | | | |
| - | Так, на прикладах з неорганічної та органічної хімії ми спостерігаємо взаємний вплив атомів. Хімічну будову молекул виражають за допомогою структурних формул.
| + | <br> |
| | | | |
| - | ОЛЕКСАНДР МИХАЙЛОВИЧ БУТЛЕРОВ (1828—1886) Російський хімік-органік, професор Казанського (1854—1868), а далі до кінця життя професор Петербурзького університетів, академік Петербурзької АН (з 1871). Почесний член Московського і Київського університетів. За-сновник великої школи російських хіміків-органіків. Створив і обгрунтував теорію хімічної будови. Добув ізобутилен і відкрив реакцію його полімеризації. Синтезував низку органічних сполук, серед яких перший в історії хімії синтез цукристої речовини (1861). Його праці з гідратації етилену покладено в основу одного з сучасних способів добування етилового спирту.
| + | Гідроксильна група, у свою чергу, впливає на властивості бензольного ядра і полегшує заміщення в ньому атомів Гідрогену: |
| | | | |
| - | Структурні формули передають порядок зв'язку атомів у молекулі, але не показують взаємного розміщення їх у просторі.
| + | [[Image:But2.jpg|300px|Перетворення фенолу 2]] <br> |
| | | | |
| - | Структурні формули завжди записують для окремої молекули, позначаючи рисочкою кожну зв'язувальну електронну пару. Вони справедливі тільки для речовин молекулярної будови. До таких речовин належать більшість органічних сполук, оксигеновмісні кислоти (крім НР03 і H2Si03) та деякі оксиди неметалів (CO, C02, NO, N02, S02, H20 тощо). Так, структурні формули сульфатної та ацетатної кислот | + | <br> |
| | | | |
| - | <br>
| + | Так, на прикладах з неорганічної та органічної хімії ми спостерігаємо взаємний вплив атомів. Хімічну будову молекул виражають за допомогою структурних формул. |
| | | | |
| - | передають порядок розміщення атомів у мол кислот. Структурні формули не слід плутати із застарілим графічним зображенням формул, де рисочкою позначається не спільна електронна, а ступінь окиснення елемента. Наприклад, графічне зображення формули хлориду натрію Na—СІ не можна вважати структурною формулою, оскільки NaCl — йонна сполука. В узлах її кристалічних ґраток містяться не молекули; а йони Na+ і СІ- . Між ними немає зв'язку, утвореного парою електронів, йони Na+ і СІ- утримуються разом завдяки електростатичному притяганню. Розглядаючи хімічну структуру як певну послідовність атомів у молекулі та їхній взаємний вплив один на одного, О. М. Бутлерову вдалося розкрити суть явища ізомерії, відомого ще з часів Й. Берцеліуса. Це пояснюється тим, що порядок сполучення атомів у молекулі впливає на властивості речовини.
| + | <br> |
| | | | |
| - | Ізомерія — це явище існування речовин з однаковим якісним і кількісним складом, але різною хімічною будовою, а тому й різними властивостями.
| + | '''Олександр Михайлович Бутлеров (1828—1886)'''<br> |
| | | | |
| - | Теорія хімічної будови, яка спочатку була сформульована як учення про будову органічних сполук, виявилася справедливою і для неорганічних речовин, які мають молекулярну будову. У результаті вона стала загальною теорією хімії.
| + | Російський хімік-органік, професор Казанського (1854—1868), а далі до кінця життя професор Петербурзького університетів, академік Петербурзької АН (з 1871). Почесний член Московського і Київського університетів. За-сновник великої школи російських хіміків-органіків. Створив і обгрунтував теорію хімічної будови. Добув ізобутилен і відкрив реакцію його [[Застосування_вуглеводнів._Поняття_про_полімери_на_прикладі_поліетилену._Застосування_поліетилену|полімеризації]]. Синтезував низку органічних сполук, серед яких перший в історії хімії синтез цукристої речовини (1861). Його праці з гідратації етилену покладено в основу одного з сучасних способів добування етилового спирту. |
| | | | |
| - | <br> | + | <br> |
| | | | |
| - | <br> | + | Структурні формули передають порядок зв'язку атомів у молекулі, але не показують взаємного розміщення їх у просторі. |
| | + | |
| | + | <br> |
| | + | |
| | + | Структурні формули завжди записують для окремої молекули, позначаючи рисочкою кожну зв'язувальну електронну пару. Вони справедливі тільки для речовин молекулярної будови. До таких речовин належать більшість органічних сполук, оксигеновмісні кислоти (крім НР03 і H2Si03) та деякі оксиди неметалів (CO, C02, NO, N02, S02, H20 тощо). Так, структурні формули сульфатної та ацетатної [[13._Кислоти,_їх_склад,_назви|кислот]] передають порядок розміщення атомів у молекулах кислот. |
| | + | |
| | + | <br> |
| | + | |
| | + | [[Image:But3.jpg|350px|структурні формули сульфатної та ацетатної кислот]] <br> |
| | + | |
| | + | |
| | + | |
| | + | Структурні формули не слід плутати із застарілим графічним зображенням формул, де рисочкою позначається не спільна електронна, а ступінь окиснення елемента. Наприклад, графічне зображення формули хлориду натрію Na—СІ не можна вважати структурною формулою, оскільки NaCl — йонна сполука. В узлах її кристалічних ґраток містяться не молекули; а йони Na+ і СІ- . Між ними немає зв'язку, утвореного парою [[Будова_атома._Електрон._Йон|електронів]], йони Na+ і СІ- утримуються разом завдяки електростатичному притяганню. Розглядаючи хімічну структуру як певну послідовність атомів у молекулі та їхній взаємний вплив один на одного, О. М. Бутлерову вдалося розкрити суть явища ізомерії, відомого ще з часів Й. Берцеліуса. Це пояснюється тим, що порядок сполучення атомів у молекулі впливає на властивості [[Ілюстрації_до_теми_Чисті_речовини_та_суміші._Способи_розділення_сумішей._Повітря_–_природна_суміш.|речовини]]. |
| | + | |
| | + | |
| | + | |
| | + | '''Ізомерія''' — це явище існування речовин з однаковим якісним і кількісним складом, але різною хімічною будовою, а тому й різними властивостями. |
| | + | |
| | + | |
| | + | |
| | + | Теорія хімічної будови, яка спочатку була сформульована як учення про будову органічних сполук, виявилася справедливою і для неорганічних речовин, які мають молекулярну будову. У результаті вона стала загальною теорією [[Химия|хімії]]. |
| | + | |
| | + | <br> ''Вислано читачами з інтернет-сайту''<br> |
| | + | |
| | + | |
| | + | |
| | + | '''<u>Зміст уроку</u>''' |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] [http://school.xvatit.com/index.php?title=%D0%9A%D0%B0%D1%82%D0%B5%D0%B3%D0%BE%D1%80%D0%B8%D1%8F:%D0%A2%D0%B5%D0%BE%D1%80%D1%96%D1%8F_%D1%85%D1%96%D0%BC%D1%96%D1%87%D0%BD%D0%BE%D1%97_%D0%B1%D1%83%D0%B4%D0%BE%D0%B2%D0%B8_%D0%BE%D1%80%D0%B3%D0%B0%D0%BD%D1%96%D1%87%D0%BD%D0%B8%D1%85_%D1%81%D0%BF%D0%BE%D0%BB%D1%83%D0%BA_%D0%9E._%D0%9C._%D0%91%D1%83%D1%82%D0%BB%D0%B5%D1%80%D0%BE%D0%B2%D0%B0._%D0%9A%D0%BE%D0%BD%D1%81%D0%BF%D0%B5%D0%BA%D1%82_%D1%83%D1%80%D0%BE%D0%BA%D1%83_%D1%96_%D0%BE%D0%BF%D0%BE%D1%80%D0%BD%D0%B8%D0%B9_%D0%BA%D0%B0%D1%80%D0%BA%D0%B0%D1%81 конспект уроку і опорний каркас] |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] [http://school.xvatit.com/index.php?title=%D0%9A%D0%B0%D1%82%D0%B5%D0%B3%D0%BE%D1%80%D0%B8%D1%8F:%D0%A2%D0%B5%D0%BE%D1%80%D1%96%D1%8F_%D1%85%D1%96%D0%BC%D1%96%D1%87%D0%BD%D0%BE%D1%97_%D0%B1%D1%83%D0%B4%D0%BE%D0%B2%D0%B8_%D0%BE%D1%80%D0%B3%D0%B0%D0%BD%D1%96%D1%87%D0%BD%D0%B8%D1%85_%D1%81%D0%BF%D0%BE%D0%BB%D1%83%D0%BA_%D0%9E._%D0%9C._%D0%91%D1%83%D1%82%D0%BB%D0%B5%D1%80%D0%BE%D0%B2%D0%B0._%D0%9F%D1%80%D0%B5%D0%B7%D0%B5%D0%BD%D1%82%D0%B0%D1%86%D1%96%D1%8F_%D1%83%D1%80%D0%BE%D0%BA%D1%83 презентація уроку] |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] акселеративні методи та інтерактивні технології |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] закриті вправи (тільки для використання вчителями) |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] оцінювання |
| | + | |
| | + | '''<u>Практика</u>''' |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] задачі та вправи,самоперевірка |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] практикуми, лабораторні, кейси |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] рівень складності задач: звичайний, високий, олімпійський |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] [http://school.xvatit.com/index.php?title=%D0%9A%D0%B0%D1%82%D0%B5%D0%B3%D0%BE%D1%80%D0%B8%D1%8F:%D0%A2%D0%B5%D0%BE%D1%80%D1%96%D1%8F_%D1%85%D1%96%D0%BC%D1%96%D1%87%D0%BD%D0%BE%D1%97_%D0%B1%D1%83%D0%B4%D0%BE%D0%B2%D0%B8_%D0%BE%D1%80%D0%B3%D0%B0%D0%BD%D1%96%D1%87%D0%BD%D0%B8%D1%85_%D1%81%D0%BF%D0%BE%D0%BB%D1%83%D0%BA_%D0%9E._%D0%9C._%D0%91%D1%83%D1%82%D0%BB%D0%B5%D1%80%D0%BE%D0%B2%D0%B0._%D0%94%D0%BE%D0%BC%D0%B0%D1%88%D0%BD%D1%94_%D0%B7%D0%B0%D0%B2%D0%B4%D0%B0%D0%BD%D0%BD%D1%8F домашнє завдання] |
| | + | |
| | + | '''<u>Ілюстрації</u>''' |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] [http://school.xvatit.com/index.php?title=%D0%9A%D0%B0%D1%82%D0%B5%D0%B3%D0%BE%D1%80%D0%B8%D1%8F:%D0%A2%D0%B5%D0%BE%D1%80%D1%96%D1%8F_%D1%85%D1%96%D0%BC%D1%96%D1%87%D0%BD%D0%BE%D1%97_%D0%B1%D1%83%D0%B4%D0%BE%D0%B2%D0%B8_%D0%BE%D1%80%D0%B3%D0%B0%D0%BD%D1%96%D1%87%D0%BD%D0%B8%D1%85_%D1%81%D0%BF%D0%BE%D0%BB%D1%83%D0%BA_%D0%9E._%D0%9C._%D0%91%D1%83%D1%82%D0%BB%D0%B5%D1%80%D0%BE%D0%B2%D0%B0._%D0%86%D0%BB%D1%8E%D1%81%D1%82%D1%80%D0%B0%D1%86%D1%96%D1%97:_%D0%B2%D1%96%D0%B4%D0%B5%D0%BE%D0%BA%D0%BB%D1%96%D0%BF%D0%B8,_%D0%B0%D1%83%D0%B4%D1%96%D0%BE,_%D1%84%D0%BE%D1%82%D0%BE%D0%B3%D1%80%D0%B0%D1%84%D1%96%D1%97,_%D0%B3%D1%80%D0%B0%D1%84%D1%96%D0%BA%D0%B8,_%D1%82%D0%B0%D0%B1%D0%BB%D0%B8%D1%86%D1%96,_%D0%BA%D0%BE%D0%BC%D1%96%D0%BA%D1%81%D0%B8,_%D0%BC%D1%83%D0%BB%D1%8C%D1%82%D0%B8%D0%BC%D0%B5%D0%B4%D1%96%D0%B0 ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа] |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] реферати |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фішки для допитливих |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] [http://school.xvatit.com/index.php?title=%D0%9A%D0%B0%D1%82%D0%B5%D0%B3%D0%BE%D1%80%D0%B8%D1%8F:%D0%A2%D0%B5%D0%BE%D1%80%D1%96%D1%8F_%D1%85%D1%96%D0%BC%D1%96%D1%87%D0%BD%D0%BE%D1%97_%D0%B1%D1%83%D0%B4%D0%BE%D0%B2%D0%B8_%D0%BE%D1%80%D0%B3%D0%B0%D0%BD%D1%96%D1%87%D0%BD%D0%B8%D1%85_%D1%81%D0%BF%D0%BE%D0%BB%D1%83%D0%BA_%D0%9E._%D0%9C._%D0%91%D1%83%D1%82%D0%BB%D0%B5%D1%80%D0%BE%D0%B2%D0%B0._%D0%A8%D0%BF%D0%B0%D1%80%D0%B3%D0%B0%D0%BB%D0%BA%D0%B8 шпаргалки] |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] гумор, притчі, приколи, приказки, кросворди, цитати |
| | + | |
| | + | '''<u>Доповнення</u>''' |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] зовнішнє незалежне тестування (ЗНТ) |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] підручники основні і допоміжні |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] тематичні свята, девізи |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] статті |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] національні особливості |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] словник термінів |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] інше |
| | + | |
| | + | '''<u>Тільки для вчителів</u>''' |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] [http://xvatit.com/Idealny_urok.html ідеальні уроки] |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] календарний план на рік |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] методичні рекомендації |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] програми |
| | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] [http://xvatit.com/forum/ обговорення] |
| | | | |
| | Если у вас есть исправления или предложения к данному уроку, [http://xvatit.com/index.php?do=feedback напишите нам]. | | Если у вас есть исправления или предложения к данному уроку, [http://xvatit.com/index.php?do=feedback напишите нам]. |
| | | | |
| | Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - [http://xvatit.com/forum/ Образовательный форум]. | | Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - [http://xvatit.com/forum/ Образовательный форум]. |
Текущая версия на 07:55, 14 сентября 2012
Гіпермаркет Знань>>Хімія>>Хімія 11 клас>> Хімія: Теорія хімічної будови органічних сполук О. М. Бутлерова.
Теорія хімічної будови. Поняття «хімічна будова» вперше ввів О. М. Бутлеров у 1861 р. Він зауважував, що властивості речовин визначаються не тільки їхнім складом (якісним і кількісним), як вважалося раніше, а й внутрішньою структурою молекул, тобто порядком з'єднання атомів один з одним, які входять до складу молекули. Цей порядок і є хімічною будовою молекули. У поняття «хімічна будова» О. М. Бутлеров включав також характер зв'язку атомів, їхній взаємний вплив один на одного. Наприклад, водень і кисень, утворивши воду, настільки змінилися від взаємного впливу, що вода вже не має властивостей ні водню, ні кисню, хоча й містить Гідроген і Оксиген, що входили до складу відповідно водню і кисню. У молекулі фенолу С6Н5ОН бензольне ядро впливає на властивості гідроксильної групи, посилюючи її кислотність (аналогія зі спиртами):
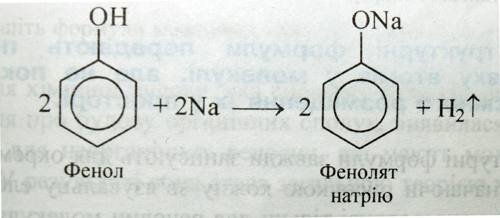
Гідроксильна група, у свою чергу, впливає на властивості бензольного ядра і полегшує заміщення в ньому атомів Гідрогену:
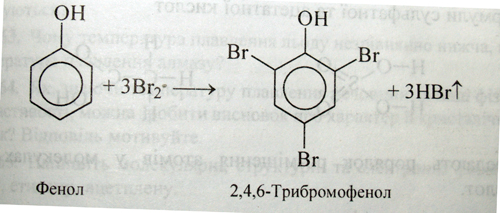
Так, на прикладах з неорганічної та органічної хімії ми спостерігаємо взаємний вплив атомів. Хімічну будову молекул виражають за допомогою структурних формул.
Олександр Михайлович Бутлеров (1828—1886)
Російський хімік-органік, професор Казанського (1854—1868), а далі до кінця життя професор Петербурзького університетів, академік Петербурзької АН (з 1871). Почесний член Московського і Київського університетів. За-сновник великої школи російських хіміків-органіків. Створив і обгрунтував теорію хімічної будови. Добув ізобутилен і відкрив реакцію його полімеризації. Синтезував низку органічних сполук, серед яких перший в історії хімії синтез цукристої речовини (1861). Його праці з гідратації етилену покладено в основу одного з сучасних способів добування етилового спирту.
Структурні формули передають порядок зв'язку атомів у молекулі, але не показують взаємного розміщення їх у просторі.
Структурні формули завжди записують для окремої молекули, позначаючи рисочкою кожну зв'язувальну електронну пару. Вони справедливі тільки для речовин молекулярної будови. До таких речовин належать більшість органічних сполук, оксигеновмісні кислоти (крім НР03 і H2Si03) та деякі оксиди неметалів (CO, C02, NO, N02, S02, H20 тощо). Так, структурні формули сульфатної та ацетатної кислот передають порядок розміщення атомів у молекулах кислот.
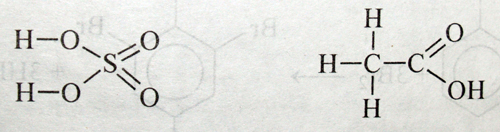
Структурні формули не слід плутати із застарілим графічним зображенням формул, де рисочкою позначається не спільна електронна, а ступінь окиснення елемента. Наприклад, графічне зображення формули хлориду натрію Na—СІ не можна вважати структурною формулою, оскільки NaCl — йонна сполука. В узлах її кристалічних ґраток містяться не молекули; а йони Na+ і СІ- . Між ними немає зв'язку, утвореного парою електронів, йони Na+ і СІ- утримуються разом завдяки електростатичному притяганню. Розглядаючи хімічну структуру як певну послідовність атомів у молекулі та їхній взаємний вплив один на одного, О. М. Бутлерову вдалося розкрити суть явища ізомерії, відомого ще з часів Й. Берцеліуса. Це пояснюється тим, що порядок сполучення атомів у молекулі впливає на властивості речовини.
Ізомерія — це явище існування речовин з однаковим якісним і кількісним складом, але різною хімічною будовою, а тому й різними властивостями.
Теорія хімічної будови, яка спочатку була сформульована як учення про будову органічних сполук, виявилася справедливою і для неорганічних речовин, які мають молекулярну будову. У результаті вона стала загальною теорією хімії.
Вислано читачами з інтернет-сайту
Зміст уроку
 конспект уроку і опорний каркас конспект уроку і опорний каркас
 презентація уроку презентація уроку
 акселеративні методи та інтерактивні технології акселеративні методи та інтерактивні технології
 закриті вправи (тільки для використання вчителями) закриті вправи (тільки для використання вчителями)
 оцінювання
Практика оцінювання
Практика
 задачі та вправи,самоперевірка задачі та вправи,самоперевірка
 практикуми, лабораторні, кейси практикуми, лабораторні, кейси
 рівень складності задач: звичайний, високий, олімпійський рівень складності задач: звичайний, високий, олімпійський
 домашнє завдання
Ілюстрації домашнє завдання
Ілюстрації
 ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа
 реферати реферати
 фішки для допитливих фішки для допитливих
 шпаргалки шпаргалки
 гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення
 зовнішнє незалежне тестування (ЗНТ) зовнішнє незалежне тестування (ЗНТ)
 підручники основні і допоміжні підручники основні і допоміжні
 тематичні свята, девізи тематичні свята, девізи
 статті статті
 національні особливості національні особливості
 словник термінів словник термінів
 інше
Тільки для вчителів інше
Тільки для вчителів
 ідеальні уроки ідеальні уроки
 календарний план на рік календарний план на рік
 методичні рекомендації методичні рекомендації
 програми програми
 обговорення обговорення
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|













