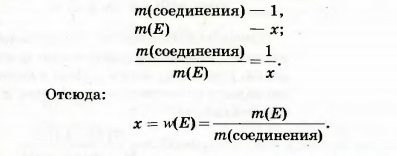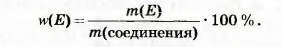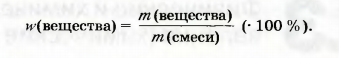|
|
|
| (2 промежуточные версии не показаны) | | Строка 1: |
Строка 1: |
| - | <metakeywords>Гипермаркет Знаний - первый в мире!, Гипермаркет Знаний, Химия, 7 класс, Массовая доля элемента в сложном веществе</metakeywords> | + | <metakeywords>Гипермаркет Знаний - первый в мире!, Гипермаркет Знаний, Химия, 7 класс, Массовая доля элемента в сложном веществе, вещество, элемента, формула, Оксигена, молекул</metakeywords> |
| | | | |
| | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 7 класс|Химия 7 класс]]>> Массовая доля элемента в сложном веществе<br> ''' | | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 7 класс|Химия 7 класс]]>> Массовая доля элемента в сложном веществе<br> ''' |
| | | | |
| - | <br> Массовая доля элемента в сложном веществе<br><br>Материал параграфа поможет вам:<br><br>> выяснить, что такое массовая доля элемента в соединении, и определять ее значение;<br>> рассчитывать массу элемента в определенной массе соединения, исходя из массовой доли элемента;<br>> правильно оформлять решение химических задач.<br><br>Каждое сложное вещество (химическое соединение) образовано несколькими элементами. Знать содержание элементов в соединении необходимо для его эффективного использования. Например, лучшим азотным удобрением считают то, в котором содержится наибольшее количество Нитрогена (этот элемент необходим растениям). Аналогично оценивают качество металлической руды, определяя, насколько она «богата» на металлический элемент.<br><br>Содержание элемента в соединении характеризуют его массовой долей. Эту величину обозначают латинской буквой w («дубль-вэ»).<br><br>Выведем формулу для вычисления массовой доли элемента в соединении по известным массам соединения и элемента. Обозначим массовую долю элемента буквой х. Приняв во внимание, что масса соединения — это целое, а масса элемента — часть от целого, составляем пропорцию:<br><br>карт<br><br>Массовая доля элемента в соединении — это отношение массы элемента к соответствующей массе соединения.<br><br>Заметим, что массы элемента и соединения нужно брать в одинаковых единицах измерения (например, в граммах).<br><br>Это интересно <br><br>В двух соединениях Сульфура— SO2 и MoS3 — массовые доли элементов одинаковы и составляют по 0,5 (или 50 %).<br><br>Массовая доля не имеет размерности. Ее часто выражают в процентах. В этом случае формула принимает такой вид:<br><br>карт<br><br><br>Очевидным является то, что сумма массовых долей всех элементов в соединении равна 1 (или 100 % ).<br><br>Приведем несколько примеров решения расчетных задач. Условие задачи и ее решение оформляют таким образом. Лист тетради или классную доску <br>делят вертикальной линией на две неодинаковые части. В левой, меньшей, части сокращенно записывают условие задачи, проводят горизонтальную линию и под ней указывают то, что нужно найти <br>или вычислить. В правой части записывают математические формулы, объяснение, расчеты и ответ.<br><br>Задача 1. В 80 г соединения содержится 32 г Оксигена. Вычислить массовую долю Оксигена в соединении.<br><br>карт<br><br>Массовую долю элемента в соединении также вычисляют, используя химическую формулу соединения. Поскольку массы атомов и молекул пропорциональны относительным атомным и молекулярным массам, то<br><br>карт<br><br>где N(E) — количество атомов элемента в формуле соединения.<br><br>Задача 2. Рассчитать массовые доли элементов в метане CH4.<br><br>карт<br><br>карт<br><br>По известной массовой доле элемента можно рассчитать массу элемента, которая содержится в определенной массе соединения. Из математической формулы для массовой доли элемента вытекает:<br><br>m(E) = w(E) • m(соединения).<br><br>Задача 3. Какая масса Нитрогена содержится в аммиачной селитре <br>(азотное удобрение) массой I кг, если массовая доля этого <br>элемента в соединении равна 0,35?<br><br>rfhn<br><br>Понятие «массовая доля» используют для характеристики количественного состава смесей веществ. Соответствующая математическая формула имеет <br>такой вид:<br><br>rfhn<br><br>Выводы<br><br>Массовая доля элемента в соединении — это отношение массы элемента к соответствующей массе соединения.<br><br>Массовую долю элемента в соединении вычисляют по известным массам элемента и соединения или по его химической формуле.<br><br>Зная массовую долю элемента, можно рассчитать его массу, которая содержится в определенной массе соединения.<br><br>?<br>92. Как вычислить массовую долю элемента в соединении, если известны:<br>а) масса элемента и соответствующая масса соединения; б) химиче<br>ская формула соединения?<br><br>93. В 20 г вещества содержится 16 г Брома. Найдите массовую долю этого <br>элемента в веществе, выразив ее обычной дробью, десятичной дробью <br>и в процентах.<br><br>94. Вычислите (желательно устно) массовые доли элементов в соединениях <br>с такими формулами: SO2, LiH, CrO3.<br><br>95. Сопоставляя формулы веществ, а также значения относительных атом<br>ных масс, определите, в каком из веществ каждой пары массовая доля <br>первого в формуле элемента больше: a) N2O, NO; б) CO, CO2; в) B2O3, B2S3.<br><br>96. Выполните необходимые вычисления для уксусной кислоты CH3COOH <br>и глицерина C3H5(OH)3 и заполните таблицу:<br><br>5х3<br>CxHyOz H(CxHk Oz) w(C) W(H) W(O)<br><br>97. Массовая доля Нитрогена в некотором соединении равна 28 %. В ка<br>кой массе соединения содержится 56 г Нитрогена?<br><br>98. Массовая доля Кальция в его соединении с Гидрогеном равна 0,952. <br>Определите массу Гидрогена, которая содержится в 20 г соединения.<br><br>99. Смешали 100 г цемента и 150 г песка. Какова массовая доля цемента <br>в приготовленной смеси? | + | <br> '''Массовая доля элемента в сложном веществе<br><br>'''<u>'''Материал параграфа поможет вам:'''</u> |
| | + | |
| | + | ''> выяснить, что такое массовая доля элемента в соединении, и определять ее значение;<br>> рассчитывать массу элемента в определенной массе соединения, исходя из массовой доли элемента;<br>> правильно оформлять решение химических задач.''<br><br>Каждое сложное '''[[Відео до уроку: Речовини. Чисті речовини і суміші|вещество]]''' (химическое соединение) образовано несколькими элементами. Знать содержание элементов в соединении необходимо для его эффективного использования. Например, лучшим азотным удобрением считают то, в котором содержится наибольшее количество Нитрогена (этот элемент необходим растениям). Аналогично оценивают качество металлической руды, определяя, насколько она «[http://xvatit.com/busines/ '''богата''']» на металлический элемент. |
| | + | |
| | + | Содержание '''[[Презентація уроку «Атоми, молекули, йони. Хімічні елементи, їхні назви і символи»|элемента]]''' в соединении характеризуют его массовой долей. Эту величину обозначают латинской буквой w («дубль-вэ»). |
| | + | |
| | + | Выведем формулу для вычисления массовой доли элемента в соединении по известным массам соединения и элемента. Обозначим массовую долю элемента буквой х. Приняв во внимание, что масса соединения — это целое, а масса элемента — часть от целого, составляем пропорцию:<br><br>[[Image:18.09-044.jpg|480px|Пропорция]]<br><br>Массовая доля элемента в соединении — это отношение массы элемента к соответствующей массе соединения. |
| | + | |
| | + | Заметим, что массы элемента и соединения нужно брать в одинаковых единицах измерения (например, в граммах).<br><br><u>'''Это интересно'''</u> |
| | + | |
| | + | В двух соединениях Сульфура— SO<sub>2</sub> и MoS<sub>3</sub> — массовые доли элементов одинаковы и составляют по 0,5 (или 50 %). |
| | + | |
| | + | Массовая доля не имеет размерности. Ее часто выражают в процентах. В этом случае '''[[Хімічні формули речовин. Повні уроки|формула]]''' принимает такой вид: |
| | + | |
| | + | <br>[[Image:18.09-045.jpg|320px|Формула]]<br><br>Очевидным является то, что сумма массовых долей всех элементов в соединении равна 1 (или 100 % ). |
| | + | |
| | + | Приведем несколько примеров решения расчетных задач. Условие задачи и ее решение оформляют таким образом. Лист тетради или классную доску делят вертикальной линией на две неодинаковые части. В левой, меньшей, части сокращенно записывают условие задачи, проводят горизонтальную линию и под ней указывают то, что нужно найти или вычислить. В правой части записывают математические формулы, объяснение, расчеты и ответ.<br><br>'''''Задача 1.''''' В 80 г соединения содержится 32 г [[Відео до уроку: Поширеність та колообіг Оксигену в природі. Застосування кисню, його біологічна роль|'''Оксигена''']]. Вычислить массовую долю Оксигена в соединении.<br><br>[[Image:18.09-046.jpg|550px|Задача]]<br><br>Массовую долю элемента в соединении также вычисляют, используя химическую формулу соединения. Поскольку массы атомов и [[Тема 34. Тіла, речовини , молекули|'''молекул''']] пропорциональны относительным атомным и молекулярным массам, то<br><br>[[Image:18.09-047.jpg|240px|Задача]]<br><br>где N(E) — количество атомов элемента в формуле соединения.<br><br>'''''Задача 2.''''' Рассчитать массовые доли элементов в метане CH<sub>4</sub>. |
| | + | |
| | + | <br>[[Image:18.09-048.jpg|550px|Задача]]<br>[[Image:18.09-049.jpg|550px|Задача]]<br><br>По известной массовой доле элемента можно рассчитать массу элемента, которая содержится в определенной массе соединения. Из математической формулы для массовой доли элемента вытекает:<br><br>'''m(E) = w(E) • m(соединения).'''<br><br>'''''Задача 3.''''' Какая масса Нитрогена содержится в аммиачной селитре (азотное удобрение) массой 1 кг, если массовая доля этого элемента в соединении равна 0,35?<br><br>[[Image:18.09-050.jpg|550px|Задача]]<br><br>Понятие «массовая доля» используют для характеристики количественного состава смесей веществ. Соответствующая математическая формула имеет такой вид: |
| | + | |
| | + | [[Image:18.09-051.jpg|420px|Формула]]<br><br><u>'''Выводы'''</u> |
| | + | |
| | + | Массовая доля элемента в соединении — это отношение массы элемента к соответствующей массе соединения. |
| | + | |
| | + | Массовую долю элемента в соединении вычисляют по известным массам элемента и соединения или по его химической формуле. |
| | + | |
| | + | Зная массовую долю элемента, можно рассчитать его массу, которая содержится в определенной массе соединения.<br><br>'''?'''<br>''92. Как вычислить массовую долю элемента в соединении, если известны: а) масса элемента и соответствующая масса соединения; б) химическая формула соединения?'' |
| | + | |
| | + | ''93. В 20 г вещества содержится 16 г Брома. Найдите массовую долю этого элемента в веществе, выразив ее обычной дробью, десятичной дробью и в процентах.'' |
| | + | |
| | + | ''94. Вычислите (желательно устно) массовые доли элементов в соединениях с такими формулами: SO<sub>2</sub>, LiH, CrO<sub>3</sub>.'' |
| | + | |
| | + | ''95. Сопоставляя формулы веществ, а также значения относительных атом ных масс, определите, в каком из веществ каждой пары массовая доля первого в формуле элемента больше: '' |
| | + | |
| | + | ''a) N<sub>2</sub>O, NO; б) CO, CO<sub>2</sub>; в) B<sub>2</sub>O<sub>3</sub>, B<sub>2</sub>S<sub>3</sub>.<br><br>96. Выполните необходимые вычисления для уксусной кислоты CH<sub>3</sub>COOH и глицерина C<sub>3</sub>H<sub>5</sub>(OH)<sub>3</sub> и заполните таблицу:'' |
| | + | |
| | + | {| width="498" border="1" cellspacing="1" cellpadding="1" |
| | + | |- |
| | + | | C<sub>x</sub>H<sub>y</sub>O<sub>z</sub> |
| | + | | M<sub>r</sub>(C<sub>x</sub>H<sub>y</sub> O<sub>z</sub>) |
| | + | | w(C) |
| | + | | W(H) |
| | + | | W(O) |
| | + | |- |
| | + | | |
| | + | | |
| | + | | |
| | + | | |
| | + | | |
| | + | |- |
| | + | | |
| | + | | |
| | + | | |
| | + | | |
| | + | | |
| | + | |} |
| | + | |
| | + | ''<br>97. Массовая доля Нитрогена в некотором соединении равна 28 %. В какой массе соединения содержится 56 г Нитрогена?'' |
| | + | |
| | + | ''98. Массовая доля Кальция в его соединении с Гидрогеном равна 0,952. Определите массу Гидрогена, которая содержится в 20 г соединения.'' |
| | + | |
| | + | ''99. Смешали 100 г цемента и 150 г песка. Какова массовая доля цемента в приготовленной смеси?'' |
| | | | |
| | <br> | | <br> |
Текущая версия на 17:55, 18 сентября 2012
Гипермаркет знаний>>Химия>>Химия 7 класс>> Массовая доля элемента в сложном веществе
Массовая доля элемента в сложном веществе
Материал параграфа поможет вам:
> выяснить, что такое массовая доля элемента в соединении, и определять ее значение;
> рассчитывать массу элемента в определенной массе соединения, исходя из массовой доли элемента;
> правильно оформлять решение химических задач.
Каждое сложное вещество (химическое соединение) образовано несколькими элементами. Знать содержание элементов в соединении необходимо для его эффективного использования. Например, лучшим азотным удобрением считают то, в котором содержится наибольшее количество Нитрогена (этот элемент необходим растениям). Аналогично оценивают качество металлической руды, определяя, насколько она «богата» на металлический элемент.
Содержание элемента в соединении характеризуют его массовой долей. Эту величину обозначают латинской буквой w («дубль-вэ»).
Выведем формулу для вычисления массовой доли элемента в соединении по известным массам соединения и элемента. Обозначим массовую долю элемента буквой х. Приняв во внимание, что масса соединения — это целое, а масса элемента — часть от целого, составляем пропорцию:
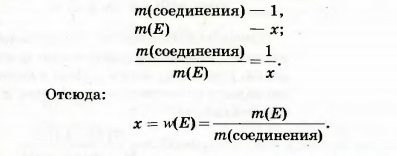
Массовая доля элемента в соединении — это отношение массы элемента к соответствующей массе соединения.
Заметим, что массы элемента и соединения нужно брать в одинаковых единицах измерения (например, в граммах).
Это интересно
В двух соединениях Сульфура— SO2 и MoS3 — массовые доли элементов одинаковы и составляют по 0,5 (или 50 %).
Массовая доля не имеет размерности. Ее часто выражают в процентах. В этом случае формула принимает такой вид:
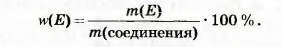
Очевидным является то, что сумма массовых долей всех элементов в соединении равна 1 (или 100 % ).
Приведем несколько примеров решения расчетных задач. Условие задачи и ее решение оформляют таким образом. Лист тетради или классную доску делят вертикальной линией на две неодинаковые части. В левой, меньшей, части сокращенно записывают условие задачи, проводят горизонтальную линию и под ней указывают то, что нужно найти или вычислить. В правой части записывают математические формулы, объяснение, расчеты и ответ.
Задача 1. В 80 г соединения содержится 32 г Оксигена. Вычислить массовую долю Оксигена в соединении.

Массовую долю элемента в соединении также вычисляют, используя химическую формулу соединения. Поскольку массы атомов и молекул пропорциональны относительным атомным и молекулярным массам, то
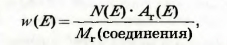
где N(E) — количество атомов элемента в формуле соединения.
Задача 2. Рассчитать массовые доли элементов в метане CH4.


По известной массовой доле элемента можно рассчитать массу элемента, которая содержится в определенной массе соединения. Из математической формулы для массовой доли элемента вытекает:
m(E) = w(E) • m(соединения).
Задача 3. Какая масса Нитрогена содержится в аммиачной селитре (азотное удобрение) массой 1 кг, если массовая доля этого элемента в соединении равна 0,35?

Понятие «массовая доля» используют для характеристики количественного состава смесей веществ. Соответствующая математическая формула имеет такой вид:
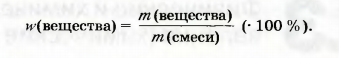
Выводы
Массовая доля элемента в соединении — это отношение массы элемента к соответствующей массе соединения.
Массовую долю элемента в соединении вычисляют по известным массам элемента и соединения или по его химической формуле.
Зная массовую долю элемента, можно рассчитать его массу, которая содержится в определенной массе соединения.
?
92. Как вычислить массовую долю элемента в соединении, если известны: а) масса элемента и соответствующая масса соединения; б) химическая формула соединения?
93. В 20 г вещества содержится 16 г Брома. Найдите массовую долю этого элемента в веществе, выразив ее обычной дробью, десятичной дробью и в процентах.
94. Вычислите (желательно устно) массовые доли элементов в соединениях с такими формулами: SO2, LiH, CrO3.
95. Сопоставляя формулы веществ, а также значения относительных атом ных масс, определите, в каком из веществ каждой пары массовая доля первого в формуле элемента больше:
a) N2O, NO; б) CO, CO2; в) B2O3, B2S3.
96. Выполните необходимые вычисления для уксусной кислоты CH3COOH и глицерина C3H5(OH)3 и заполните таблицу:
| CxHyOz
| Mr(CxHy Oz)
| w(C)
| W(H)
| W(O)
|
|
|
|
|
|
|
|
|
|
|
|
|
97. Массовая доля Нитрогена в некотором соединении равна 28 %. В какой массе соединения содержится 56 г Нитрогена?
98. Массовая доля Кальция в его соединении с Гидрогеном равна 0,952. Определите массу Гидрогена, которая содержится в 20 г соединения.
99. Смешали 100 г цемента и 150 г песка. Какова массовая доля цемента в приготовленной смеси?
Попель П. П., Крикля Л. С., Хімія: Підруч. для 7 кл. загальноосвіт. навч. закл. — К.: ВЦ «Академія», 2008. — 136 с.: іл.
Содержание урока
 конспект урока и опорный каркас конспект урока и опорный каркас
 презентация урока презентация урока
 интерактивные технологии интерактивные технологии
 акселеративные методы обучения
Практика акселеративные методы обучения
Практика
 тесты, тестирование онлайн тесты, тестирование онлайн
 задачи и упражнения задачи и упражнения
 домашние задания домашние задания
 практикумы и тренинги практикумы и тренинги
 вопросы для дискуссий в классе
Иллюстрации вопросы для дискуссий в классе
Иллюстрации
 видео- и аудиоматериалы видео- и аудиоматериалы
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 комиксы, притчи, поговорки, кроссворды, анекдоты, приколы, цитаты
Дополнения комиксы, притчи, поговорки, кроссворды, анекдоты, приколы, цитаты
Дополнения
 рефераты рефераты
 шпаргалки шпаргалки
 фишки для любознательных фишки для любознательных
 статьи (МАН) статьи (МАН)
 литература основная и дополнительная литература основная и дополнительная
 словарь терминов
Совершенствование учебников и уроков словарь терминов
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 календарные планы календарные планы
 учебные программы учебные программы
 методические рекомендации методические рекомендации
 обсуждения обсуждения
 Идеальные уроки-кейсы Идеальные уроки-кейсы
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|