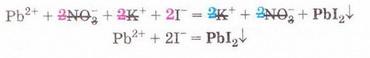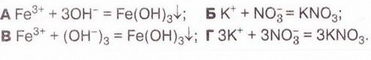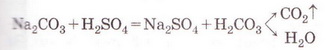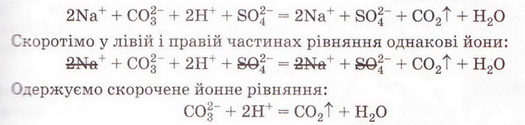|
|
|
| Строка 21: |
Строка 21: |
| | Скласти йонне рівняння досить просто. Виконаймо дослід і розгляньмо послідовність складання йонного рівняння на прикладі реакції між калій йодидом і плюмбум(ІІ) нітратом у розчині. Про її перебіг свідчить утворення яскраво-жовтого осаду плюмбум(ІІ) йодиду (мал. 12.1).<br> | | Скласти йонне рівняння досить просто. Виконаймо дослід і розгляньмо послідовність складання йонного рівняння на прикладі реакції між калій йодидом і плюмбум(ІІ) нітратом у розчині. Про її перебіг свідчить утворення яскраво-жовтого осаду плюмбум(ІІ) йодиду (мал. 12.1).<br> |
| | | | |
| - | [[Image:Chemistry_80.jpg]] | + | [[Image:Chemistry 80.jpg]] |
| | | | |
| - | Спочатку запишімо рівняння реакції без урахування дисоціації електролітів:<br>Pb(NO<sub>3</sub>)<sub>2</sub> + 2KI = 2KNO<sub>3</sub> + Pbl<sub>2</sub> [[Image:Znak_2.jpg]]<br> | + | Спочатку запишімо рівняння реакції без урахування дисоціації електролітів:<br>Pb(NO<sub>3</sub>)<sub>2</sub> + 2KI = 2KNO<sub>3</sub> + Pbl<sub>2</sub> [[Image:Znak 2.jpg]]<br> |
| | | | |
| | Аби скласти рівняння цієї реакції у йонній формі, слід зважити на те, що електроліти у розчині дисоціюють на йони. За таблицею «Розчинність кислот, основ і солей у воді» (див. додаток) визначмо, які з-поміж реагентів є сильними електролітами. Обидві розчинні солі - плюмбум(ІІ) нітрат і калій йодид - у водному розчині практично повністю дисоціюють за йони. Тож запишімо їхні формули у йонному вигляді:<br> | | Аби скласти рівняння цієї реакції у йонній формі, слід зважити на те, що електроліти у розчині дисоціюють на йони. За таблицею «Розчинність кислот, основ і солей у воді» (див. додаток) визначмо, які з-поміж реагентів є сильними електролітами. Обидві розчинні солі - плюмбум(ІІ) нітрат і калій йодид - у водному розчині практично повністю дисоціюють за йони. Тож запишімо їхні формули у йонному вигляді:<br> |
| Строка 29: |
Строка 29: |
| | РЬ<sup>2+</sup> + 2NO<sup>-</sup><sub>3 </sub>+ 2К<sup>+ </sup>+ 2I<sup>-</sup><br> | | РЬ<sup>2+</sup> + 2NO<sup>-</sup><sub>3 </sub>+ 2К<sup>+ </sup>+ 2I<sup>-</sup><br> |
| | | | |
| - | Проаналізуймо, які з цих йонів взаємодіятимуть між собою з огляду знаки їхніх зарядів. Це потрібно, аби пересвідчитися, що ми правильно визначили продукти реакції. Електростатичні сили зумовлюватимуть притягування різнойменних і відштовхування однойменно заряджених йонів (мал. 12.2). | + | Проаналізуймо, які з цих йонів взаємодіятимуть між собою з огляду знаки їхніх зарядів. Це потрібно, аби пересвідчитися, що ми правильно визначили продукти реакції. Електростатичні сили зумовлюватимуть притягування різнойменних і відштовхування однойменно заряджених йонів (мал. 12.2). |
| | | | |
| - | [[Image:Chemistry_81.jpg]]<br>Отже, продукти реакції - калій нітрат і плюмбум(ІІ) йодид. Калій нітрат - сильний електроліт, повністю дисоціює, тому у правій частині рівняння записуємо катіони Калію та нітрат-аніони. Плюмбум(ІІ) йодид практично нерозчинний, тож його формулу залишаємо незмінною<br> | + | [[Image:Chemistry 81.jpg]]<br>Отже, продукти реакції - калій нітрат і плюмбум(ІІ) йодид. Калій нітрат - сильний електроліт, повністю дисоціює, тому у правій частині рівняння записуємо катіони Калію та нітрат-аніони. Плюмбум(ІІ) йодид практично нерозчинний, тож його формулу залишаємо незмінною<br> |
| | | | |
| - | РЬ<sup>2+</sup> + 2NO<sup>-</sup><sub>3 </sub>+ 2К<sup>+</sup> + 2I<sup>-</sup> = 2K<sup>+</sup>+ 2N0<sup>-</sup><sub>3</sub> + Рbl<sub>2</sub> [[Image:Znak_2.jpg]]<br> | + | РЬ<sup>2+</sup> + 2NO<sup>-</sup><sub>3 </sub>+ 2К<sup>+</sup> + 2I<sup>-</sup> = 2K<sup>+</sup>+ 2N0<sup>-</sup><sub>3</sub> + Рbl<sub>2</sub> [[Image:Znak 2.jpg]]<br> |
| | | | |
| | Зверніть увагу: у йонному рівнянні коефіцієнти перед формулами кожного з йонів записують з урахуванням індексів у формулах електролітів та коефіцієнтів перед ними. Приміром, унаслідок дисоціації однієї формульної одиниці плюмбум(ІІ) нітрату утворюється один катіон Плюмбуму(ІІ) і два нітрат-аніони. А під час дисоціації двох формульних одиниць калій йодиду утворюються два катіони Калію та два йодид-аніони.<br> | | Зверніть увагу: у йонному рівнянні коефіцієнти перед формулами кожного з йонів записують з урахуванням індексів у формулах електролітів та коефіцієнтів перед ними. Приміром, унаслідок дисоціації однієї формульної одиниці плюмбум(ІІ) нітрату утворюється один катіон Плюмбуму(ІІ) і два нітрат-аніони. А під час дисоціації двох формульних одиниць калій йодиду утворюються два катіони Калію та два йодид-аніони.<br> |
| | | | |
| - | Очевидно, що в лівій і правій частинах йонного рівняння є однакові йони (які саме?). Оскільки вони не беруть участі в реакції, їхні формули ножна скоротити: | + | Очевидно, що в лівій і правій частинах йонного рівняння є однакові йони (які саме?). Оскільки вони не беруть участі в реакції, їхні формули ножна скоротити: |
| | | | |
| - | [[Image:Chemistry_81_2.jpg]] | + | [[Image:Chemistry 81 2.jpg]] |
| | | | |
| | Вилучімо з лівої та правої частин рівняння формули катіонів Калію й - нітрат-аніонів, аби одержати скорочене йонне рівняння. У ньому записані тільки ті частинки, які реально взаємодіють у розчині з утворенням яскраво-жовтого осаду плюмбум(ІІ) йодиду. Тобто скорочене йонне рівняння відбиває суть реакції обміну між електролітами у розчині. Воно показує, які йони взаємодіють і яка речовина є продуктом реакції.<br> | | Вилучімо з лівої та правої частин рівняння формули катіонів Калію й - нітрат-аніонів, аби одержати скорочене йонне рівняння. У ньому записані тільки ті частинки, які реально взаємодіють у розчині з утворенням яскраво-жовтого осаду плюмбум(ІІ) йодиду. Тобто скорочене йонне рівняння відбиває суть реакції обміну між електролітами у розчині. Воно показує, які йони взаємодіють і яка речовина є продуктом реакції.<br> |
| Строка 47: |
Строка 47: |
| | <u>Завдання</u><br> | | <u>Завдання</u><br> |
| | | | |
| - | Виберіть скорочене йонне рівняння, яке відповідає реакції між ферум(ІІІ) нітратом і калій гідроксидом у розчині: | + | Виберіть скорочене йонне рівняння, яке відповідає реакції між ферум(ІІІ) нітратом і калій гідроксидом у розчині: |
| | | | |
| - | [[Image:Chemistry_81_3.jpg]]<br> | + | [[Image:Chemistry 81 3.jpg]]<br> |
| | | | |
| | З'ясуймо, за яких ще умов, окрім утворення осаду, реакції обміну у розчинах електролітів будуть необоротними - тобто відбуватимуться до кінця. Дослідімо реакцію між натрій гідроксидом і нітратною кислотою у розчині. Наочно пересвідчитися у перебігу реакції нейтралізації допоможе застосування індикатора. До розчину натрій гідроксиду добавмо кілька крапель спиртового розчину фенолфталеїну - специфічного індикатора лужного середовища. Ви, звичайно, пам'ятаєте, що під дією гідроксид-аніонів фенолфталеїн набуває малинового забарвлення. Краплями, щоразу обережно струшуючи колбу, добавлятимемо розбавлену нітратну кислоту (мал. 12.3), аж поки малинове забарвлення фенолфталеїну не зникне. Знебарвлення розчину свідчить про нейтралізацію лугу кислотою:<br> | | З'ясуймо, за яких ще умов, окрім утворення осаду, реакції обміну у розчинах електролітів будуть необоротними - тобто відбуватимуться до кінця. Дослідімо реакцію між натрій гідроксидом і нітратною кислотою у розчині. Наочно пересвідчитися у перебігу реакції нейтралізації допоможе застосування індикатора. До розчину натрій гідроксиду добавмо кілька крапель спиртового розчину фенолфталеїну - специфічного індикатора лужного середовища. Ви, звичайно, пам'ятаєте, що під дією гідроксид-аніонів фенолфталеїн набуває малинового забарвлення. Краплями, щоразу обережно струшуючи колбу, добавлятимемо розбавлену нітратну кислоту (мал. 12.3), аж поки малинове забарвлення фенолфталеїну не зникне. Знебарвлення розчину свідчить про нейтралізацію лугу кислотою:<br> |
| Строка 55: |
Строка 55: |
| | NaOH + HNO<sub>3</sub> = NaN0<sub>3</sub> + Н<sub>2</sub>0<br> | | NaOH + HNO<sub>3</sub> = NaN0<sub>3</sub> + Н<sub>2</sub>0<br> |
| | | | |
| - | [[Image:Chemistry_82.jpg]] | + | [[Image:Chemistry 82.jpg]] |
| | | | |
| - | За допомогою таблиці розчинності (див. додаток) визначмо, що з чотирьох речовин - реагентів і продуктів реакції - до сильних електролітів належать три. Це натрій гідроксид (луг), нітратна кислота і натрій нітрат розчинна сіль. Вода - дуже слабкий електроліт, тож практично не дисоціює. З огляду на це, запишімо повне йонне рівняння реакції між натрій гідроксидом і нітратною кислотою у розчині: | + | За допомогою таблиці розчинності (див. додаток) визначмо, що з чотирьох речовин - реагентів і продуктів реакції - до сильних електролітів належать три. Це натрій гідроксид (луг), нітратна кислота і натрій нітрат розчинна сіль. Вода - дуже слабкий електроліт, тож практично не дисоціює. З огляду на це, запишімо повне йонне рівняння реакції між натрій гідроксидом і нітратною кислотою у розчині: |
| | | | |
| - | [[Image:Chemistry_82_2.jpg]] | + | [[Image:Chemistry 82 2.jpg]] |
| | | | |
| | Очевидно, що молекули води утворюються внаслідок взаємодії у розчині катіонів Гідрогену й гідроксид-аніонів.<br>Отже, реакція обміну між електролітами у розчині практично необоротна, якщо один з продуктів - дуже слабкий електроліт, наприклад вода, або інша малодисоційована речовина.<br> | | Очевидно, що молекули води утворюються внаслідок взаємодії у розчині катіонів Гідрогену й гідроксид-аніонів.<br>Отже, реакція обміну між електролітами у розчині практично необоротна, якщо один з продуктів - дуже слабкий електроліт, наприклад вода, або інша малодисоційована речовина.<br> |
| Строка 75: |
Строка 75: |
| | За малюнком 12.4 опишіть на макрорівні хімічну реакцію між натрій карбонатом і сульфатною кислотою у розчині. Поясніть, чому не можна для проведення досліду брати розчини соди та кислоти у більших (мал. 12.4, 1), ніж вказано в інструкції (мал. 12.4, 2), кількостях.<br> | | За малюнком 12.4 опишіть на макрорівні хімічну реакцію між натрій карбонатом і сульфатною кислотою у розчині. Поясніть, чому не можна для проведення досліду брати розчини соди та кислоти у більших (мал. 12.4, 1), ніж вказано в інструкції (мал. 12.4, 2), кількостях.<br> |
| | | | |
| - | [[Image:Chemistry_83.jpg]] | + | [[Image:Chemistry 83.jpg]] |
| | | | |
| - | Скориставшись таблицею розчинності і див. додаток), запишімо рівняння реакції (пам'ятаймо, карбонатна кислота нестійка, існує у розчині як гідрат): | + | Скориставшись таблицею розчинності і див. додаток), запишімо рівняння реакції (пам'ятаймо, карбонатна кислота нестійка, існує у розчині як гідрат): |
| | | | |
| - | [[Image:Chemistry_83_1.jpg]] | + | [[Image:Chemistry 83 1.jpg]] |
| | | | |
| | З-поміж п'яти речовин - реагентів і продуктів реакції - до сильних електролітів належать три. Це натрій карбонат, сульфатна кислота і натрій сульфат. Вода - дуже слабкий електроліт, а карбон(IV) оксид (вуглекислий газ) видаляється зі сфери реакції.<br> | | З-поміж п'яти речовин - реагентів і продуктів реакції - до сильних електролітів належать три. Це натрій карбонат, сульфатна кислота і натрій сульфат. Вода - дуже слабкий електроліт, а карбон(IV) оксид (вуглекислий газ) видаляється зі сфери реакції.<br> |
| | | | |
| - | [[Image:Chemistry_83_2.jpg]] | + | [[Image:Chemistry 83 2.jpg]] |
| | | | |
| | Очевидно, що утворення молекул води й вуглекислого газу є наслідком взаємодії між катіонами Гідрогену й карбонат-аніонами у розчині. Ця реакція необоротна (відбувається до кінця), оскільки вода - дуже слабкий електроліт, а вуглекислий газ видаляється зі сфери реакції.<br> | | Очевидно, що утворення молекул води й вуглекислого газу є наслідком взаємодії між катіонами Гідрогену й карбонат-аніонами у розчині. Ця реакція необоротна (відбувається до кінця), оскільки вода - дуже слабкий електроліт, а вуглекислий газ видаляється зі сфери реакції.<br> |
| Строка 105: |
Строка 105: |
| | ''Г. А. Лашевська, Геометрія, 9 клас<br>Вислано читачами з інтернет-сайтів '' | | ''Г. А. Лашевська, Геометрія, 9 клас<br>Вислано читачами з інтернет-сайтів '' |
| | | | |
| - | <br> <sub>Збірка конспектів уроків по всім класами, домашня робота, скачати реферати з хімії, книги та підручники згідно каленадарного плануванння з хімії для 9 класу</sub> | + | <br> <sub>Збірка конспектів уроків по всім класами, [[Гіпермаркет_Знань_-_перший_в_світі!|домашня робота]], скачати реферати [[Хімія|з хімії]], книги та підручники згідно каленадарного плануванння [[Хімія_9_клас|з хімії для 9 класу]]</sub> |
| | | | |
| | <br> | | <br> |
Версия 17:17, 30 марта 2010
Гіпермаркет Знань>>Хімія>>Хімія 9 клас>> Хімія: Реакції обміну між електролітами
РЕАКЦІЇ ОБМІНУ МІЖ ЕЛЕКТРОЛІТАМИ
Реакції обміну у розчинах електролітів, умови їх перебігу. Йонні рівняння
Після опрацювання § 12 ви зможете:
складати рівняння реакцій обміну у розчинах електролітів у повній і скороченій йонній формах.
На шляху до успіху пригадаємо з вивчених курсів хімії, фізики, математики:
що таке хімічне рівняння; як взаємодіють заряди; що таке подібні доданки та у який спосіб їх зводять; які реакції називають реакціями: а) обміну; б) нейтралізації; що таке ступінь окиснення; які оксиди та гідрати оксидів реагують із кислотами; за яких умов відбуваються до кінця реакції у розчинах між: а) кислотами та солями; б) двома солями; в) солями і лугами; як позначають у хімічних рівняннях утворення осаду й виділення газу.
• Реакції обміну між електролітами у розчинах відбуваються за участю йонів - частинок, які реально існують у розчинах солей, лугів і кислот. Такі реакції називають йонними, а рівняння цих реакцій - йонними рівняннями.
Уточнімо: йонними рівняннями можуть бути зображені будь-які реакції, що відбуваються за участю електролітів у розчинах. Якщо вони не супроводжуються зміною зарядів йонів (не змінюються ступені окиснення елементів), то їх називають реакціями йонного обміну.
Скласти йонне рівняння досить просто. Виконаймо дослід і розгляньмо послідовність складання йонного рівняння на прикладі реакції між калій йодидом і плюмбум(ІІ) нітратом у розчині. Про її перебіг свідчить утворення яскраво-жовтого осаду плюмбум(ІІ) йодиду (мал. 12.1).

Спочатку запишімо рівняння реакції без урахування дисоціації електролітів:
Pb(NO3)2 + 2KI = 2KNO3 + Pbl2 
Аби скласти рівняння цієї реакції у йонній формі, слід зважити на те, що електроліти у розчині дисоціюють на йони. За таблицею «Розчинність кислот, основ і солей у воді» (див. додаток) визначмо, які з-поміж реагентів є сильними електролітами. Обидві розчинні солі - плюмбум(ІІ) нітрат і калій йодид - у водному розчині практично повністю дисоціюють за йони. Тож запишімо їхні формули у йонному вигляді:
РЬ2+ + 2NO-3 + 2К+ + 2I-
Проаналізуймо, які з цих йонів взаємодіятимуть між собою з огляду знаки їхніх зарядів. Це потрібно, аби пересвідчитися, що ми правильно визначили продукти реакції. Електростатичні сили зумовлюватимуть притягування різнойменних і відштовхування однойменно заряджених йонів (мал. 12.2).
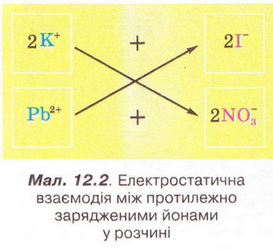
Отже, продукти реакції - калій нітрат і плюмбум(ІІ) йодид. Калій нітрат - сильний електроліт, повністю дисоціює, тому у правій частині рівняння записуємо катіони Калію та нітрат-аніони. Плюмбум(ІІ) йодид практично нерозчинний, тож його формулу залишаємо незмінною
РЬ2+ + 2NO-3 + 2К+ + 2I- = 2K++ 2N0-3 + Рbl2 
Зверніть увагу: у йонному рівнянні коефіцієнти перед формулами кожного з йонів записують з урахуванням індексів у формулах електролітів та коефіцієнтів перед ними. Приміром, унаслідок дисоціації однієї формульної одиниці плюмбум(ІІ) нітрату утворюється один катіон Плюмбуму(ІІ) і два нітрат-аніони. А під час дисоціації двох формульних одиниць калій йодиду утворюються два катіони Калію та два йодид-аніони.
Очевидно, що в лівій і правій частинах йонного рівняння є однакові йони (які саме?). Оскільки вони не беруть участі в реакції, їхні формули ножна скоротити:
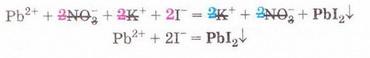
Вилучімо з лівої та правої частин рівняння формули катіонів Калію й - нітрат-аніонів, аби одержати скорочене йонне рівняння. У ньому записані тільки ті частинки, які реально взаємодіють у розчині з утворенням яскраво-жовтого осаду плюмбум(ІІ) йодиду. Тобто скорочене йонне рівняння відбиває суть реакції обміну між електролітами у розчині. Воно показує, які йони взаємодіють і яка речовина є продуктом реакції.
Виконаний дослід дає підстави стверджувати, що однією з умов необоротності реакції між електролітами у розчині є утворення осаду.
Завдання
Виберіть скорочене йонне рівняння, яке відповідає реакції між ферум(ІІІ) нітратом і калій гідроксидом у розчині:
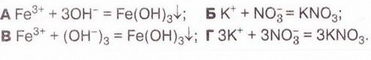
З'ясуймо, за яких ще умов, окрім утворення осаду, реакції обміну у розчинах електролітів будуть необоротними - тобто відбуватимуться до кінця. Дослідімо реакцію між натрій гідроксидом і нітратною кислотою у розчині. Наочно пересвідчитися у перебігу реакції нейтралізації допоможе застосування індикатора. До розчину натрій гідроксиду добавмо кілька крапель спиртового розчину фенолфталеїну - специфічного індикатора лужного середовища. Ви, звичайно, пам'ятаєте, що під дією гідроксид-аніонів фенолфталеїн набуває малинового забарвлення. Краплями, щоразу обережно струшуючи колбу, добавлятимемо розбавлену нітратну кислоту (мал. 12.3), аж поки малинове забарвлення фенолфталеїну не зникне. Знебарвлення розчину свідчить про нейтралізацію лугу кислотою:
NaOH + HNO3 = NaN03 + Н20

За допомогою таблиці розчинності (див. додаток) визначмо, що з чотирьох речовин - реагентів і продуктів реакції - до сильних електролітів належать три. Це натрій гідроксид (луг), нітратна кислота і натрій нітрат розчинна сіль. Вода - дуже слабкий електроліт, тож практично не дисоціює. З огляду на це, запишімо повне йонне рівняння реакції між натрій гідроксидом і нітратною кислотою у розчині:
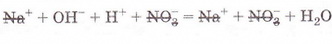
Очевидно, що молекули води утворюються внаслідок взаємодії у розчині катіонів Гідрогену й гідроксид-аніонів.
Отже, реакція обміну між електролітами у розчині практично необоротна, якщо один з продуктів - дуже слабкий електроліт, наприклад вода, або інша малодисоційована речовина.
Завдання
Виберіть ті пари електролітів, реакції між якими у розчині відбуваються практично до кінця (необоротно):
А Н2S04 і КОН; Б К2SiO3 і НN03; В НСІ і КN03; Г КN03 і NaОН.
Розгляньмо ще один випадок перебігу до кінця реакції між електролітами у розчині. Змішаймо розчин натрій карбонату з розбавленою сульфатною кислотою.
Завдання
За малюнком 12.4 опишіть на макрорівні хімічну реакцію між натрій карбонатом і сульфатною кислотою у розчині. Поясніть, чому не можна для проведення досліду брати розчини соди та кислоти у більших (мал. 12.4, 1), ніж вказано в інструкції (мал. 12.4, 2), кількостях.

Скориставшись таблицею розчинності і див. додаток), запишімо рівняння реакції (пам'ятаймо, карбонатна кислота нестійка, існує у розчині як гідрат):
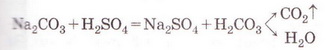
З-поміж п'яти речовин - реагентів і продуктів реакції - до сильних електролітів належать три. Це натрій карбонат, сульфатна кислота і натрій сульфат. Вода - дуже слабкий електроліт, а карбон(IV) оксид (вуглекислий газ) видаляється зі сфери реакції.
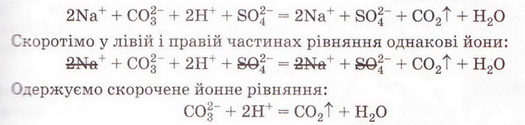
Очевидно, що утворення молекул води й вуглекислого газу є наслідком взаємодії між катіонами Гідрогену й карбонат-аніонами у розчині. Ця реакція необоротна (відбувається до кінця), оскільки вода - дуже слабкий електроліт, а вуглекислий газ видаляється зі сфери реакції.
Завдання
Виберіть ті пари електролітів, реакції між якими у розчині відбуваються практично до кінця (необоротно):
А Н2S04 і К2С03; Б Na2S і НСІ; В НNO3 і Na2S04; Г KNO3 і НСІ.
Виконані досліди доводять, що реакції обміну між електролітами у розчині необоротні, якщо поміж продуктів реакції є осад, газ, вода або інший слабкий електроліт.
Якщо виконується хоча б одна з цих умов, реакція відбувається до кінця. Якщо ж ні, то внаслідок змішування розчинів утворюється суміш йонів. Про це свідчить повне йонне рівняння реакції між натрій хлоридом і калій нітратом у розчині
Na+ + Сl- + К+ + N0-3 = Na+ + NO-з+ К+ + Сl-
Аби дістати більше експериментальних підтверджень правильності зроблених висновків, виконайте лабораторні досліди.
Г. А. Лашевська, Геометрія, 9 клас
Вислано читачами з інтернет-сайтів
Збірка конспектів уроків по всім класами, домашня робота, скачати реферати з хімії, книги та підручники згідно каленадарного плануванння з хімії для 9 класу
Зміст уроку
 конспект уроку і опорний каркас конспект уроку і опорний каркас
 презентація уроку презентація уроку
 акселеративні методи та інтерактивні технології акселеративні методи та інтерактивні технології
 закриті вправи (тільки для використання вчителями) закриті вправи (тільки для використання вчителями)
 оцінювання
Практика оцінювання
Практика
 задачі та вправи,самоперевірка задачі та вправи,самоперевірка
 практикуми, лабораторні, кейси практикуми, лабораторні, кейси
 рівень складності задач: звичайний, високий, олімпійський рівень складності задач: звичайний, високий, олімпійський
 домашнє завдання
Ілюстрації домашнє завдання
Ілюстрації
 ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа
 реферати реферати
 фішки для допитливих фішки для допитливих
 шпаргалки шпаргалки
 гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення
 зовнішнє незалежне тестування (ЗНТ) зовнішнє незалежне тестування (ЗНТ)
 підручники основні і допоміжні підручники основні і допоміжні
 тематичні свята, девізи тематичні свята, девізи
 статті статті
 національні особливості національні особливості
 словник термінів словник термінів
 інше
Тільки для вчителів інше
Тільки для вчителів
 ідеальні уроки ідеальні уроки
 календарний план на рік календарний план на рік
 методичні рекомендації методичні рекомендації
 програми програми
 обговорення обговорення
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|