|
|
|
| Строка 5: |
Строка 5: |
| | <metakeywords>Физика, 10 класс, Внутренняя энергия</metakeywords> | | <metakeywords>Физика, 10 класс, Внутренняя энергия</metakeywords> |
| | | | |
| - | Термодинамика была создана в середине XIX в. после открытия закона сохранения энергии. В ее основе лежит понятие ''внутренняя энергия''. С него мы и начнем. Предварительно остановимся на вопросе о том, какая связь существует между термодинамикой и молекулярно-[[Идеальный_газ_в_молекулярно-кинетической_теории|кинетической]] теорией.<br> '''Термодинамика и статистическая механика.''' Первой научной теорией тепловых процессов была не молекулярно-кинетическая теория, а термодинамика. Она возникла при изучении оптимальных условий использования теплоты для совершения работы. Это произошло в середине XIX в., задолго до того, как молекулярно-кинетическая теория получила всеобщее признание.<br> Сейчас в науке и [[Давление_в_природе_и_технике|технике]] при изучении тепловых явлений используются как термодинамика, так и молекулярно-кинетическая теория. В теоретической физике молекулярно-кинетическую теорию называют ''статистической механикой''. Термодинамика и статистическая механика изучают различными методами одни и те же явления и взаимно дополняют друг друга.<br> ''Главное содержание термодинамики состоит в двух основных ее законах, касающихся поведения энергии.'' Эти законы установлены опытным путем. Они справедливы для всех веществ независимо от их внутреннего строения.<br> Статистическая механика более глубокая и точная наука, чем термодинамика, но и более сложная. К ней прибегают в тех случаях, когда простые соотношения термодинамики оказываются недостаточными для объяснения наблюдаемых явлений.<br> '''Внутренняя энергия в молекулярно-кинетической теории.''' В середине XIX в. было доказано, что наряду с механической энергией макроскопические тела обладают еще и энергией, заключенной внутри самих тел. Эта ''внутренняя энергия'' входит в баланс энергетических превращений в природе. После открытия внутренней энергии был сформулирован ''закон сохранения и превращения энергии''.<br> Что такое внутренняя [[Кинетическая_энергия_и_ее_изменение|энергия]]?<br> Когда скользящая по льду шайба останавливается под действием силы трения, то ее механическая (кинетическая) энергия не просто исчезает, а передается беспорядочно движущимся молекулам льда и шайбы. Неровности поверхностей трущихся тел деформируются при движении, и интенсивность беспорядочного движения молекул возрастает. Оба тела нагреваются, что и означает увеличение их внутренней энергии.<br> Нетрудно наблюдать и обратный переход внутренней энергии в механическую. Если нагревать воду в пробирке, закрытой пробкой, то внутренняя энергия воды и внутренняя энергия пара начнут возрастать. Давление пара увеличится настолько, что пробка будет выбита. Кинетическая энергия пробки увеличится за счет внутренней энергии пара. Расширяясь, водяной пар совершает работу и охлаждается. Его внутренняя энергия при этом уменьшается.<br> С точки зрения молекулярно-кинетической теории '''внутренняя энергия макроскопического тела равна сумме кинетических энергий беспорядочного движения всех молекул (или атомов) тела и потенциальных энергий взаимодействия всех молекул друг с другом (но не с молекулами других тел).'''<br> Вычислить внутреннюю энергию тела (или ее изменение), учитывая [[Броуновское_движение|движение]] отдельных молекул и их положения относительно друг друга, практически невозможно из-за огромного числа молекул в макроскопических телах. Поэтому необходимо уметь определять значение внутренней энергии (или ее изменение) в зависимости от макроскопических параметров, которые можно непосредственно измерить.<br> '''Внутренняя энергия идеального одноатомного газа.''' Наиболее прост по своим свойствам одноатомный газ, состоящий из отдельных атомов, а не молекул. Одноатомными являются инертные газы - гелий, неон, аргон и др. Вычислим внутреннюю энергию идеального одноатомного газа.<br> Так как молекулы идеального газа не взаимодействуют друг с другом, то их потенциальная энергия равна нулю. Вся внутренняя энергия идеального газа определяется кинетической энергией беспорядочного движения его молекул.<br> Для вычисления внутренней энергии идеального одноатомного газа массой ''m'' нужно умножить среднюю кинетическую энергию одного атома на число атомов . Учитывая, что ''kN<sub>A</sub>=R'', получим формулу для внутренней энергии идеального газа:<br>[[Image:A75-1.jpg|center|215x48px|Внутренняя энергия]] '''Внутренняя энергия идеального одноатомного газа прямо пропорциональна его абсолютной [[Определение_температуры|температуре]].'''<br> Она не зависит от объема и других макроскопических параметров системы.<br> Изменение внутренней энергии идеального газа равно [[Image:A75-2.jpg|170x30px|Внутренняя энергия]], т.е. определяется температурами начального и конечного состояний газа и не зависит от процесса.<br> Если идеальный газ состоит из более сложных молекул, чем одноатомный, то его внутренняя энергия также пропорциональна абсолютной температуре, но коэффициент пропорциональности между ''U'' и ''T'' другой. Объясняется это тем, что сложные молекулы не только ''движутся поступательно, но и вращаются''. Внутренняя энергия таких газов равна сумме энергий поступательного и вращательного движений молекул.<br> '''Зависимость внутренней энергии от макроскопических параметров.''' Мы установили, что внутренняя энергия идеального газа зависит от одного параметра - температуры. От объема внутренняя энергия идеального газа не зависит потому, что потенциальная энергия взаимодействия его молекул равна нулю.<br> У реальных газов, жидкостей и твердых тел средняя потенциальная энергия взаимодействия молекул ''не равна нулю''. Правда, для газов она много меньше средней кинетической энергии молекул, но для твердых и жидких тел сравнима с ней.<br> Средняя потенциальная энергия взаимодействия молекул газа зависит от объема вещества, так как при изменении объема меняется среднее расстояние между [[Определение_температуры|молекулами]]. Следовательно, ''внутренняя энергия реального газа в термодинамике в общем случае зависит, наряду с температурой T, и от объема V.''<br> Значения макроскопических параметров (температуры ''T'', объема ''V'' и др.) однозначно определяют состояние тел. Поэтому они определяют и внутреннюю энергию макроскопических тел.<br> Внутренняя энергия ''U'' макроскопических тел однозначно определяется параметрами, характеризующими состояние этих тел: температурой и объемом.<br> В основе термодинамики лежит понятие внутренней энергии. Эта энергия зависит от макроскопических параметров: температуры и объема.<br> Внутренняя энергия идеального газа прямо пропорциональна его абсолютной температуре.<br><br><br> ???<br> 1. Приведите примеры превращения [[Уменьшение_механической_энергии_системы_под_действием_сил_трения|механической]] энергии во внутреннюю и обратно в технике и быту.<br> 2. От каких физических величин зависит внутренняя энергия тела?<br> 3. Чему равна внутренняя энергия идеального одноатомного газа?<br>
| + | <h2>Вступление</h2> |
| | | | |
| - | <br> ''Г.Я.Мякишев, Б.Б.Буховцев, Н.Н.Сотский, Физика 10 класс''
| + | Термодинамика была создана в середине XIX в. после открытия закона сохранения энергии. В ее основе лежит понятие ''внутренняя энергия''. С него мы и начнем. Предварительно остановимся на вопросе о том, какая связь существует между термодинамикой и молекулярно-[[Идеальный_газ_в_молекулярно-кинетической_теории|кинетической]] теорией. |
| | | | |
| - | <br> <sub>Материалы [[Физика и астрономия|по физике]], задание и ответы по классам, планы конспектов уроков [[Физика 10 класс|по физике для 10 класса]]</sub> | + | <h2>Термодинамика и статистическая механика</h2> |
| | | | |
| - | '''<u>Содержание урока</u>'''
| + | Первой научной теорией тепловых процессов была не молекулярно-кинетическая теория, а термодинамика. Она возникла при изучении оптимальных условий использования теплоты для совершения работы. Это произошло в середине XIX в., задолго до того, как молекулярно-кинетическая теория получила всеобщее признание. |
| - | '''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] конспект урока '''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] опорный каркас
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] презентация урока
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] акселеративные методы
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] интерактивные технологии
| + | |
| - |
| + | |
| - | '''<u>Практика</u>'''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] задачи и упражнения
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] самопроверка
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] практикумы, тренинги, кейсы, квесты
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] домашние задания
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] дискуссионные вопросы
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] риторические вопросы от учеников
| + | |
| - |
| + | |
| - | '''<u>Иллюстрации</u>'''
| + | |
| - | '''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] аудио-, видеоклипы и мультимедиа '''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фотографии, картинки
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] графики, таблицы, схемы
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] юмор, анекдоты, приколы, комиксы
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] притчи, поговорки, кроссворды, цитаты
| + | |
| - |
| + | |
| - | '''<u>Дополнения</u>'''
| + | |
| - | '''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] рефераты'''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] статьи
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фишки для любознательных
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] шпаргалки
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] учебники основные и дополнительные
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] словарь терминов
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] прочие
| + | |
| - |
| + | |
| - | <u>Совершенствование учебников и уроков
| + | |
| - | </u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] исправление ошибок в учебнике'''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обновление фрагмента в учебнике
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] элементы новаторства на уроке
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] замена устаревших знаний новыми
| + | |
| - |
| + | |
| - | '''<u>Только для учителей</u>'''
| + | |
| - | '''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] идеальные уроки '''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] календарный план на год
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] методические рекомендации
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] программы
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обсуждения
| + | |
| - |
| + | |
| - |
| + | |
| - | '''<u>Интегрированные уроки</u>'''
| + | |
| - |
| + | |
| | | | |
| - | Если у вас есть исправления или предложения к данному уроку, [http://xvatit.com/index.php?do=feedback напишите нам].
| + | Сейчас в науке и [[Давление_в_природе_и_технике|технике]] при изучении тепловых явлений используются как термодинамика, так и молекулярно-кинетическая теория. В теоретической физике молекулярно-кинетическую теорию называют ''статистической механикой''. Термодинамика и статистическая механика изучают различными методами одни и те же явления и взаимно дополняют друг друга. |
| | | | |
| - | Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - [http://xvatit.com/forum/ Образовательный форум]. | + | Главное содержание термодинамики состоит в двух основных ее законах, касающихся поведения энергии. Эти законы установлены опытным путем. Они справедливы для всех веществ независимо от их внутреннего строения. |
| | + | |
| | + | Статистическая механика более глубокая и точная наука, чем термодинамика, но и более сложная. К ней прибегают в тех случаях, когда простые соотношения термодинамики оказываются недостаточными для объяснения наблюдаемых явлений. |
| | + | |
| | + | <h2>Внутренняя энергия в молекулярно-кинетической теории</h2> |
| | + | |
| | + | В середине XIX в. было доказано, что наряду с механической энергией макроскопические тела обладают еще и энергией, заключенной внутри самих тел. Эта ''внутренняя энергия'' входит в баланс энергетических превращений в природе. После открытия внутренней энергии был сформулирован ''закон сохранения и превращения энергии''. |
| | + | |
| | + | '''Что такое внутренняя [[Кинетическая_энергия_и_ее_изменение|энергия]]?''' |
| | + | |
| | + | Когда скользящая по льду шайба останавливается под действием силы трения, то ее механическая (кинетическая) энергия не просто исчезает, а передается беспорядочно движущимся молекулам льда и шайбы. Неровности поверхностей трущихся тел деформируются при движении, и интенсивность беспорядочного движения молекул возрастает. Оба тела нагреваются, что и означает увеличение их внутренней энергии. |
| | + | |
| | + | Нетрудно наблюдать и обратный переход внутренней энергии в механическую. Если нагревать воду в пробирке, закрытой пробкой, то внутренняя энергия воды и внутренняя энергия пара начнут возрастать. Давление пара увеличится настолько, что пробка будет выбита. Кинетическая энергия пробки увеличится за счет внутренней энергии пара. Расширяясь, водяной пар совершает работу и охлаждается. Его внутренняя энергия при этом уменьшается. |
| | + | |
| | + | С точки зрения молекулярно-кинетической теории внутренняя энергия макроскопического тела равна сумме кинетических энергий беспорядочного движения всех молекул (или атомов) тела и потенциальных энергий взаимодействия всех молекул друг с другом (но не с молекулами других тел). |
| | + | |
| | + | Вычислить внутреннюю энергию тела (или ее изменение), учитывая [[Броуновское_движение|движение]] отдельных молекул и их положения относительно друг друга, практически невозможно из-за огромного числа молекул в макроскопических телах. Поэтому необходимо уметь определять значение внутренней энергии (или ее изменение) в зависимости от макроскопических параметров, которые можно непосредственно измерить. |
| | + | |
| | + | <h2>Внутренняя энергия идеального одноатомного газа</h2> |
| | + | |
| | + | Наиболее прост по своим свойствам одноатомный газ, состоящий из отдельных атомов, а не молекул. Одноатомными являются инертные газы - гелий, неон, аргон и др. Вычислим внутреннюю энергию идеального одноатомного газа. |
| | + | |
| | + | Так как молекулы идеального газа не взаимодействуют друг с другом, то их потенциальная энергия равна нулю. Вся внутренняя энергия идеального газа определяется кинетической энергией беспорядочного движения его молекул. |
| | + | |
| | + | Для вычисления внутренней энергии идеального одноатомного газа массой ''m'' нужно умножить среднюю кинетическую энергию одного атома на число атомов . Учитывая, что ''kN<sub>A</sub>=R'', получим формулу для внутренней энергии идеального газа: |
| | + | |
| | + | <br>[[Image:A75-1.jpg|center|215x48px|Внутренняя энергия]]<br> |
| | + | |
| | + | '''Внутренняя энергия идеального одноатомного газа прямо пропорциональна его абсолютной [[Определение_температуры|температуре]].''' |
| | + | |
| | + | Она не зависит от объема и других макроскопических параметров системы. |
| | + | |
| | + | Изменение внутренней энергии идеального газа равно <br>[[Image:A75-2.jpg|170x30px|Внутренняя энергия]]<br>, т.е. определяется температурами начального и конечного состояний газа и не зависит от процесса. |
| | + | |
| | + | Если идеальный газ состоит из более сложных молекул, чем одноатомный, то его внутренняя энергия также пропорциональна абсолютной температуре, но коэффициент пропорциональности между ''U'' и ''T'' другой. Объясняется это тем, что сложные молекулы не только ''движутся поступательно, но и вращаются''. Внутренняя энергия таких газов равна сумме энергий поступательного и вращательного движений молекул. |
| | + | |
| | + | <h2>Зависимость внутренней энергии от макроскопических параметров</h2> |
| | + | |
| | + | Мы установили, что внутренняя энергия идеального газа зависит от одного параметра - температуры. От объема внутренняя энергия идеального газа не зависит потому, что потенциальная энергия взаимодействия его молекул равна нулю. |
| | + | |
| | + | У реальных газов, жидкостей и твердых тел средняя потенциальная энергия взаимодействия молекул ''не равна нулю''. Правда, для газов она много меньше средней кинетической энергии молекул, но для твердых и жидких тел сравнима с ней. |
| | + | |
| | + | Средняя потенциальная энергия взаимодействия молекул газа зависит от объема вещества, так как при изменении объема меняется среднее расстояние между [[Определение_температуры|молекулами]]. Следовательно, ''внутренняя энергия реального газа в термодинамике в общем случае зависит, наряду с температурой T, и от объема V.'' |
| | + | |
| | + | Значения макроскопических параметров (температуры ''T'', объема ''V'' и др.) однозначно определяют состояние тел. Поэтому они определяют и внутреннюю энергию макроскопических тел. |
| | + | |
| | + | Внутренняя энергия ''U'' макроскопических тел однозначно определяется параметрами, характеризующими состояние этих тел: температурой и объемом.<br> В основе термодинамики лежит понятие внутренней энергии. Эта энергия зависит от макроскопических параметров: температуры и объема. |
| | + | |
| | + | Внутренняя энергия идеального газа прямо пропорциональна его абсолютной температуре. |
| | + | |
| | + | <h2>Вопросы</h2> |
| | + | |
| | + | 1. Приведите примеры превращения [[Уменьшение_механической_энергии_системы_под_действием_сил_трения|механической]] энергии во внутреннюю и обратно в технике и быту.<br> |
| | + | 2. От каких физических величин зависит внутренняя энергия тела?<br> |
| | + | 3. Чему равна внутренняя энергия идеального одноатомного газа?<br> |
| | + | |
| | + | <br> ''Г.Я.Мякишев, Б.Б.Буховцев, Н.Н.Сотский, Физика 10 класс'' |
Версия 17:02, 30 июня 2015
Гипермаркет знаний>>Физика и астрономия>>Физика 10 класс>>Физика: Внутренняя энергия
Вступление
Термодинамика была создана в середине XIX в. после открытия закона сохранения энергии. В ее основе лежит понятие внутренняя энергия. С него мы и начнем. Предварительно остановимся на вопросе о том, какая связь существует между термодинамикой и молекулярно-кинетической теорией.
Термодинамика и статистическая механика
Первой научной теорией тепловых процессов была не молекулярно-кинетическая теория, а термодинамика. Она возникла при изучении оптимальных условий использования теплоты для совершения работы. Это произошло в середине XIX в., задолго до того, как молекулярно-кинетическая теория получила всеобщее признание.
Сейчас в науке и технике при изучении тепловых явлений используются как термодинамика, так и молекулярно-кинетическая теория. В теоретической физике молекулярно-кинетическую теорию называют статистической механикой. Термодинамика и статистическая механика изучают различными методами одни и те же явления и взаимно дополняют друг друга.
Главное содержание термодинамики состоит в двух основных ее законах, касающихся поведения энергии. Эти законы установлены опытным путем. Они справедливы для всех веществ независимо от их внутреннего строения.
Статистическая механика более глубокая и точная наука, чем термодинамика, но и более сложная. К ней прибегают в тех случаях, когда простые соотношения термодинамики оказываются недостаточными для объяснения наблюдаемых явлений.
Внутренняя энергия в молекулярно-кинетической теории
В середине XIX в. было доказано, что наряду с механической энергией макроскопические тела обладают еще и энергией, заключенной внутри самих тел. Эта внутренняя энергия входит в баланс энергетических превращений в природе. После открытия внутренней энергии был сформулирован закон сохранения и превращения энергии.
Что такое внутренняя энергия?
Когда скользящая по льду шайба останавливается под действием силы трения, то ее механическая (кинетическая) энергия не просто исчезает, а передается беспорядочно движущимся молекулам льда и шайбы. Неровности поверхностей трущихся тел деформируются при движении, и интенсивность беспорядочного движения молекул возрастает. Оба тела нагреваются, что и означает увеличение их внутренней энергии.
Нетрудно наблюдать и обратный переход внутренней энергии в механическую. Если нагревать воду в пробирке, закрытой пробкой, то внутренняя энергия воды и внутренняя энергия пара начнут возрастать. Давление пара увеличится настолько, что пробка будет выбита. Кинетическая энергия пробки увеличится за счет внутренней энергии пара. Расширяясь, водяной пар совершает работу и охлаждается. Его внутренняя энергия при этом уменьшается.
С точки зрения молекулярно-кинетической теории внутренняя энергия макроскопического тела равна сумме кинетических энергий беспорядочного движения всех молекул (или атомов) тела и потенциальных энергий взаимодействия всех молекул друг с другом (но не с молекулами других тел).
Вычислить внутреннюю энергию тела (или ее изменение), учитывая движение отдельных молекул и их положения относительно друг друга, практически невозможно из-за огромного числа молекул в макроскопических телах. Поэтому необходимо уметь определять значение внутренней энергии (или ее изменение) в зависимости от макроскопических параметров, которые можно непосредственно измерить.
Внутренняя энергия идеального одноатомного газа
Наиболее прост по своим свойствам одноатомный газ, состоящий из отдельных атомов, а не молекул. Одноатомными являются инертные газы - гелий, неон, аргон и др. Вычислим внутреннюю энергию идеального одноатомного газа.
Так как молекулы идеального газа не взаимодействуют друг с другом, то их потенциальная энергия равна нулю. Вся внутренняя энергия идеального газа определяется кинетической энергией беспорядочного движения его молекул.
Для вычисления внутренней энергии идеального одноатомного газа массой m нужно умножить среднюю кинетическую энергию одного атома на число атомов . Учитывая, что kNA=R, получим формулу для внутренней энергии идеального газа:
Внутренняя энергия идеального одноатомного газа прямо пропорциональна его абсолютной температуре.
Она не зависит от объема и других макроскопических параметров системы.
Изменение внутренней энергии идеального газа равно
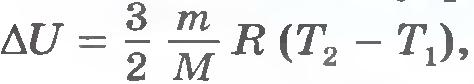
, т.е. определяется температурами начального и конечного состояний газа и не зависит от процесса.
Если идеальный газ состоит из более сложных молекул, чем одноатомный, то его внутренняя энергия также пропорциональна абсолютной температуре, но коэффициент пропорциональности между U и T другой. Объясняется это тем, что сложные молекулы не только движутся поступательно, но и вращаются. Внутренняя энергия таких газов равна сумме энергий поступательного и вращательного движений молекул.
Зависимость внутренней энергии от макроскопических параметров
Мы установили, что внутренняя энергия идеального газа зависит от одного параметра - температуры. От объема внутренняя энергия идеального газа не зависит потому, что потенциальная энергия взаимодействия его молекул равна нулю.
У реальных газов, жидкостей и твердых тел средняя потенциальная энергия взаимодействия молекул не равна нулю. Правда, для газов она много меньше средней кинетической энергии молекул, но для твердых и жидких тел сравнима с ней.
Средняя потенциальная энергия взаимодействия молекул газа зависит от объема вещества, так как при изменении объема меняется среднее расстояние между молекулами. Следовательно, внутренняя энергия реального газа в термодинамике в общем случае зависит, наряду с температурой T, и от объема V.
Значения макроскопических параметров (температуры T, объема V и др.) однозначно определяют состояние тел. Поэтому они определяют и внутреннюю энергию макроскопических тел.
Внутренняя энергия U макроскопических тел однозначно определяется параметрами, характеризующими состояние этих тел: температурой и объемом.
В основе термодинамики лежит понятие внутренней энергии. Эта энергия зависит от макроскопических параметров: температуры и объема.
Внутренняя энергия идеального газа прямо пропорциональна его абсолютной температуре.
Вопросы
1. Приведите примеры превращения механической энергии во внутреннюю и обратно в технике и быту.
2. От каких физических величин зависит внутренняя энергия тела?
3. Чему равна внутренняя энергия идеального одноатомного газа?
Г.Я.Мякишев, Б.Б.Буховцев, Н.Н.Сотский, Физика 10 класс
|










