|
|
|
| Строка 1: |
Строка 1: |
| - | '''[[Гіпермаркет Знань - перший в світі!|Гіпермаркет Знань]]>>[[Хімія|Хімія]]>>[[Хімія 8 клас|Хімія 8 клас]]>>Хімія: Кристалічні ґратки. Атомні, молекулярні та йонні кристали. Залежність фiзичних властивостей речовин від типів кристалічних ґраток''' <metakeywords>Хімія, клас, урок, на Тему, Кристалічні ґратки, Атомні кристали, молекулярні кристали, йонні кристали, Залежність фiзичних властивостей, речовин від типів, кристалічних ґраток</metakeywords> <br> | + | '''[[Гіпермаркет Знань - перший в світі!|Гіпермаркет Знань]]>>[[Хімія|Хімія]]>>[[Хімія 8 клас|Хімія 8 клас]]>>Кристалічні ґратки. Атомні, молекулярні та йонні кристали. Залежність фiзичних властивостей речовин від типів кристалічних ґраток''' <metakeywords>Хімія, клас, урок, на Тему, Кристалічні ґратки, Атомні кристали, молекулярні кристали, йонні кристали, Залежність фiзичних властивостей, речовин від типів, кристалічних ґраток</metakeywords> <br> |
| | | | |
| - | <br> | + | <br> |
| | | | |
| - | <br> | + | Тобі вже відомі такі частинки, як [[42._Будова_атома:_ядро_і_електронна_оболонка._Склад_атомних_ядер._Протонне_число._Нуклонне_число._Сучасне_формулювання_періодичного_закону|атоми]], [[Атоми,_молекули,_йони._Хімічні_елементи,_їхні_назви_і_символи|молекули]], [[Атоми,_молекули,_йони._Хімічні_елементи,_їхні_назви_і_симовли._Повні_уроки|йони]]. Це відносно проста форма організації речовини. У стандартних умовах ці частинки, як правило, індивідуально не існують. За допомогою різних типів хімічних зв'язків вони об'єднуються й утворюють вищу форму організації речовини — хімічні сполуки, що поділяються на прості і складні речовини, які існують у твердому, рідкому та газуватому стані. Якщо гази характеризуються повною невпорядкованістю розташування молекул одна відносно одної, то в рідинах деяка впорядкованість частинок спостерігається. Адже для рідин характерна наявність певного об'єму, хоча й відсутня певна форма. [[Лабораторна_робота_на_тему_«Визначення_густини_твердих_тіл_і_рідин»|Рідини]] займають проміжне місце між газами і твердими тілами, яким властивий суворий порядок розташування частинок, що утворюють речовину.<br> |
| | | | |
| - | <u>Тобі треба<br>розуміти:</u> залежність фізичних властивостей речовин від їх кристалічної будови;<br><u>знати типи кристалічних ґраток:</u> йонні; атомні; молекулярні;<br><u>уміти:</u> прогнозувати властивості речовин залежно від виду хімічного зв'язку і типу кристалічних ґраток.<br><br><br>Тобі вже відомі такі частинки, як атоми, молекули, йони. Це відносно проста форма організації речовини. У стандартних умовах ці частинки, як правило, індивідуально не існують. За допомогою різних типів хімічних зв'язків вони об'єднуються й утворюють вищу форму організації речовини — хімічні сполуки, що поділяються на прості і складні речовини, які існують у твердому, рідкому та газуватому стані. Якщо гази характеризуються повною невпорядкованістю розташування молекул одна відносно одної, то в рідинах деяка впорядкованість частинок спостерігається. Адже для рідин характерна наявність певного об'єму, хоча й відсутня певна форма. Рідини займають проміжне місце між газами і твердими тілами, яким властивий суворий порядок розташування частинок, що утворюють речовину.<br>
| + | У [[Лабораторна_робота_на_тему_«Вимірювання_об’єму_твердих_тіл,_рідин_і_газів»|твердих речовинах]] частинки розташовані у просторі суворо закономірно для кожної речовини. Щоб якось уявити цю закономірність, у тривимірному просторі подумки об'єднай центри молекул прямими лініями, які перетинаються. При цьому утвориться просторовий каркас, який називають кристалічними ґратками. Місця, в яких лінії перетинаються, називають вузлами кристалічних ґраток. Залежно від природи частинок, що містяться у вузлах кристалічних ґраток, розрізняють йонні, атомні, молекулярні кристалічні ґратки. Відомі ще й. металічні кристалічні ґратки, їх вивчатимеш пізніше (мал. 16).<br> |
| | | | |
| - | У твердих речовинах частинки розташовані у просторі суворо закономірно для кожної речовини. Щоб якось уявити цю закономірність, у тривимірному просторі подумки об'єднай центри молекул прямими лініями, які перетинаються. При цьому утвориться просторовий каркас, який називають кристалічними ґратками. Місця, в яких лінії перетинаються, називають вузлами кристалічних ґраток. Залежно від природи частинок, що містяться у вузлах кристалічних ґраток, розрізняють йонні, атомні, молекулярні кристалічні ґратки. Відомі ще й. металічні кристалічні ґратки, їх вивчатимеш пізніше (мал. 16).<br>
| + | '''Йонні кристалічні ґратки.''' Типовим представником сполук з йонним типом кристалічних ґраток є натрій хлорид NaCl. Його кристалічні ґратки утворені йонами Натрію Na<sup>+</sup> та йонами Хлору Сl<sup>-</sup>, які почергово розміщуються у вузлах ґраток (мал. 17). Иони утримуються один з одним силами притягання, і кристал солі є ніби єдиним цілим.<br><br>[[Image:Мал. 16. Типи кристалічних ґраток.jpg|Типи кристалічних ґраток: а — атомні; б — йонні; в — металічні; г — молекулярні. фото]]<br>''Мал. 16. Типи кристалічних ґраток: а — атомні; б — йонні; в — металічні; г — молекулярні''<br><br><br><br>[[Image:Мал. 17. Схема зображення йонних кристалічних ґраток натрій хлориду.jpg|Схема зображення йонних кристалічних ґраток натрій хлориду. фото]]<br>''Мал. 17. Схема зображення йонних кристалічних ґраток натрій хлориду''<br><br>Оскільки в кристалі сили притягання поширюються однаково в усіх напрямках, йони Натрію і Хлору сполучаються дуже міцно, хоча кожний із них не зафіксований нерухомо. Иони безперервно здійснюють теплові коливання навколо свого положення в ґратках. Міцність йонних кристалів залежить також і від заряду та радіуса йонів. Однак їх поступальний рух уздовж ґраток не відбувається, тому всі речовини з йонним зв'язком за стандартної температури — тверді (кристалічні), з досить високою температурою плавлення і ще вищою — кипіння.<br> |
| - | | + | |
| - | '''Йонні кристалічні ґратки.''' Типовим представником сполук з йонним типом кристалічних ґраток є натрій хлорид NaCl. Його кристалічні ґратки утворені йонами Натрію Na<sup>+</sup> та йонами Хлору Сl<sup>-</sup>, які почергово розміщуються у вузлах ґраток (мал. 17). Иони утримуються один з одним силами притягання, і кристал солі є ніби єдиним цілим.<br><br>[[Image:Мал. 16. Типи кристалічних ґраток.jpg]]<br>Мал. 16. Типи кристалічних ґраток: а — атомні; б — йонні; в — металічні; г — молекулярні<br><br><br><br>[[Image:Мал. 17. Схема зображення йонних кристалічних ґраток натрій хлориду.jpg]]<br>Мал. 17. Схема зображення йонних кристалічних ґраток натрій хлориду<br><br>Оскільки в кристалі сили притягання поширюються однаково в усіх напрямках, йони Натрію і Хлору сполучаються дуже міцно, хоча кожний із них не зафіксований нерухомо. Иони безперервно здійснюють теплові коливання навколо свого положення в ґратках. Міцність йонних кристалів залежить також і від заряду та радіуса йонів. Однак їх поступальний рух уздовж ґраток не відбувається, тому всі речовини з йонним зв'язком за стандартної температури — тверді (кристалічні), з досить високою температурою плавлення і ще вищою — кипіння.<br> | + | |
| | | | |
| | Молекул у йонних кристалах немає, є тільки йони. Лише у газуватому стані (пара) натрій хлорид існує у вигляді молекул NaCl.<br>Подібно до натрій хлориду майже всі солі, основні оксиди, гідроксиди складаються не з молекул, а з йонів.<br>Зверни увагу, хімічні формули йонних сполук передають лише співвідношення позитивно і негативно заряджених йонів у кристалічних ґратках. Йонні сполуки в цілому електронейтральні. Наприклад, згідно з формулою йонного кристала CaF<sub>2</sub> співвідношення позитивно заряджених йонів Са<sup>2+</sup> і негативно заряджених йонів F<sup>-</sup> у ґратках дорівнює 1:2. Оскільки кожні два позитивні заряди Са<sup>2+</sup> нейтралізуються двома негативними зарядами 2F<sup>-</sup>, то речовина CaF<sub>2</sub> — електронейтральна.<br> | | Молекул у йонних кристалах немає, є тільки йони. Лише у газуватому стані (пара) натрій хлорид існує у вигляді молекул NaCl.<br>Подібно до натрій хлориду майже всі солі, основні оксиди, гідроксиди складаються не з молекул, а з йонів.<br>Зверни увагу, хімічні формули йонних сполук передають лише співвідношення позитивно і негативно заряджених йонів у кристалічних ґратках. Йонні сполуки в цілому електронейтральні. Наприклад, згідно з формулою йонного кристала CaF<sub>2</sub> співвідношення позитивно заряджених йонів Са<sup>2+</sup> і негативно заряджених йонів F<sup>-</sup> у ґратках дорівнює 1:2. Оскільки кожні два позитивні заряди Са<sup>2+</sup> нейтралізуються двома негативними зарядами 2F<sup>-</sup>, то речовина CaF<sub>2</sub> — електронейтральна.<br> |
| Строка 17: |
Строка 15: |
| | <br> | | <br> |
| | | | |
| - | '''Атомні кристалічні ґратки.''' У вузлах атомних кристалічних ґраток містяться окремі атоми, сполучені між собою ковалентними зв'язками. Такі кристалічні ґратки має алмаз (мал. 18). У його кристалі кожний атом Карбону сполучений ковалентними зв'язками з чотирма сусідніми атомами Карбону, тобто утворює чотири спільні електронні пари. Ось чому можна говорити, що Карбон — чотиривалентний елемент. | + | '''[[Практичне_завдання_до_теми_Кристалічні_ґратки._Атомні,_молекулярні_та_йонні_кристали.|Атомні кристалічні ґратки]].''' У вузлах атомних кристалічних ґраток містяться окремі атоми, сполучені між собою ковалентними зв'язками. Такі кристалічні ґратки має алмаз (мал. 18). У його кристалі кожний атом Карбону сполучений ковалентними зв'язками з чотирма сусідніми атомами Карбону, тобто утворює чотири спільні електронні пари. Ось чому можна говорити, що Карбон — чотиривалентний елемент. |
| | | | |
| - | <sub> -4 +1 +4 -2</sub><br>Ступінь окиснення Карбону також -4 або +4, залежно від того, з яким елементом він взаємодіє — СН<sub>4</sub>, СО<sub>2</sub>.<br><br><br>[[Image:Мал. 18. Схематичне зображення атомних кристалічних ґраток алмазу.jpg]]<br>Мал. 18. Схематичне зображення атомних кристалічних ґраток алмазу<br><br>Алмаз та інші речовини, які мають атомні кристалічні ґратки, характеризуються великою твердістю, дуже високими температурами плавлення і кипіння, вони практично не розчиняються в жодних розчинниках, не проводять електричний струм, оскільки вільних електронів немає, всі 4 валентні електрони беруть участь в утворенні ковалентних зв'язків. Атомні ґратки мають лише деякі речовини у твердому стані (силіцій Si, бор В, силіцій(IV) оксид SiO<sub>2</sub>, силіцій(ІV) карбід SiC та ін.). | + | <sub> -4 +1 +4 -2</sub><br>Ступінь окиснення Карбону також -4 або +4, залежно від того, з яким елементом він взаємодіє — СН<sub>4</sub>, СО<sub>2</sub>.<br><br><br>[[Image:Мал. 18. Схематичне зображення атомних кристалічних ґраток алмазу.jpg|Схематичне зображення атомних кристалічних ґраток алмазу. фото]]<br>''Мал. 18. Схематичне зображення атомних кристалічних ґраток алмазу<br>''<br>Алмаз та інші речовини, які мають атомні кристалічні ґратки, характеризуються великою твердістю, дуже високими температурами плавлення і кипіння, вони практично не розчиняються в жодних розчинниках, не проводять електричний струм, оскільки вільних електронів немає, всі 4 валентні електрони беруть участь в утворенні ковалентних зв'язків. Атомні ґратки мають лише деякі речовини у твердому стані (силіцій Si, бор В, силіцій(IV) оксид SiO<sub>2</sub>, силіцій(ІV) карбід SiC та ін.). |
| | | | |
| - | '''<br>Молекулярні кристалічні ґратки.''' У вузлах молекулярних кристалічних ґраток містяться молекули як неполярні, так і полярні. Наприклад, у вузлах кристалічних ґраток йоду містяться молекули йоду І<sub>2</sub> (мал. 19). Сили міжмолекулярної взаємодії, так звані сили Ван-дер-Ваальса, значно слабкіші за сили ковалентного зв'язку. Тому речовини з молекулярними ґратками мають невелику твердість, вони легкоплавкі і леткі. До таких речовин належать, наприклад, йод, нафтален, бром, вода, спирт, хлор, амоніак NH<sub>3</sub>, метан СН<sub>4</sub>.<br><br>[[Image:Мал. 19. Схематичне зображення молекулярних кристалічних ґраток йоду.jpg]]<br>Мал. 19. Схематичне зображення молекулярних кристалічних ґраток йоду<br><br>Отже, будова речовини та її властивості пов'язані. Тому якщо відома будова речовини, можна прогнозувати її властивості, і навпаки, якщо відомі властивості речовини, можна робити висновки про її будову.<br>Зв'язок будови і властивостей речовин показаний в узагальнюючій табл. 14.<br><br>Таблиця 14. Тип кристалічних ґраток і властивості речовин<br>[[Image:Таблиця 14. Тип кристалічних ґраток і властивості речовин.jpg]]<br><br><u>Bисновки</u><br>У кристалічних речовинах атоми, молекули, йони розміщуються в певному порядку, утворюючи кристалічні ґратки. Розрізняють атомні, молекулярні, йонні та металічні кристалічні ґратки.<br>Між будовою речовини, яка визначається типом хімічного зв'язку і типом кристалічних ґраток, та її властивостями існує певна залежність: чим міцніший хімічний зв'язок, що утримує частинки у вузлах кристалічних ґраток, тим міцніші кристали, тим твердіша речовина, тим вищі її температури плавлення і кипіння.<br><br><u>Завдання для самоконтролю</u><br>1. У чому полягає відмінність йонних, атомних і молекулярних кристалічних ґраток?<br>2. Як, знаючи фізичні властивості речовини, можна дійти висновку про тип її кристалічних ґраток? Покажи на прикладі.<br>3. Поясни причину відмінності температури плавлення речовин із різним типом кристалічних ґраток.<br>4. За якими ознаками можна віднести до речовин з молекулярними кристалічними ґратками: а) лід; б) нафтален?<br>5. Молекулярні кристалічні ґратки можуть мати речовини з хімічним зв'язком<br>(а) йонним; (в) ковалентним полярним;<br>(б) металічним; (г) ковалентним неполярним.<br>6. Речовини з молекулярними кристалічними ґратками<br>(а) легкоплавкі; (в) добре проводять електричний струм;<br>(б) леткі; (г) мають низьку теплопровідність.<br>7. Речовина, що має найвищу температуру плавлення, — це<br>(а) йод; (б) лід; (в) кальцій флуорид.<br><br><u>Додаткові завдання</u><br>8*. Яке передбачення про кристалічні ґратки речовини можна висловити, якщо відомо, що за стандартних умов вона перебуває у газуватому стані, а за температури - 40 °С ця речовина являє собою безбарвні кристали, які не проводять електричний струм?<br>9*. Речовина, хімічні зв'язки в якій сформовані між атомами елементів із зарядами ядер +1 і +16, у твердому стані має кристалічні ґратки<br>(а) йонні; (б) молекулярні; (в) атомні.<br>10*. Речовина, утворена елементами із скороченими електронними конфігураціями атомів ...3s<sup>1</sup>3p<sup>0</sup> і ...3s<sup>2</sup>3p<sup>5</sup>, має кристалічні ґратки <br>(а) атомні; (б) йонні; (в) молекулярні. | + | '''<br>[[Практичне_завдання_до_теми_Кристалічні_ґратки._Атомні,_молекулярні_та_йонні_кристали.|Молекулярні кристалічні ґратки]].''' У вузлах молекулярних кристалічних ґраток містяться молекули як неполярні, так і полярні. Наприклад, у вузлах кристалічних ґраток йоду містяться молекули йоду І<sub>2</sub> (мал. 19). Сили міжмолекулярної взаємодії, так звані сили Ван-дер-Ваальса, значно слабкіші за сили ковалентного зв'язку. Тому речовини з молекулярними ґратками мають невелику твердість, вони легкоплавкі і леткі. До таких речовин належать, наприклад, йод, нафтален, бром, вода, спирт, хлор, амоніак NH<sub>3</sub>, метан СН<sub>4</sub>.<br><br>[[Image:Мал. 19. Схематичне зображення молекулярних кристалічних ґраток йоду.jpg|Схематичне зображення молекулярних кристалічних ґраток йоду. фото]]<br>''Мал. 19. Схематичне зображення молекулярних кристалічних ґраток йоду''<br><br>Отже, будова речовини та її властивості пов'язані. Тому якщо відома будова речовини, можна прогнозувати її властивості, і навпаки, якщо відомі властивості речовини, можна робити висновки про її будову.<br>Зв'язок будови і властивостей речовин показаний в узагальнюючій табл. 14.<br><br>''Таблиця 14. Тип кристалічних ґраток і властивості речовин''<br>[[Image:Таблиця 14. Тип кристалічних ґраток і властивості речовин.jpg|Тип кристалічних ґраток і властивості речовин. фото]]<br><br>'''Bисновки'''<br>У кристалічних речовинах атоми, молекули, йони розміщуються в певному порядку, утворюючи кристалічні ґратки. Розрізняють атомні, молекулярні, йонні та металічні кристалічні ґратки.<br>Між будовою речовини, яка визначається типом хімічного зв'язку і типом кристалічних ґраток, та її властивостями існує певна залежність: чим міцніший хімічний зв'язок, що утримує частинки у вузлах кристалічних ґраток, тим міцніші кристали, тим твердіша речовина, тим вищі її температури плавлення і кипіння.<br><br>'''Завдання для самоконтролю'''<br>''1. У чому полягає відмінність йонних, атомних і молекулярних кристалічних ґраток?<br>2. Як, знаючи фізичні властивості речовини, можна дійти висновку про тип її кристалічних ґраток? Покажи на прикладі.<br>3. Поясни причину відмінності температури плавлення речовин із різним типом кристалічних ґраток.<br>4. За якими ознаками можна віднести до речовин з молекулярними кристалічними ґратками: а) лід; б) нафтален?<br>5. Молекулярні кристалічні ґратки можуть мати речовини з хімічним зв'язком<br>(а) йонним; (в) ковалентним полярним;<br>(б) металічним; (г) ковалентним неполярним.<br>6. Речовини з молекулярними кристалічними ґратками<br>(а) легкоплавкі; (в) добре проводять електричний струм;<br>(б) леткі; (г) мають низьку теплопровідність.<br>7. Речовина, що має найвищу температуру плавлення, — це<br>(а) йод; (б) лід; (в) кальцій флуорид.''<br><br>'''Додаткові завдання'''<br>''8*. Яке передбачення про кристалічні ґратки речовини можна висловити, якщо відомо, що за стандартних умов вона перебуває у газуватому стані, а за температури - 40 °С ця речовина являє собою безбарвні кристали, які не проводять електричний струм?<br>9*. Речовина, хімічні зв'язки в якій сформовані між атомами елементів із зарядами ядер +1 і +16, у твердому стані має кристалічні ґратки<br>(а) йонні; (б) молекулярні; (в) атомні.<br>10*. Речовина, утворена елементами із скороченими електронними конфігураціями атомів ...3s<sup>1</sup>3p<sup>0</sup> і ...3s<sup>2</sup>3p<sup>5</sup>, має кристалічні ґратки <br>(а) атомні; (б) йонні; (в) молекулярні.'' |
| | | | |
| | <br> | | <br> |
| | | | |
| - | ----
| + | ''Н.М. Буринська, [[Хімія_8_клас|Хімія, 8 клас]]<br>Вислано читачами інтернет-сайту'' |
| - | | + | |
| - | Н.М. Буринська, Хімія, 8 клас<br>Вислано читачами інтернет-сайту | + | |
| | | | |
| | <br> <sub>[[Гіпермаркет Знань - перший в світі!|Онлайн]] бібліотека з підручниками і книгами, плани-конспекти уроків з [[Хімія 8 клас|хімії]] для 8 класу, книги та підручники згідно каленадарного плануванння з хімії</sub> <br> | | <br> <sub>[[Гіпермаркет Знань - перший в світі!|Онлайн]] бібліотека з підручниками і книгами, плани-конспекти уроків з [[Хімія 8 клас|хімії]] для 8 класу, книги та підручники згідно каленадарного плануванння з хімії</sub> <br> |
| | | | |
| | '''<u>Зміст уроку</u>''' | | '''<u>Зміст уроку</u>''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] конспект уроку і опорний каркас | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] конспект уроку і опорний каркас |
| - | [[Image:1236084776 kr.jpg|10x10px]] презентація уроку | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] презентація уроку |
| - | [[Image:1236084776 kr.jpg|10x10px]] акселеративні методи та інтерактивні технології | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] акселеративні методи та інтерактивні технології |
| - | [[Image:1236084776 kr.jpg|10x10px]] закриті вправи (тільки для використання вчителями) | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] закриті вправи (тільки для використання вчителями) |
| - | [[Image:1236084776 kr.jpg|10x10px]] оцінювання | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] оцінювання |
| | | | |
| | '''<u>Практика</u>''' | | '''<u>Практика</u>''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] задачі та вправи,самоперевірка | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] задачі та вправи,самоперевірка |
| - | [[Image:1236084776 kr.jpg|10x10px]] практикуми, лабораторні, кейси | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] практикуми, лабораторні, кейси |
| - | [[Image:1236084776 kr.jpg|10x10px]] рівень складності задач: звичайний, високий, олімпійський | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] рівень складності задач: звичайний, високий, олімпійський |
| - | [[Image:1236084776 kr.jpg|10x10px]] домашнє завдання | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] домашнє завдання |
| | | | |
| | '''<u>Ілюстрації</u>''' | | '''<u>Ілюстрації</u>''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа |
| - | [[Image:1236084776 kr.jpg|10x10px]] реферати | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] реферати |
| - | [[Image:1236084776 kr.jpg|10x10px]] фішки для допитливих | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фішки для допитливих |
| - | [[Image:1236084776 kr.jpg|10x10px]] шпаргалки | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] шпаргалки |
| - | [[Image:1236084776 kr.jpg|10x10px]] гумор, притчі, приколи, приказки, кросворди, цитати | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] гумор, притчі, приколи, приказки, кросворди, цитати |
| | | | |
| | '''<u>Доповнення</u>''' | | '''<u>Доповнення</u>''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] зовнішнє незалежне тестування (ЗНТ) | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] зовнішнє незалежне тестування (ЗНТ) |
| - | [[Image:1236084776 kr.jpg|10x10px]] підручники основні і допоміжні | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] підручники основні і допоміжні |
| - | [[Image:1236084776 kr.jpg|10x10px]] тематичні свята, девізи | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] тематичні свята, девізи |
| - | [[Image:1236084776 kr.jpg|10x10px]] статті | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] статті |
| - | [[Image:1236084776 kr.jpg|10x10px]] національні особливості | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] національні особливості |
| - | [[Image:1236084776 kr.jpg|10x10px]] словник термінів | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] словник термінів |
| - | [[Image:1236084776 kr.jpg|10x10px]] інше | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] інше |
| | | | |
| | '''<u>Тільки для вчителів</u>''' | | '''<u>Тільки для вчителів</u>''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] [http://xvatit.com/Idealny_urok.html ідеальні уроки] | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] [http://xvatit.com/Idealny_urok.html ідеальні уроки] |
| - | [[Image:1236084776 kr.jpg|10x10px]] календарний план на рік | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] календарний план на рік |
| - | [[Image:1236084776 kr.jpg|10x10px]] методичні рекомендації | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] методичні рекомендації |
| - | [[Image:1236084776 kr.jpg|10x10px]] програми | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] програми |
| - | [[Image:1236084776 kr.jpg|10x10px]] [http://xvatit.com/forum/ обговорення] | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] [http://xvatit.com/forum/ обговорення] |
| | | | |
| | <br> | | <br> |
Текущая версия на 08:39, 18 июля 2012
Гіпермаркет Знань>>Хімія>>Хімія 8 клас>>Кристалічні ґратки. Атомні, молекулярні та йонні кристали. Залежність фiзичних властивостей речовин від типів кристалічних ґраток
Тобі вже відомі такі частинки, як атоми, молекули, йони. Це відносно проста форма організації речовини. У стандартних умовах ці частинки, як правило, індивідуально не існують. За допомогою різних типів хімічних зв'язків вони об'єднуються й утворюють вищу форму організації речовини — хімічні сполуки, що поділяються на прості і складні речовини, які існують у твердому, рідкому та газуватому стані. Якщо гази характеризуються повною невпорядкованістю розташування молекул одна відносно одної, то в рідинах деяка впорядкованість частинок спостерігається. Адже для рідин характерна наявність певного об'єму, хоча й відсутня певна форма. Рідини займають проміжне місце між газами і твердими тілами, яким властивий суворий порядок розташування частинок, що утворюють речовину.
У твердих речовинах частинки розташовані у просторі суворо закономірно для кожної речовини. Щоб якось уявити цю закономірність, у тривимірному просторі подумки об'єднай центри молекул прямими лініями, які перетинаються. При цьому утвориться просторовий каркас, який називають кристалічними ґратками. Місця, в яких лінії перетинаються, називають вузлами кристалічних ґраток. Залежно від природи частинок, що містяться у вузлах кристалічних ґраток, розрізняють йонні, атомні, молекулярні кристалічні ґратки. Відомі ще й. металічні кристалічні ґратки, їх вивчатимеш пізніше (мал. 16).
Йонні кристалічні ґратки. Типовим представником сполук з йонним типом кристалічних ґраток є натрій хлорид NaCl. Його кристалічні ґратки утворені йонами Натрію Na+ та йонами Хлору Сl-, які почергово розміщуються у вузлах ґраток (мал. 17). Иони утримуються один з одним силами притягання, і кристал солі є ніби єдиним цілим.

Мал. 16. Типи кристалічних ґраток: а — атомні; б — йонні; в — металічні; г — молекулярні
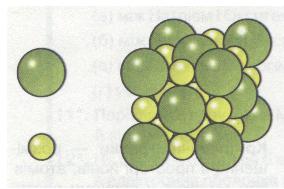
Мал. 17. Схема зображення йонних кристалічних ґраток натрій хлориду
Оскільки в кристалі сили притягання поширюються однаково в усіх напрямках, йони Натрію і Хлору сполучаються дуже міцно, хоча кожний із них не зафіксований нерухомо. Иони безперервно здійснюють теплові коливання навколо свого положення в ґратках. Міцність йонних кристалів залежить також і від заряду та радіуса йонів. Однак їх поступальний рух уздовж ґраток не відбувається, тому всі речовини з йонним зв'язком за стандартної температури — тверді (кристалічні), з досить високою температурою плавлення і ще вищою — кипіння.
Молекул у йонних кристалах немає, є тільки йони. Лише у газуватому стані (пара) натрій хлорид існує у вигляді молекул NaCl.
Подібно до натрій хлориду майже всі солі, основні оксиди, гідроксиди складаються не з молекул, а з йонів.
Зверни увагу, хімічні формули йонних сполук передають лише співвідношення позитивно і негативно заряджених йонів у кристалічних ґратках. Йонні сполуки в цілому електронейтральні. Наприклад, згідно з формулою йонного кристала CaF2 співвідношення позитивно заряджених йонів Са2+ і негативно заряджених йонів F- у ґратках дорівнює 1:2. Оскільки кожні два позитивні заряди Са2+ нейтралізуються двома негативними зарядами 2F-, то речовина CaF2 — електронейтральна.
Хоча реальних молекул у йонних кристалах не існує, для однаковості з ковалентними речовинами прийнято за допомогою формул NaCl, CaF2 тощо передавати найпростіший склад йонної речовини та характеризувати її також певним значенням відносної молекулярної (формульної) маси на підставі її формульного складу. А поняття про валентність як певне число ковалентних зв'язків до йонних сполук застосувати неможливо (тому й будемо говорити про ступінь окиснення елементів).
Атомні кристалічні ґратки. У вузлах атомних кристалічних ґраток містяться окремі атоми, сполучені між собою ковалентними зв'язками. Такі кристалічні ґратки має алмаз (мал. 18). У його кристалі кожний атом Карбону сполучений ковалентними зв'язками з чотирма сусідніми атомами Карбону, тобто утворює чотири спільні електронні пари. Ось чому можна говорити, що Карбон — чотиривалентний елемент.
-4 +1 +4 -2
Ступінь окиснення Карбону також -4 або +4, залежно від того, з яким елементом він взаємодіє — СН4, СО2.
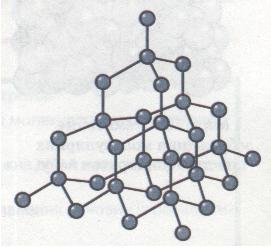
Мал. 18. Схематичне зображення атомних кристалічних ґраток алмазу
Алмаз та інші речовини, які мають атомні кристалічні ґратки, характеризуються великою твердістю, дуже високими температурами плавлення і кипіння, вони практично не розчиняються в жодних розчинниках, не проводять електричний струм, оскільки вільних електронів немає, всі 4 валентні електрони беруть участь в утворенні ковалентних зв'язків. Атомні ґратки мають лише деякі речовини у твердому стані (силіцій Si, бор В, силіцій(IV) оксид SiO2, силіцій(ІV) карбід SiC та ін.).
Молекулярні кристалічні ґратки. У вузлах молекулярних кристалічних ґраток містяться молекули як неполярні, так і полярні. Наприклад, у вузлах кристалічних ґраток йоду містяться молекули йоду І2 (мал. 19). Сили міжмолекулярної взаємодії, так звані сили Ван-дер-Ваальса, значно слабкіші за сили ковалентного зв'язку. Тому речовини з молекулярними ґратками мають невелику твердість, вони легкоплавкі і леткі. До таких речовин належать, наприклад, йод, нафтален, бром, вода, спирт, хлор, амоніак NH3, метан СН4.
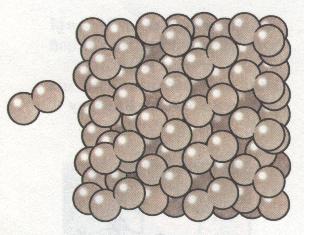
Мал. 19. Схематичне зображення молекулярних кристалічних ґраток йоду
Отже, будова речовини та її властивості пов'язані. Тому якщо відома будова речовини, можна прогнозувати її властивості, і навпаки, якщо відомі властивості речовини, можна робити висновки про її будову.
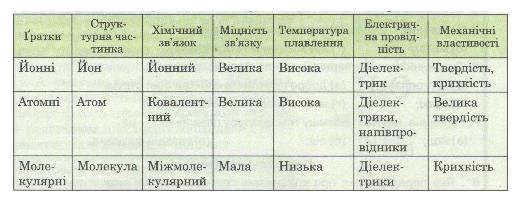
Зв'язок будови і властивостей речовин показаний в узагальнюючій табл. 14.
Таблиця 14. Тип кристалічних ґраток і властивості речовин
Bисновки
У кристалічних речовинах атоми, молекули, йони розміщуються в певному порядку, утворюючи кристалічні ґратки. Розрізняють атомні, молекулярні, йонні та металічні кристалічні ґратки.
Між будовою речовини, яка визначається типом хімічного зв'язку і типом кристалічних ґраток, та її властивостями існує певна залежність: чим міцніший хімічний зв'язок, що утримує частинки у вузлах кристалічних ґраток, тим міцніші кристали, тим твердіша речовина, тим вищі її температури плавлення і кипіння.
Завдання для самоконтролю
1. У чому полягає відмінність йонних, атомних і молекулярних кристалічних ґраток?
2. Як, знаючи фізичні властивості речовини, можна дійти висновку про тип її кристалічних ґраток? Покажи на прикладі.
3. Поясни причину відмінності температури плавлення речовин із різним типом кристалічних ґраток.
4. За якими ознаками можна віднести до речовин з молекулярними кристалічними ґратками: а) лід; б) нафтален?
5. Молекулярні кристалічні ґратки можуть мати речовини з хімічним зв'язком
(а) йонним; (в) ковалентним полярним;
(б) металічним; (г) ковалентним неполярним.
6. Речовини з молекулярними кристалічними ґратками
(а) легкоплавкі; (в) добре проводять електричний струм;
(б) леткі; (г) мають низьку теплопровідність.
7. Речовина, що має найвищу температуру плавлення, — це
(а) йод; (б) лід; (в) кальцій флуорид.
Додаткові завдання
8*. Яке передбачення про кристалічні ґратки речовини можна висловити, якщо відомо, що за стандартних умов вона перебуває у газуватому стані, а за температури - 40 °С ця речовина являє собою безбарвні кристали, які не проводять електричний струм?
9*. Речовина, хімічні зв'язки в якій сформовані між атомами елементів із зарядами ядер +1 і +16, у твердому стані має кристалічні ґратки
(а) йонні; (б) молекулярні; (в) атомні.
10*. Речовина, утворена елементами із скороченими електронними конфігураціями атомів ...3s13p0 і ...3s23p5, має кристалічні ґратки
(а) атомні; (б) йонні; (в) молекулярні.
Н.М. Буринська, Хімія, 8 клас
Вислано читачами інтернет-сайту
Онлайн бібліотека з підручниками і книгами, плани-конспекти уроків з хімії для 8 класу, книги та підручники згідно каленадарного плануванння з хімії
Зміст уроку
 конспект уроку і опорний каркас конспект уроку і опорний каркас
 презентація уроку презентація уроку
 акселеративні методи та інтерактивні технології акселеративні методи та інтерактивні технології
 закриті вправи (тільки для використання вчителями) закриті вправи (тільки для використання вчителями)
 оцінювання
Практика оцінювання
Практика
 задачі та вправи,самоперевірка задачі та вправи,самоперевірка
 практикуми, лабораторні, кейси практикуми, лабораторні, кейси
 рівень складності задач: звичайний, високий, олімпійський рівень складності задач: звичайний, високий, олімпійський
 домашнє завдання
Ілюстрації домашнє завдання
Ілюстрації
 ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа
 реферати реферати
 фішки для допитливих фішки для допитливих
 шпаргалки шпаргалки
 гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення
 зовнішнє незалежне тестування (ЗНТ) зовнішнє незалежне тестування (ЗНТ)
 підручники основні і допоміжні підручники основні і допоміжні
 тематичні свята, девізи тематичні свята, девізи
 статті статті
 національні особливості національні особливості
 словник термінів словник термінів
 інше
Тільки для вчителів інше
Тільки для вчителів
 ідеальні уроки ідеальні уроки
 календарний план на рік календарний план на рік
 методичні рекомендації методичні рекомендації
 програми програми
 обговорення обговорення
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|















