|
|
| Строка 1: |
Строка 1: |
| - | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 8 класс|Химия 8 класс]]>> Химия: Молярный объем газов'''<metakeywords>химия, 8 класс, класс, урок химии, на тему, урок на тему, урок для 8 класса, Молярный объем газов</metakeywords>''' | + | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 8 класс|Химия 8 класс]]>> Химия: Молярный объем газов'''<metakeywords>химия, 8 класс, класс, урок химии, на тему, урок на тему, урок для 8 класса, Молярный объем газов</metakeywords> |
| | | | |
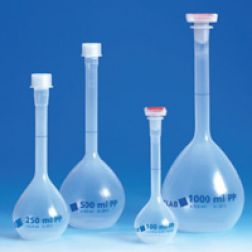
| - | Масса одного моля вещества называется молярной. А как будет называться объем одного моля вещества? Очевидно, что он также будет называться молярным. Чему равен молярный объем воды? Когда мы отмеривали 1 ноль воды, мы не взвешивали на весах 18 г воды — это очень неудобно. Мы пользовались мерной посудой: цилиндром, мензуркой или колбой, так как знали, что плотность воды (масса одной единицы объема) равна 1 г/мл. Поэтому полярный объем воды равен 18 мл. У жидкостей и твердых веществ он зависит от плотности веществ. | + | Масса одного моля вещества называется молярной. А как будет называться объем одного моля вещества? Очевидно, что он также будет называться молярным. Чему равен молярный объем воды? Когда мы отмеривали 1 ноль воды, мы не взвешивали на весах 18 г [[Тема_4._Неорганічні_сполуки:_вода_та_мінеральні_солі.|воды]] — это очень неудобно. Мы пользовались мерной посудой: цилиндром, мензуркой или колбой, так как знали, что плотность воды (масса одной единицы объема) равна 1 г/мл. Поэтому полярный объем воды равен 18 мл. У жидкостей и твердых веществ он зависит от плотности веществ. |
| | | | |
| - | [[Image:smlooo.jpg]] | + | [[Image:Smlooo.jpg|газы]] |
| | | | |
| - | <br>Другое дело у газов. | + | <br>Другое дело у газов. |
| | | | |
| - | <br>Если взять 1 моль водорода II (2 г). 1 моль кислорода О2 (32 г), 1 моль озона О3 (48 г), 1 моль углекислого газа С02 (44 г) а даже 1 моль водяных паров Н2О (18 г) при одинаковых условиях, например нормальных (в химии принято называть нор мольными условиями температуру 0º С и давление 760 мм рт. ст., или 101,3 кПа). то окажется, что один моль любого из газов займет один и тот же объем, равный 22.4 л. | + | <br>Если взять 1 моль водорода II (2 г). 1 моль [[Кислород|кислорода]] О2 (32 г), 1 моль озона О3 (48 г), 1 моль углекислого газа С02 (44 г) а даже 1 моль водяных паров Н2О (18 г) при одинаковых условиях, например нормальных (в химии принято называть нор мольными условиями [[Повітряна_оболонка_Землі._Температура_та_атмосферний_тиск.|температуру]] 0º С и [[Давление_и_сила_давления|давление]] 760 мм рт. ст., или 101,3 кПа). то окажется, что один моль любого из газов займет один и тот же объем, равный 22.4 л. |
| | | | |
| - | <br>Так как это объем газа количеством вещества 1 моль, то он называется молярным объемом и обозначается Vм. | + | <br>Так как это объем газа количеством вещества 1 моль, то он называется молярным объемом и обозначается Vм. |
| | | | |
| - | <br>А если взять 44.8 л газа, то какое количество вещества его будет взято? Конечно же 2 моль, так кик заданный объем вдвое больше молярного. | + | <br>А если взять 44.8 л газа, то какое количество вещества его будет взято? Конечно же 2 моль, так кик заданный объем вдвое больше молярного. |
| | | | |
| - | [[Image:him8-49.jpg]] | + | [[Image:Him8-49.jpg|химия]] |
| | | | |
| | + | <br> |
| | | | |
| | + | [[Image:Him8-50.jpg|химия]] |
| | | | |
| - | [[Image:him8-50.jpg]]
| + | <br>1. Молярный, милллмолярный и киломолярный объемы газов. 2. Нормальные условия. |
| | | | |
| - | <br>1. Молярный, милллмолярный и киломолярный объемы газов. 2. Нормальные условия. | + | <br>Найдите массу и число молекул при н. у. для: а) 11.2 л кислорода: б) 5,6 м3 азота; в) 22,4 мл хлора.<br>Найдите объем, который при н. у. займут: а) 3 г водорода: б) 96 кг озона; в) 12 * 10^20 молекул [[Азот_(Химия_9_класс)|азота]]. |
| | | | |
| - | <br>Найдите массу и число молекул при н. у. для: а) 11.2 л кислорода: б) 5,6 м3 азота; в) 22,4 мл хлора.<br>Найдите объем, который при н. у. займут: а) 3 г водорода: б) 96 кг озона; в) 12 * 10^20 молекул азота. | + | <br>Найдите плотности (массу 1 k) аргона, хлора, кислорода и озона при н. у. Сколько молекул каждого вещества будет содержаться в 1 л при тех же условиях?<br> |
| | | | |
| - | <br>Найдите плотности (массу 1 k) аргона, хлора, кислорода и озона при н. у. Сколько молекул каждого вещества будет содержаться в 1 л при тех же условиях?<br>
| + | <br> <sub>планирование [[Химия|химии]], книги [[Химия 8 класс|по химии 8 класса]], закрытые [[Гипермаркет знаний - первый в мире!|задания]] для использования учителями </sub> |
| - | | + | |
| - | <br> <sub>планирование [[Химия|химии]], книги [[Химия_8_класс|по химии 8 класса]], закрытые [[Гипермаркет_знаний_-_первый_в_мире!|задания]] для использования учителями </sub> | + | |
| | | | |
| | '''<u>Содержание урока</u>''' | | '''<u>Содержание урока</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] конспект урока ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] конспект урока ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] опорный каркас | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] опорный каркас |
| - | [[Image:1236084776 kr.jpg|10x10px]] презентация урока | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] презентация урока |
| - | [[Image:1236084776 kr.jpg|10x10px]] акселеративные методы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] акселеративные методы |
| - | [[Image:1236084776 kr.jpg|10x10px]] интерактивные технологии | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] интерактивные технологии |
| | | | |
| | '''<u>Практика</u>''' | | '''<u>Практика</u>''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] задачи и упражнения | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] задачи и упражнения |
| - | [[Image:1236084776 kr.jpg|10x10px]] самопроверка | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] самопроверка |
| - | [[Image:1236084776 kr.jpg|10x10px]] практикумы, тренинги, кейсы, квесты | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] практикумы, тренинги, кейсы, квесты |
| - | [[Image:1236084776 kr.jpg|10x10px]] домашние задания | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] домашние задания |
| - | [[Image:1236084776 kr.jpg|10x10px]] дискуссионные вопросы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] дискуссионные вопросы |
| - | [[Image:1236084776 kr.jpg|10x10px]] риторические вопросы от учеников | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] риторические вопросы от учеников |
| - |
| + | |
| | '''<u>Иллюстрации</u>''' | | '''<u>Иллюстрации</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] аудио-, видеоклипы и мультимедиа ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] аудио-, видеоклипы и мультимедиа ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] фотографии, картинки | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фотографии, картинки |
| - | [[Image:1236084776 kr.jpg|10x10px]] графики, таблицы, схемы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] графики, таблицы, схемы |
| - | [[Image:1236084776 kr.jpg|10x10px]] юмор, анекдоты, приколы, комиксы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] юмор, анекдоты, приколы, комиксы |
| - | [[Image:1236084776 kr.jpg|10x10px]] притчи, поговорки, кроссворды, цитаты | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] притчи, поговорки, кроссворды, цитаты |
| | | | |
| | '''<u>Дополнения</u>''' | | '''<u>Дополнения</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] рефераты''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] рефераты''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] статьи | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] статьи |
| - | [[Image:1236084776 kr.jpg|10x10px]] фишки для любознательных | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фишки для любознательных |
| - | [[Image:1236084776 kr.jpg|10x10px]] шпаргалки | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] шпаргалки |
| - | [[Image:1236084776 kr.jpg|10x10px]] учебники основные и дополнительные | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] учебники основные и дополнительные |
| - | [[Image:1236084776 kr.jpg|10x10px]] словарь терминов | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] словарь терминов |
| - | [[Image:1236084776 kr.jpg|10x10px]] прочие | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] прочие |
| | '''<u></u>''' | | '''<u></u>''' |
| | <u>Совершенствование учебников и уроков | | <u>Совершенствование учебников и уроков |
| - | </u>'''[[Image:1236084776 kr.jpg|10x10px]] исправление ошибок в учебнике''' | + | </u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] исправление ошибок в учебнике''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] обновление фрагмента в учебнике | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обновление фрагмента в учебнике |
| - | [[Image:1236084776 kr.jpg|10x10px]] элементы новаторства на уроке | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] элементы новаторства на уроке |
| - | [[Image:1236084776 kr.jpg|10x10px]] замена устаревших знаний новыми | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] замена устаревших знаний новыми |
| - |
| + | |
| | '''<u>Только для учителей</u>''' | | '''<u>Только для учителей</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] идеальные уроки ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] идеальные уроки ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] календарный план на год | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] календарный план на год |
| - | [[Image:1236084776 kr.jpg|10x10px]] методические рекомендации | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] методические рекомендации |
| - | [[Image:1236084776 kr.jpg|10x10px]] программы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] программы |
| - | [[Image:1236084776 kr.jpg|10x10px]] обсуждения | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обсуждения |
| | | | |
| | | | |
Масса одного моля вещества называется молярной. А как будет называться объем одного моля вещества? Очевидно, что он также будет называться молярным. Чему равен молярный объем воды? Когда мы отмеривали 1 ноль воды, мы не взвешивали на весах 18 г воды — это очень неудобно. Мы пользовались мерной посудой: цилиндром, мензуркой или колбой, так как знали, что плотность воды (масса одной единицы объема) равна 1 г/мл. Поэтому полярный объем воды равен 18 мл. У жидкостей и твердых веществ он зависит от плотности веществ.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.