|
|
|
| Строка 5: |
Строка 5: |
| | <metakeywords>Физика, 10 класс, Применение первого закона, термодинамики к различным, процессам</metakeywords> | | <metakeywords>Физика, 10 класс, Применение первого закона, термодинамики к различным, процессам</metakeywords> |
| | | | |
| - | 79.Применение первого закона термодинамики к различным процессам<br>С помощью первого закона термодинамики можно де¬лать важные заключения о характере протекающих про¬цессов. Рассмотрим различные процессы, при которых одна из физических величин остается неизменной (изопроцессы), например случай, когда система представляет со¬бой идеальный газ.<br>Изохорный процесс. При изохорном процессе объем газа не меняется, и поэтому работа газа равна нулю. Изме¬нение внутренней энергии газа согласно уравнению (13.11) равно количеству переданной ему теплоты:<br><br>Если газ нагревается, то *****и ******, его внутренняя энергия увеличивается. При охлаждении газа ***** и *****, изменение внутренней энергии отрица¬тельно и внутренняя энергия газа уменьшается.<br>Изотермический процесс. При изотермическом процес¬се (******) внутренняя энергия идеального газа (см. формулу (13.1)) не меняется. Согласно формуле (13.11) все переданное газу количество теплоты идет на совершение работы:<br><br>Если газ получает тепло (******), то он совершает поло¬жительную работу (*****). Если, напротив, газ отдает тепло окружающей среде (термостату), то **** и ****. Работа же внешних сил над газом в последнем случае по¬ложительна.<br>Изобарный процесс. При изобарном процессе согласно формуле (13.11) передаваемое газу количество теплоты идет на изменение его внутренней энергии и на соверше¬ние им работы при постоянном давлении:<br><br>Адиабатный процесс. Рассмотрим теперь процесс, про¬текающий в системе, которая не обменивается теплом с окружающими телами. Процесс в теплоизолированной системе называют адиабатным.<br>При адиабатном процессе ***** и согласно уравнению (13.10) изменение внутренней энергии происходит только за счет совершения работы:<br><br>Конечно, нельзя окружить систему оболочкой, абсо¬лютно не допускающей теплопередачу. Но в ряде случаев можно считать реальные процессы очень близкими к адиа¬батным. Для этого они должны протекать достаточно быстро, так, чтобы за время процесса не произошло за¬метного теплообмена между системой и окружающими те¬лами.<br>Согласно уравнению (13.14) при совершении над систе¬мой положительной работы, например при сжатии газа, его внутренняя энергия увеличивается, что означает повы¬шение температуры газа. И наоборот, при расширении газа сам газ совершает положительную работу ( *****)*****и****его внутренняя энергия уменьшается - газ охлаждается.<br>Нагревание воздуха при быстром сжатии нашло приме¬нение в двигателях Дизеля. В этих двигателях отсутствует система зажигания горючей смеси, необходимая для обыч¬ных карбюраторных двигателей внутреннего сгорания. В цилиндр засасывается не горючая смесь, а атмосферный воздух. К концу такта сжатия в цилиндр с помо¬щью специальной форсунки впрыс¬кивается жидкое топливо (рис. 13.8). К этому моменту температура воздуха так велика, что горючее воспламеня¬ется. Двигатели Дизеля имеют боль¬ший коэффициент полезного дейст¬вия, чем обычные, но более массивны и сложны в изготовлении и эксплуа¬тации. Все большее количество авто¬мобилей снабжается двигателями Ди¬зеля, благодаря дешевизне дизельного топлива.<br><br>При работе мощных компрессоров, сжимающих воздух, температура воз¬духа настолько увеличивается, что приходится прибегать к специальной системе охлаждения цилиндров. Адиабатное охлаждение газов при их расширении используется в машинах для сжижения газов.<br>Охлаждение газа при адиабатном расширении происходит в грандиозных масштабах в атмосфере Земли. Нагретый воздух поднимается вверх и расширяется, так как атмо¬сферное давление падает с увеличением высоты. Это расши¬рение сопровождается значительным охлаждением. В резу¬льтате водяные пары конденсируются и образуют облака.<br>Теплообмен в изолированной системе. Рассмотрим теп¬лообмен внутри системы, состоящей из нескольких тел, имеющих первоначально различные температуры, напри¬мер теплообмен между водой в сосуде и опущенным в воду горячим железным шариком. Будем считать, что система достаточно изолирована от окружающих тел и ее внутрен¬няя энергия не изменяется (изолированная система). Ни¬какой работы внутри этой системы не совершается. Тогда согласно первому закону термодинамики (см. уравнение (13.10)) изменение энергии любого тела системы равно ко¬личеству теплоты, отданной или полученной этим телом до наступления теплового равновесия внутри системы: ******. Складывая подобные выражения для всех тел си¬стемы и учитывая, что суммарная внутренняя энергия не меняется (*****), получим следующее уравнение:<br><br>Это уравнение носит название уравнения теплового ба¬ланса. Здесь ***** - количества теплоты, получен¬ные или отданные телами. Эти количества теплоты выра¬жаются формулой (13.5) или формулами (13.6)-(13.9), если в процессе теплообмена происходят превращения ве¬щества из жидкого состояния в газообразное или твердое (или же, напротив, образуется жидкость).<br>Внутренняя энергия идеального газа не изменяется только при изотермическом процессе. При изохорном она изменяется за счет теплопередачи, а при изобарном про¬цессе внутренняя энергия газа изменяется как за счет теп¬лопередачи, так и за счет совершения работы. В теплоизо¬лированной системе происходит адиабатный процесс. Изменение энергии системы в этом процессе равно работе внешних сил.<br><br><br>???<br>1. В каком случае работа газа больше: при изотермическом расширении от объема ***** до объема **** или при изобарном расширении от объема **** до объема *****?<br>2. Как следует записать уравнение теплового баланса для изоли¬рованной системы из трех тел. переходящей в равновесное состояние?<br>
| + | С помощью первого закона термодинамики можно делать важные заключения о характере протекающих процессов. Рассмотрим различные процессы, при которых одна из физических величин остается неизменной (изопроцессы), например случай, когда система представляет собой идеальный газ.<br> '''Изохорный процесс.''' При изохорном процессе объем газа не меняется, и поэтому работа газа равна нулю. Изменение внутренней энергии газа согласно уравнению (13.11) равно количеству переданной ему теплоты:<br>[[Image:a79-1.jpg|center]] Если газ нагревается, то [[Image:a79-7.jpg]], его внутренняя энергия увеличивается. При охлаждении газа [[Image:a79-8.jpg]] и [[Image:a79-9.jpg]], изменение внутренней энергии отрицательно и внутренняя энергия газа уменьшается.<br> '''Изотермический процесс.''' При изотермическом процессе (''T''=const) внутренняя энергия идеального газа (см. формулу (13.1)) не меняется. Согласно формуле (13.11) все переданное газу количество теплоты идет на совершение работы:<br>[[Image:a79-2.jpg|center]] Если газ получает тепло [[Image:a79-10.jpg]], то он совершает положительную работу [[Image:a79-11.jpg]]. Если, напротив, газ отдает тепло окружающей среде (термостату), то [[Image:a79-12.jpg]]. Работа же внешних сил над газом в последнем случае положительна.<br> '''Изобарный процесс.''' При изобарном процессе согласно формуле (13.11) передаваемое газу количество теплоты идет на изменение его внутренней энергии и на совершение им работы при постоянном давлении:<br>[[Image:a79-3.jpg|center]] '''Адиабатный процесс.''' Рассмотрим теперь процесс, протекающий в системе, которая не обменивается теплом с окружающими телами. Процесс в теплоизолированной системе называют '''адиабатным'''.<br> При адиабатном процессе ''Q''=0 и согласно уравнению (13.10) изменение внутренней энергии происходит только за счет совершения работы:<br>[[Image:a79-4.jpg|center]] Конечно, нельзя окружить систему оболочкой, абсолютно не допускающей теплопередачу. Но в ряде случаев можно считать реальные процессы очень близкими к адиабатным. Для этого они должны протекать достаточно быстро, так, чтобы за время процесса не произошло заметного теплообмена между системой и окружающими телами.<br> Согласно уравнению (13.14) при совершении над системой положительной работы, например при сжатии газа, его внутренняя энергия увеличивается, что означает повышение температуры газа. И наоборот, при расширении газа сам газ совершает положительную работу [[Image:a79-11.jpg]] и его внутренняя энергия уменьшается - газ охлаждается.<br> Нагревание воздуха при быстром сжатии нашло применение в двигателях Дизеля. В этих двигателях отсутствует система зажигания горючей смеси, необходимая для обычных карбюраторных двигателей внутреннего сгорания. В цилиндр засасывается не горючая смесь, а атмосферный воздух. К концу такта сжатия в цилиндр с помощью специальной форсунки впрыскивается жидкое топливо (''рис.13.8''). К этому моменту температура воздуха так велика, что горючее воспламеняется. Двигатели Дизеля имеют больший коэффициент полезного действия, чем обычные, но более массивны и сложны в изготовлении и эксплуатации. Все большее количество автомобилей снабжается двигателями Дизеля, благодаря дешевизне дизельного топлива.<br>[[Image:a13.8.jpg|center]] При работе мощных компрессоров, сжимающих воздух, температура воздуха настолько увеличивается, что приходится прибегать к специальной системе охлаждения цилиндров. Адиабатное охлаждение газов при их расширении используется в машинах для сжижения газов.<br> Охлаждение газа при адиабатном расширении происходит в грандиозных масштабах в атмосфере Земли. Нагретый воздух поднимается вверх и расширяется, так как атмосферное давление падает с увеличением высоты. Это расширение сопровождается значительным охлаждением. В результате водяные пары конденсируются и образуют облака.<br> '''Теплообмен в изолированной системе.''' Рассмотрим теплообмен внутри системы, состоящей из нескольких тел, имеющих первоначально различные температуры, например теплообмен между водой в сосуде и опущенным в воду горячим железным шариком. Будем считать, что система достаточно изолирована от окружающих тел и ее внутренняя энергия не изменяется (изолированная система). Никакой работы внутри этой системы не совершается. Тогда согласно первому закону термодинамики (см. уравнение (13.10)) изменение энергии любого тела системы равно количеству теплоты, отданной или полученной этим телом до наступления теплового равновесия внутри системы. Складывая подобные выражения для всех тел системы и учитывая, что суммарная внутренняя энергия не меняется [[Image:a79-5.jpg]], получим следующее уравнение:<br>[[Image:a79-6.jpg|center]] Это уравнение носит название '''уравнения теплового баланса'''. Здесь [[Image:a79-13.jpg]] - количества теплоты, полученные или отданные телами. Эти количества теплоты выражаются формулой (13.5) или формулами (13.6)-(13.9), если в процессе теплообмена происходят превращения вещества из жидкого состояния в газообразное или твердое (или же, напротив, образуется жидкость).<br> Внутренняя энергия идеального газа не изменяется только при изотермическом процессе. При изохорном она изменяется за счет теплопередачи, а при изобарном процессе внутренняя энергия газа изменяется как за счет теплопередачи, так и за счет совершения работы. В теплоизолированной системе происходит адиабатный процесс. Изменение энергии системы в этом процессе равно работе внешних сил.<br><br><br> ???<br> 1. В каком случае работа газа больше: при изотермическом расширении от объема ''V<sub>1</sub> ''до объема ''V<sub>2</sub>'' или при изобарном расширении от объема ''V<sub>1</sub> ''до объема ''V<sub>2</sub>''?<br> 2. Как следует записать уравнение теплового баланса для изолированной системы из трех тел, переходящей в равновесное состояние?<br> |
| | | | |
| - | | + | <br> ''Г.Я.Мякишев, Б.Б.Буховцев, Н.Н.Сотский, Физика 10 класс'' |
| - | ''Г.Я.Мякишев, Б.Б.Буховцев, Н.Н.Сотский, Физика 10 класс'' | + | |
| | | | |
| | <br> <sub>Планирование уроков [[Физика и астрономия|по физике]], ответы на тесты, задания и ответы по классам, домашнее задание и работа [[Физика 10 класс|по физике для 10 класса]]</sub> | | <br> <sub>Планирование уроков [[Физика и астрономия|по физике]], ответы на тесты, задания и ответы по классам, домашнее задание и работа [[Физика 10 класс|по физике для 10 класса]]</sub> |
Версия 22:25, 21 августа 2010
Гипермаркет знаний>>Физика и астрономия>>Физика 10 класс>>Физика: Применение первого закона термодинамики к различным процессам
С помощью первого закона термодинамики можно делать важные заключения о характере протекающих процессов. Рассмотрим различные процессы, при которых одна из физических величин остается неизменной (изопроцессы), например случай, когда система представляет собой идеальный газ.
Изохорный процесс. При изохорном процессе объем газа не меняется, и поэтому работа газа равна нулю. Изменение внутренней энергии газа согласно уравнению (13.11) равно количеству переданной ему теплоты:
Если газ нагревается, то 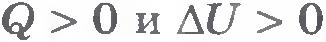 , его внутренняя энергия увеличивается. При охлаждении газа , его внутренняя энергия увеличивается. При охлаждении газа  и и  , изменение внутренней энергии отрицательно и внутренняя энергия газа уменьшается. , изменение внутренней энергии отрицательно и внутренняя энергия газа уменьшается.
Изотермический процесс. При изотермическом процессе (T=const) внутренняя энергия идеального газа (см. формулу (13.1)) не меняется. Согласно формуле (13.11) все переданное газу количество теплоты идет на совершение работы:
Если газ получает тепло  , то он совершает положительную работу , то он совершает положительную работу 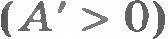 . Если, напротив, газ отдает тепло окружающей среде (термостату), то . Если, напротив, газ отдает тепло окружающей среде (термостату), то  . Работа же внешних сил над газом в последнем случае положительна. . Работа же внешних сил над газом в последнем случае положительна.
Изобарный процесс. При изобарном процессе согласно формуле (13.11) передаваемое газу количество теплоты идет на изменение его внутренней энергии и на совершение им работы при постоянном давлении:
Адиабатный процесс. Рассмотрим теперь процесс, протекающий в системе, которая не обменивается теплом с окружающими телами. Процесс в теплоизолированной системе называют адиабатным.
При адиабатном процессе Q=0 и согласно уравнению (13.10) изменение внутренней энергии происходит только за счет совершения работы:
Конечно, нельзя окружить систему оболочкой, абсолютно не допускающей теплопередачу. Но в ряде случаев можно считать реальные процессы очень близкими к адиабатным. Для этого они должны протекать достаточно быстро, так, чтобы за время процесса не произошло заметного теплообмена между системой и окружающими телами.
Согласно уравнению (13.14) при совершении над системой положительной работы, например при сжатии газа, его внутренняя энергия увеличивается, что означает повышение температуры газа. И наоборот, при расширении газа сам газ совершает положительную работу 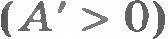 и его внутренняя энергия уменьшается - газ охлаждается. и его внутренняя энергия уменьшается - газ охлаждается.
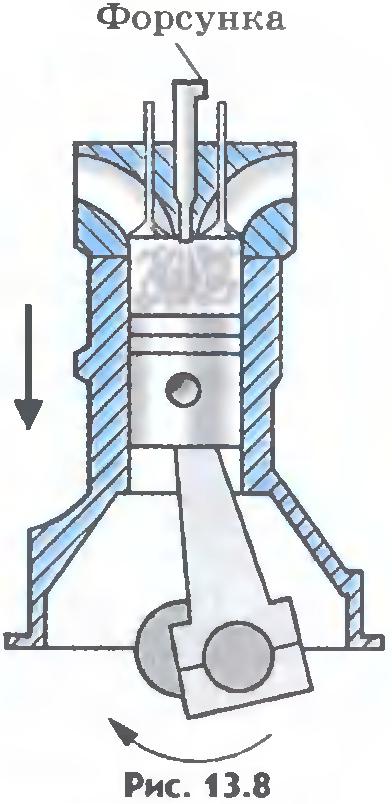
Нагревание воздуха при быстром сжатии нашло применение в двигателях Дизеля. В этих двигателях отсутствует система зажигания горючей смеси, необходимая для обычных карбюраторных двигателей внутреннего сгорания. В цилиндр засасывается не горючая смесь, а атмосферный воздух. К концу такта сжатия в цилиндр с помощью специальной форсунки впрыскивается жидкое топливо (рис.13.8). К этому моменту температура воздуха так велика, что горючее воспламеняется. Двигатели Дизеля имеют больший коэффициент полезного действия, чем обычные, но более массивны и сложны в изготовлении и эксплуатации. Все большее количество автомобилей снабжается двигателями Дизеля, благодаря дешевизне дизельного топлива.
При работе мощных компрессоров, сжимающих воздух, температура воздуха настолько увеличивается, что приходится прибегать к специальной системе охлаждения цилиндров. Адиабатное охлаждение газов при их расширении используется в машинах для сжижения газов.
Охлаждение газа при адиабатном расширении происходит в грандиозных масштабах в атмосфере Земли. Нагретый воздух поднимается вверх и расширяется, так как атмосферное давление падает с увеличением высоты. Это расширение сопровождается значительным охлаждением. В результате водяные пары конденсируются и образуют облака.
Теплообмен в изолированной системе. Рассмотрим теплообмен внутри системы, состоящей из нескольких тел, имеющих первоначально различные температуры, например теплообмен между водой в сосуде и опущенным в воду горячим железным шариком. Будем считать, что система достаточно изолирована от окружающих тел и ее внутренняя энергия не изменяется (изолированная система). Никакой работы внутри этой системы не совершается. Тогда согласно первому закону термодинамики (см. уравнение (13.10)) изменение энергии любого тела системы равно количеству теплоты, отданной или полученной этим телом до наступления теплового равновесия внутри системы. Складывая подобные выражения для всех тел системы и учитывая, что суммарная внутренняя энергия не меняется  , получим следующее уравнение: , получим следующее уравнение:
Это уравнение носит название уравнения теплового баланса. Здесь  - количества теплоты, полученные или отданные телами. Эти количества теплоты выражаются формулой (13.5) или формулами (13.6)-(13.9), если в процессе теплообмена происходят превращения вещества из жидкого состояния в газообразное или твердое (или же, напротив, образуется жидкость). - количества теплоты, полученные или отданные телами. Эти количества теплоты выражаются формулой (13.5) или формулами (13.6)-(13.9), если в процессе теплообмена происходят превращения вещества из жидкого состояния в газообразное или твердое (или же, напротив, образуется жидкость).
Внутренняя энергия идеального газа не изменяется только при изотермическом процессе. При изохорном она изменяется за счет теплопередачи, а при изобарном процессе внутренняя энергия газа изменяется как за счет теплопередачи, так и за счет совершения работы. В теплоизолированной системе происходит адиабатный процесс. Изменение энергии системы в этом процессе равно работе внешних сил.
???
1. В каком случае работа газа больше: при изотермическом расширении от объема V1 до объема V2 или при изобарном расширении от объема V1 до объема V2?
2. Как следует записать уравнение теплового баланса для изолированной системы из трех тел, переходящей в равновесное состояние?
Г.Я.Мякишев, Б.Б.Буховцев, Н.Н.Сотский, Физика 10 класс
Планирование уроков по физике, ответы на тесты, задания и ответы по классам, домашнее задание и работа по физике для 10 класса
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|
 , получим следующее уравнение:
, получим следующее уравнение: