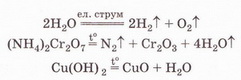|
|
|
| Строка 1: |
Строка 1: |
| | '''[[Гіпермаркет Знань - перший в світі!|Гіпермаркет Знань]]>>[[Хімія|Хімія]]>>[[Хімія 9 клас|Хімія 9 клас]]>> Хімія: Класифікація хімічних реакцій за різними ознаками. Реакції сполучення, розкладу, заміщення, обміну. Оборотні й необоротні реакції''' | | '''[[Гіпермаркет Знань - перший в світі!|Гіпермаркет Знань]]>>[[Хімія|Хімія]]>>[[Хімія 9 клас|Хімія 9 клас]]>> Хімія: Класифікація хімічних реакцій за різними ознаками. Реакції сполучення, розкладу, заміщення, обміну. Оборотні й необоротні реакції''' |
| | | | |
| - | <br> <metakeywords>Хімія, клас, урок, на тему, 9 клас, Класифікація хімічних реакцій, реакцій за різними ознаками, Реакції сполучення, розкладу, заміщення, обміну, Оборотні й необоротні реакції.</metakeywords>КЛАСИФІКАЦІЯ ХІМІЧНИХ РЕАКЦІЙ ЗА РІЗНИМИ ОЗНАКАМИ. РЕАКЦІЇ СПОЛУЧЕННЯ, РОЗКЛАДУ, ЗАМІЩЕННЯ, ОБМІНУ. ОБОРОТНІ Й НЕОБОРОТНІ РЕАКЦІЇ
| + | <metakeywords>Хімія, клас, урок, на тему, 9 клас, Класифікація хімічних реакцій, реакцій за різними ознаками, Реакції сполучення, розкладу, заміщення, обміну, Оборотні й необоротні реакції.</metakeywords> |
| | + | |
| | + | КЛАСИФІКАЦІЯ ХІМІЧНИХ РЕАКЦІЙ ЗА РІЗНИМИ ОЗНАКАМИ. РЕАКЦІЇ СПОЛУЧЕННЯ, РОЗКЛАДУ, ЗАМІЩЕННЯ, ОБМІНУ. ОБОРОТНІ Й НЕОБОРОТНІ РЕАКЦІЇ |
| | | | |
| | <u><br></u> | | <u><br></u> |
| | | | |
| - | <u>Класифікація хімічних реакцій за різними ознаками</u> | + | <u>Класифікація хімічних реакцій за різними ознаками</u><br> |
| - | | + | |
| - | Після опрацювання § 13 ви зможете:
| + | |
| - | | + | |
| - | класифікувати реакції за кількістю і складом реагентів і продукту наводити приклади та розрізняти реакції сполучення, заміщення, обміну, розкладу, оцінювати їхнє значення.
| + | |
| - | | + | |
| - | На шляху до успіху пригадаємо з вивчених курсів хімії:
| + | |
| - | | + | |
| - | шо таке хімічне рівняння; які речовини називають простими, а які – складними; як класифікують хімічні реакції за кількістю і складом реагентів і продуктів.
| + | |
| | | | |
| | Хімічні реакції класифікують за різними ознаками (див. схему).<br> | | Хімічні реакції класифікують за різними ознаками (див. схему).<br> |
| Строка 19: |
Строка 13: |
| | Схема 13.1 | | Схема 13.1 |
| | | | |
| - | [[Image:Chemistry 92.jpg]]<br> | + | [[Image:Chemistry 92.jpg|Ознаки хімічних реакцій. фото]]<br> |
| | | | |
| | Які з цих ознак вам відомі, а які потребують уточнення й докладнішого вивчення (табл. 13.1)? | | Які з цих ознак вам відомі, а які потребують уточнення й докладнішого вивчення (табл. 13.1)? |
| Строка 25: |
Строка 19: |
| | Таблиця 13.1 | | Таблиця 13.1 |
| | | | |
| - | [[Image:Chemistry 93.jpg]]<br> | + | [[Image:Chemistry 93.jpg|Ознаки. фото]]<br> |
| | | | |
| - | ''<u>Завдання</u>'' | + | '''''Завдання''''' |
| | | | |
| | Оцініть відповідність інформації, наведеної у таблиці 13.1, вашим навчальним здобуткам. | | Оцініть відповідність інформації, наведеної у таблиці 13.1, вашим навчальним здобуткам. |
| Строка 35: |
Строка 29: |
| | Схема 13.2<br> | | Схема 13.2<br> |
| | | | |
| - | [[Image:Chemistry 93 1.jpg]] | + | [[Image:Chemistry 93 1.jpg|Хімічні реакції. Схема. фото]] |
| | | | |
| | Аби встановити за цією ознакою приналежність реакції до певного типу, треба проаналізувати її хімічне рівняння. Розгляньмо конкретні приклади. | | Аби встановити за цією ознакою приналежність реакції до певного типу, треба проаналізувати її хімічне рівняння. Розгляньмо конкретні приклади. |
| | | | |
| - | • ''Реакції розкладу.'' Під дією електричного струму вода розкладається на кисень і водень (мал. 13.1): [[Image:Chemistry 94 1x.jpg]] | + | • ''Реакції розкладу.'' Під дією електричного струму вода розкладається на кисень і водень (мал. 13.1): [[Image:Chemistry 94 1x.jpg|формула. фото]] |
| | | | |
| - | [[Image:Chemistry 94.jpg]] | + | [[Image:Chemistry 94.jpg|Електроліз води. фото]] |
| | | | |
| | ''<u>Завдання</u>'' | | ''<u>Завдання</u>'' |
| Строка 51: |
Строка 45: |
| | Роздивіться малюнок 13.2. Визначте, скільки і яких речовин бере участь у цій реакції та утворюється внаслідок її перебігу. | | Роздивіться малюнок 13.2. Визначте, скільки і яких речовин бере участь у цій реакції та утворюється внаслідок її перебігу. |
| | | | |
| - | [[Image:Chemistry 94 2.jpg]] | + | [[Image:Chemistry 94 2.jpg|Схематичне зображення електролізу води на мікрорівні. фото]] |
| | | | |
| - | Продуктами реакцій розкладу можуть бути як прості, так і складні речовини. Приміром, внаслідок термічного розкладання амоній дихромату утворюється одна проста (назвіть її) і дві складні (назвіть їх) речовини: | + | Продуктами реакцій розкладу можуть бути як [[Ілюстрації_до_уроку_«Прості_і_складні_речовини._Поняття_про_неорганічні_та_органічні_речовини.»|прості, так і складні речовини]]. Приміром, внаслідок термічного розкладання амоній дихромату утворюється одна проста (назвіть її) і дві складні (назвіть їх) речовини: |
| | | | |
| | (NH<sub>4</sub>)<sub>2</sub>Cr<sub>2</sub>O<sub>7</sub>[[Image:Znak 5.jpg]]N<sub>2</sub>↑ + Cr<sub>2</sub>O<sub>3</sub> + H<sub>2</sub>O | | (NH<sub>4</sub>)<sub>2</sub>Cr<sub>2</sub>O<sub>7</sub>[[Image:Znak 5.jpg]]N<sub>2</sub>↑ + Cr<sub>2</sub>O<sub>3</sub> + H<sub>2</sub>O |
| | | | |
| - | ''<u>Завдання</u>'' | + | '''Завдання''' |
| | | | |
| - | Перетворіть схему цієї реакції на хімічне рівняння. | + | ''Перетворіть схему цієї реакції на хімічне рівняння.'' |
| | | | |
| - | Ви, звичайно, пам'ятаєте, що внаслідок нагрівання купрум(ІІ) гідроксиду утворюються дві складні речовини: купрум(ІІ) оксид і вода. | + | Ви, звичайно, пам'ятаєте, що внаслідок нагрівання купрум(ІІ) гідроксиду утворюються дві складні речовини: купрум(ІІ) [[12._Оксиди,_їх_склад,_назви|оксид ]]і [[Вода_-_найпоширеніша_речовина_на_Землі._Повні_уроки|вода]]. |
| | | | |
| - | ''<u>Завдання</u>'' | + | '''Завдання''' |
| | | | |
| - | Запишіть хімічне рівняння реакції термічного розкладання купрум(ІІ) гідроксиду.<br> | + | ''Запишіть хімічне рівняння реакції термічного розкладання купрум(ІІ) гідроксиду.''<br> |
| | | | |
| | • ''Реакції сполучення'' є протилежністю реакцій розкладу (поясніть, чому). Вони можуть відбуватися за участю як простих, так і складних речовин. Продукт реакції між простими речовинами - магнієм і киснем - магній оксид (мал. 13.3). | | • ''Реакції сполучення'' є протилежністю реакцій розкладу (поясніть, чому). Вони можуть відбуватися за участю як простих, так і складних речовин. Продукт реакції між простими речовинами - магнієм і киснем - магній оксид (мал. 13.3). |
| | | | |
| - | [[Image:Chemistry 95.jpg]] | + | [[Image:Chemistry 95.jpg|Горіння магнію. фото]] |
| | | | |
| - | ''<u>Завдання</u>'' | + | '''Завдання''' |
| | | | |
| - | Перетворіть схему реакції горіння магнію на хімічне рівняння. | + | ''Перетворіть схему реакції горіння магнію на хімічне рівняння.'' |
| | | | |
| | Гідратація (взаємодія з водою) кислотних оксидів - приклад реакції сполучення за участю двох складних речовин. | | Гідратація (взаємодія з водою) кислотних оксидів - приклад реакції сполучення за участю двох складних речовин. |
| | | | |
| - | ''<u>Завдання</u>'' | + | '''Завдання''' |
| | | | |
| - | 1. Унаслідок гідратації оксидів Карбону(IV) та Сульфуру(ІV) утворюються шкідливі для довкілля кислотні дощі. Назвіть продукти гідратації цих оксидів. | + | ''1. Унаслідок гідратації оксидів Карбону(IV) та Сульфуру(ІV) утворюються шкідливі для довкілля кислотні дощі. Назвіть продукти гідратації цих оксидів.'' |
| | | | |
| - | 2. Виберіть частинки, які зумовлюють руйнівну дію кислотних дощів на ліси: <br>А Карбонат-аніони; Б Катіони Гідрогену; В Гідроксид-аніони; Г Сульфіт-аніони; Д Молекули води. | + | ''2. Виберіть частинки, які зумовлюють руйнівну дію кислотних дощів на ліси: <br>А Карбонат-аніони; Б Катіони Гідрогену; В Гідроксид-аніони; Г Сульфіт-аніони; Д Молекули води.'' |
| | | | |
| | Продуктом взаємодії карбон(ІІ) оксиду (чадного газу) з киснем є карбон(ІV) - вуглекислий газ. | | Продуктом взаємодії карбон(ІІ) оксиду (чадного газу) з киснем є карбон(ІV) - вуглекислий газ. |
| | | | |
| - | ''<u>Завдання</u>'' | + | '''Завдання''' |
| | | | |
| - | Запишіть рівняння реакції чадного газу з киснем. | + | ''Запишіть рівняння реакції чадного газу з киснем.'' |
| | | | |
| | • ''Реакції заміщення'' ви вивчали, досліджуючи взаємодію металів із кислотами та солями у розчинах. Тож (с. 105, мал. 14.4) умієте за допомогою ряду активності металів (починаючи від магнію кожний член ряду витісняє наступні з розчинів їхніх солей та водень з розчинів кислот) спрогнозувати можливість перебігу цих реакцій. Приміром, алюміній витісняє водень з хлоридної кислоти (мал. 13.4). Натомість мідь, срібло, золото тощо стійкі до дії розчинів кислот. | | • ''Реакції заміщення'' ви вивчали, досліджуючи взаємодію металів із кислотами та солями у розчинах. Тож (с. 105, мал. 14.4) умієте за допомогою ряду активності металів (починаючи від магнію кожний член ряду витісняє наступні з розчинів їхніх солей та водень з розчинів кислот) спрогнозувати можливість перебігу цих реакцій. Приміром, алюміній витісняє водень з хлоридної кислоти (мал. 13.4). Натомість мідь, срібло, золото тощо стійкі до дії розчинів кислот. |
| | | | |
| - | [[Image:Chemistry 95 1.jpg]] | + | [[Image:Chemistry 95 1.jpg|Взаємодія алюмінію з хлоридною кислотою. фото]] |
| | | | |
| - | ''<u>Завдання</u>'' | + | '''Завдання''' |
| | | | |
| - | 1. Запишіть рівняння реакції алюмінію з хлоридною кислотою. 2. Поясніть, чому водень можна зібрати до посудини витісненням води. 3. Назвіть йони, які зумовлюють властивість хлоридної кислоти взаємодіяти з металами. | + | ''1. Запишіть рівняння реакції алюмінію з хлоридною кислотою. 2. Поясніть, чому водень можна зібрати до посудини витісненням води. 3. Назвіть йони, які зумовлюють властивість хлоридної кислоти взаємодіяти з [[Відео_до_уроку:_Багатоманітність_речовин._Прості_й_складні_речовини._Метали_й_неметали|металами]].'' |
| | | | |
| - | Мідь по-різному поводитиметься у розчинах аргентум(І) нітрату та цинк нітрату: реакція відбуватиметься лише з однією із солей (мал. 13.5). | + | Мідь по-різному поводитиметься у розчинах аргентум(І) нітрату та цинк нітрату: реакція відбуватиметься лише з однією із [[14._Солі_(середні),_їх_склад,_назви|солей ]](мал. 13.5). |
| | | | |
| - | [[Image:Chemistry 96.jpg]] | + | [[Image:Chemistry 96.jpg|Мідь по-різному проводиться у розчинах цинк нітрату та рагентум нітрату. фото]] |
| | | | |
| - | ''<u>Завдання</u>'' | + | '''Завдання''' |
| | | | |
| - | Визначте, використовуючи ряд активності металів (с. 105, мал. 14.4) у якій з двох колб (мал. 13.5) до початку реакції містився розчин аргентум(І) нітрату<br>• ''Реакції обміну'', як ви вже пересвідчилися, здебільшого відбуваються між електролітами у розчинах. Ці реакції проходять до кінця лише за певних умов (назвіть їх, за потреби зверніться до § 12). Загальний вигляд реакцій обміну, які ви вивчали, такий: | + | ''Визначте, використовуючи ряд активності металів (с. 105, мал. 14.4) у якій з двох колб (мал. 13.5) до початку реакції містився розчин аргентум(І) нітрату''<br>• ''Реакції обміну'', як ви вже пересвідчилися, здебільшого відбуваються між електролітами у розчинах. Ці реакції проходять до кінця лише за певних умов (назвіть їх, за потреби зверніться до § 12). Загальний вигляд реакцій обміну, які ви вивчали, такий: |
| | | | |
| | Основний оксид + кислота → сіль + вода. Кислотний оксид + луг → сіль + вода. <br>Луг + кислота → сіль + вода.<br>Нерозчинна основа + кислота → сіль + вода. <br>Сіль' + кислота' → сіль" + кислота".<br>Сіль' + луг → сіль" + основа↓.<br>*Амфотерний оксид + кислота → сіль + вода.<br>*Амфотерний оксид + луг → сіль + вода. <br>*Амфотерний гідроксид + кислота → сіль + вода. <br>*Амфотерний гідроксид + луг → сіль + вода. | | Основний оксид + кислота → сіль + вода. Кислотний оксид + луг → сіль + вода. <br>Луг + кислота → сіль + вода.<br>Нерозчинна основа + кислота → сіль + вода. <br>Сіль' + кислота' → сіль" + кислота".<br>Сіль' + луг → сіль" + основа↓.<br>*Амфотерний оксид + кислота → сіль + вода.<br>*Амфотерний оксид + луг → сіль + вода. <br>*Амфотерний гідроксид + кислота → сіль + вода. <br>*Амфотерний гідроксид + луг → сіль + вода. |
| | | | |
| - | ''<u>Завдання</u>'' | + | '''Завдання''' |
| | | | |
| - | До наведених у загальному вигляді записів реакцій обміну доберіть конкретні приклади. Запишіть, користуючись таблицею «Розчинність кислот основ і солей у воді», рівняння реакцій у повній і скороченій йонних формах (завдання* виконувати не обов'язково). | + | ''До наведених у загальному вигляді записів реакцій обміну доберіть конкретні приклади. Запишіть, користуючись таблицею «Розчинність кислот основ і солей у воді», рівняння реакцій у повній і скороченій йонних формах (завдання* виконувати не обов'язково).'' |
| | | | |
| | • ''Значення реакцій сполучення, розкладу, заміщення та обміну'' важко переоцінити. За допомогою реакцій цих та інших типів людство забезпечує потребу у речовинах, матеріалах і сучасних технологіях розгляньмо кілька прикладів. Приміром, промисловий спосіб добування амоніаку ґрунтується на його синтезі з простих речовин: | | • ''Значення реакцій сполучення, розкладу, заміщення та обміну'' важко переоцінити. За допомогою реакцій цих та інших типів людство забезпечує потребу у речовинах, матеріалах і сучасних технологіях розгляньмо кілька прикладів. Приміром, промисловий спосіб добування амоніаку ґрунтується на його синтезі з простих речовин: |
| Строка 127: |
Строка 121: |
| | NiCl<sub>2</sub> + NaOH → Ni(OH)<sub>2</sub>↓ + NaCl | | NiCl<sub>2</sub> + NaOH → Ni(OH)<sub>2</sub>↓ + NaCl |
| | | | |
| - | ''<u>Завдання</u>'' | + | '''Завдання''' |
| | | | |
| - | Перетворіть схеми реакцій на хімічні рівняння. Рівняння реакції йонного обміну запишіть у повній і скороченій йонних формах. | + | ''Перетворіть схеми реакцій на хімічні рівняння. Рівняння реакції йонного обміну запишіть у повній і скороченій йонних формах.'' |
| | | | |
| | Звичайно, класифікація хімічних реакцій на чотири розглянуті типи не є універсальною та всеосяжною. Під час подальшого вивчення хімії, зокрема реакцій за участю органічних сполук, ви розширите й поглибите свої уявлення щодо підходів до класифікації хімічних реакцій за ознакою кількості та складу реагентів і продуктів. Про класифікацію хімічних реакцій за іншими ознаками йтиметься у наступних параграфах. | | Звичайно, класифікація хімічних реакцій на чотири розглянуті типи не є універсальною та всеосяжною. Під час подальшого вивчення хімії, зокрема реакцій за участю органічних сполук, ви розширите й поглибите свої уявлення щодо підходів до класифікації хімічних реакцій за ознакою кількості та складу реагентів і продуктів. Про класифікацію хімічних реакцій за іншими ознаками йтиметься у наступних параграфах. |
| | | | |
| - | <u>Стисло про головне</u>
| + | '''Стисло про головне''' |
| | | | |
| | Хімічні реакції класифікують за різними ознаками - кількістю і складом реагентів і продуктів, тепловим ефектом, зміною ступенів окиснення елементів, оборотністю тощо. | | Хімічні реакції класифікують за різними ознаками - кількістю і складом реагентів і продуктів, тепловим ефектом, зміною ступенів окиснення елементів, оборотністю тощо. |
| Строка 141: |
Строка 135: |
| | Реакції розкладу відбуваються за участю одного реагенту з утворенням кількох продуктів: | | Реакції розкладу відбуваються за участю одного реагенту з утворенням кількох продуктів: |
| | | | |
| - | [[Image:Chemistry 97 1x.jpg]]<br> | + | [[Image:Chemistry 97 1x.jpg|формули. фото]]<br> |
| | | | |
| | Їхня протилежність - реакції сполучення. У них беруть участь кілька реагентів й утворюється один продукт: | | Їхня протилежність - реакції сполучення. У них беруть участь кілька реагентів й утворюється один продукт: |
| Строка 155: |
Строка 149: |
| | СаО + 2HNО<sub>3</sub> = Са(NO<sub>3</sub>)<sub>2</sub> + Н<sub>2</sub>0 <br>КОН + НВг = КВг + Н<sub>2</sub>0 <br>РЬ(ОН)<sub>2</sub> + 2НNO<sub>3</sub> = РЬ(NO<sub>3</sub>)<sub>2</sub> + 2Н<sub>2</sub>0<br>Nа<sub>2</sub>S + 2НСl = 2NаСl + Н<sub>2</sub>S↑<br>К<sub>2</sub>S0<sub>4 </sub>+ Ва(ОН)<sub>2</sub> = 2КОН +ВаS0<sub>4</sub>↓<br>NіСl<sub>2</sub> + 2Na0Н = Ni(ОН)<sub>2</sub>↓ + 2NаСl<br> | | СаО + 2HNО<sub>3</sub> = Са(NO<sub>3</sub>)<sub>2</sub> + Н<sub>2</sub>0 <br>КОН + НВг = КВг + Н<sub>2</sub>0 <br>РЬ(ОН)<sub>2</sub> + 2НNO<sub>3</sub> = РЬ(NO<sub>3</sub>)<sub>2</sub> + 2Н<sub>2</sub>0<br>Nа<sub>2</sub>S + 2НСl = 2NаСl + Н<sub>2</sub>S↑<br>К<sub>2</sub>S0<sub>4 </sub>+ Ва(ОН)<sub>2</sub> = 2КОН +ВаS0<sub>4</sub>↓<br>NіСl<sub>2</sub> + 2Na0Н = Ni(ОН)<sub>2</sub>↓ + 2NаСl<br> |
| | | | |
| - | <u>Застосуйте свої знання й уміння</u><br>
| + | '''Застосуйте свої знання й уміння'''<br> |
| | | | |
| - | 1.Виберіть схему реакції заміщення:<br>А CО + СІ<sub>2</sub> → СОСІ<sub>2</sub>; <br>Б СН<sub>4</sub> → С + Н<sub>2</sub>;<br>В MgO + HNO<sub>3</sub> → Mg(N0<sub>3</sub>)<sub>2 </sub>+ Н<sub>2</sub>0; <br>Г MnO<sub>2</sub> + AI → Al<sub>2</sub>O<sub>3 </sub>+ Mn.<br> | + | ''1.Виберіть схему реакції заміщення:<br>А CО + СІ<sub>2</sub> → СОСІ<sub>2</sub>; <br>Б СН<sub>4</sub> → С + Н<sub>2</sub>;<br>В MgO + HNO<sub>3</sub> → Mg(N0<sub>3</sub>)<sub>2 </sub>+ Н<sub>2</sub>0; <br>Г MnO<sub>2</sub> + AI → Al<sub>2</sub>O<sub>3 </sub>+ Mn.<br>'' |
| | | | |
| - | 2.Встановіть відповідність між схемами хімічних реакцій та їхніми типами: | + | ''2.Встановіть відповідність між схемами хімічних реакцій та їхніми типами:'' |
| | | | |
| - | [[Image:Chemistry 98.jpg]] | + | [[Image:Chemistry 98.jpg|таблиця. фото]] |
| | | | |
| - | 3. а) Виберіть реакцію, яка є різновидом реакції обміну:<br>А Горіння кальцію; Б Взаємодія хлору з воднем; В Реакція нейтралізації; Г Добування кисню з гідроген пероксиду.<br>б) Наведіть приклад такої реакції, запишіть її рівняння у повній і скороченій йонних формах. | + | ''3. а) Виберіть реакцію, яка є різновидом реакції обміну:<br>А Горіння кальцію; Б Взаємодія хлору з воднем; В Реакція нейтралізації; Г Добування кисню з гідроген пероксиду.<br>б) Наведіть приклад такої реакції, запишіть її рівняння у повній і скороченій йонних формах.'' |
| | | | |
| - | 4. Виберіть реакцію сполучення, у хімічному рівнянні якої сума коефіцієнтів становить 5:<br>А Прожарювання міді; Б Нагрівання калій перманганату; В Прожарювання ферум(ІІІ) гідроксиду; Г Спалювання сірки. | + | ''4. Виберіть реакцію сполучення, у хімічному рівнянні якої сума коефіцієнтів становить 5:<br>А Прожарювання міді; Б Нагрівання калій перманганату; В Прожарювання ферум(ІІІ) гідроксиду; Г Спалювання сірки.'' |
| | | | |
| - | 5.Визначте, про яку реакцію йдеться в уривку літературного твору. Запишіть її хімічне рівняння. Класифікуйте цю реакцію за кількістю та складом реагентів і продуктів. | + | ''5.Визначте, про яку реакцію йдеться в уривку літературного твору. Запишіть її хімічне рівняння. Класифікуйте цю реакцію за кількістю та складом реагентів і продуктів.'' |
| | | | |
| - | «Шипить та куриться вапно, що його гасять у великих дощаних скринях» (І. Франка). | + | ''«Шипить та куриться вапно, що його гасять у великих дощаних скринях» (І. Франка).'' |
| | | | |
| - | 6. До складу антацидних (проти печії) лікарських препаратів «Маалокс» і «Алмагель» входять магній гідроксид і алюміній гідроксид. Складіть рівняння реакцій цих сполук із хлоридною кислотою - головною складовою шлун-кового соку. Класифікуйте реакції за кількістю та складом реагентів і продуктів. Запишіть їхні рівняння у повній і скороченій йонній формах. Визначте, які йони у складі шлункового соку є причиною печії. | + | ''6. До складу антацидних (проти печії) лікарських препаратів «Маалокс» і «Алмагель» входять магній гідроксид і алюміній гідроксид. Складіть рівняння реакцій цих сполук із хлоридною кислотою - головною складовою шлун-кового соку. Класифікуйте реакції за кількістю та складом реагентів і продуктів. Запишіть їхні рівняння у повній і скороченій йонній формах. Визначте, які йони у складі шлункового соку є причиною печії.'' |
| | | | |
| - | 7. Художнику доручили ілюструвати підручник хімії для дев'ятикласників. Хімічні реакції розкладу, сполучення, заміщення, обміну він зобразив у такий спосіб (мал. 13.6). Оцініть, чи правильно художник змоделював хімічні реакції різних типів. Обґрунтуйте свій експертний висновок. | + | ''7. Художнику доручили ілюструвати підручник хімії для дев'ятикласників. Хімічні реакції розкладу, сполучення, заміщення, обміну він зобразив у такий спосіб (мал. 13.6). Оцініть, чи правильно художник змоделював хімічні реакції різних типів. Обґрунтуйте свій експертний висновок.'' |
| | | | |
| - | [[Image:Chemistry 99.jpg]] | + | [[Image:Chemistry 99.jpg|Реакції. фото]] |
| | | | |
| - | 8. Наведіть приклад реакції сполучення, у рівнянні якої сума коефіцієнтів становить 11. | + | ''8. Наведіть приклад реакції сполучення, у рівнянні якої сума коефіцієнтів становить 11.'' |
| | | | |
| - | 9. Наведіть приклад реакції обміну, у рівнянні якої сума коефіцієнтів становить 12. | + | ''9. Наведіть приклад реакції обміну, у рівнянні якої сума коефіцієнтів становить 12.'' |
| | | | |
| - | 10. Наведіть приклад реакції заміщення, у рівнянні якої сума коефіцієнтів становить 7. | + | ''10. Наведіть приклад реакції заміщення, у рівнянні якої сума коефіцієнтів становить 7.'' |
| | | | |
| - | 11. Використовуючи різноманітні джерела інформації, відшукайте приклади рівнянь хімічних реакцій, які за формальними ознаками не можна віднести до жодного з типів, розглянутих у § 13. | + | ''11. Використовуючи різноманітні джерела інформації, відшукайте приклади рівнянь хімічних реакцій, які за формальними ознаками не можна віднести до жодного з типів, розглянутих у § 13.'' |
| | | | |
| - | <u>Скарбничка досвіду</u> | + | '''<u>Скарбничка досвіду</u>''' |
| | | | |
| - | Уявіть себе: | + | ''Уявіть себе:'' |
| | | | |
| - | • художником, якому доручили ілюструвати підручник хімії для дев'ятикласників. Намалюйте комікси, які зображують хімічні реакції сполучення, розкладу, заміщення, обміну. Якщо вмієте працювати з відповідними комп'ютерними програмами - створіть анімаційний фільм; | + | ''• художником, якому доручили ілюструвати підручник хімії для дев'ятикласників. Намалюйте комікси, які зображують хімічні реакції сполучення, розкладу, заміщення, обміну. Якщо вмієте працювати з відповідними комп'ютерними програмами - створіть анімаційний фільм;'' |
| | | | |
| - | • режисером навчального фільму, в якому йдеться про класифікацію хімічних реакцій за кількістю та складом реагентів і продуктів реакції. Жанр фільму - мюзикл. Ролі формульних одиниць речовин можуть виконати ваші однокласники, приятелі, родичі тощо. Вони ж можуть узяти на себе функції художників по костюмах, дизайнерів, відеооператорів, постановників. Напишіть сценарій такого фільму, зніміть його й презентуйте.<br> | + | ''• режисером навчального фільму, в якому йдеться про класифікацію хімічних реакцій за кількістю та складом реагентів і продуктів реакції. Жанр фільму - мюзикл. Ролі формульних одиниць речовин можуть виконати ваші однокласники, приятелі, родичі тощо. Вони ж можуть узяти на себе функції художників по костюмах, дизайнерів, відеооператорів, постановників. Напишіть сценарій такого фільму, зніміть його й презентуйте.''<br> |
| | | | |
| | <br> | | <br> |
| | | | |
| - | ''Г. А. Лашевська, Хімія, 9 клас<br>Вислано читачами з інтернет-сайтів '' | + | ''Г. А. Лашевська, [[Хімія_9_клас|Хімія, 9 клас]]<br>Вислано читачами з інтернет-сайтів '' |
| | | | |
| | <br> <sub>Матеріали [[Хімія|з хімії]], планування з хімії, [[Гіпермаркет Знань - перший в світі!|завдання]] та відповіді по класам, плани конспектів уроків [[Хімія 9 клас|з хімії для 9 класу]]</sub> | | <br> <sub>Матеріали [[Хімія|з хімії]], планування з хімії, [[Гіпермаркет Знань - перший в світі!|завдання]] та відповіді по класам, плани конспектів уроків [[Хімія 9 клас|з хімії для 9 класу]]</sub> |
Текущая версия на 11:52, 18 июля 2012
Гіпермаркет Знань>>Хімія>>Хімія 9 клас>> Хімія: Класифікація хімічних реакцій за різними ознаками. Реакції сполучення, розкладу, заміщення, обміну. Оборотні й необоротні реакції
КЛАСИФІКАЦІЯ ХІМІЧНИХ РЕАКЦІЙ ЗА РІЗНИМИ ОЗНАКАМИ. РЕАКЦІЇ СПОЛУЧЕННЯ, РОЗКЛАДУ, ЗАМІЩЕННЯ, ОБМІНУ. ОБОРОТНІ Й НЕОБОРОТНІ РЕАКЦІЇ
Класифікація хімічних реакцій за різними ознаками
Хімічні реакції класифікують за різними ознаками (див. схему).
Схема 13.1
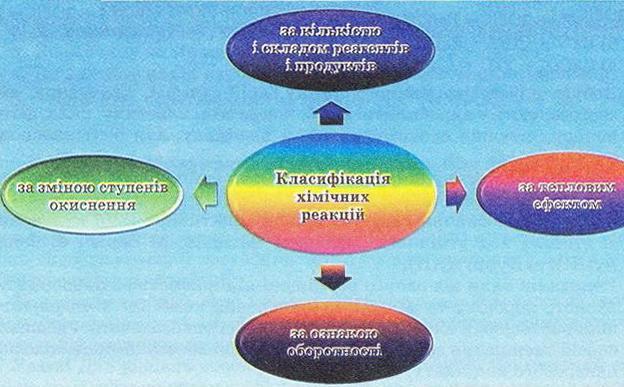
Які з цих ознак вам відомі, а які потребують уточнення й докладнішого вивчення (табл. 13.1)?
Таблиця 13.1
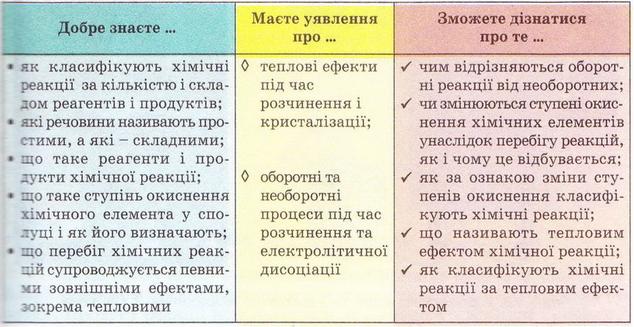
Завдання
Оцініть відповідність інформації, наведеної у таблиці 13.1, вашим навчальним здобуткам.
Класифікацію хімічних реакцій за кількістю і складом реагентів і продуктів узагальнено на схемі 13.2.
Схема 13.2
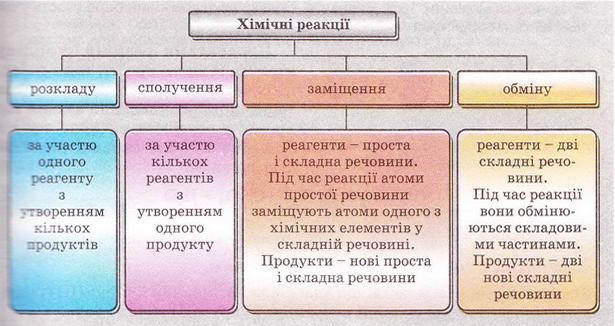
Аби встановити за цією ознакою приналежність реакції до певного типу, треба проаналізувати її хімічне рівняння. Розгляньмо конкретні приклади.
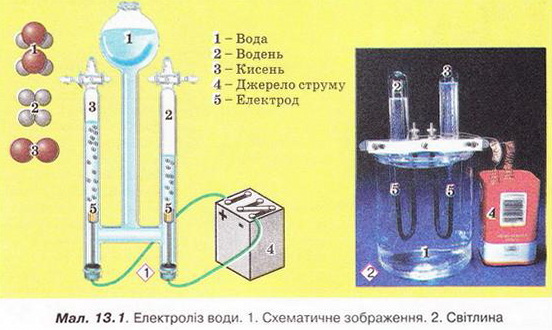
• Реакції розкладу. Під дією електричного струму вода розкладається на кисень і водень (мал. 13.1): 
Завдання
Перетворіть схему цієї реакції на хімічне рівняння.
Завдання
Роздивіться малюнок 13.2. Визначте, скільки і яких речовин бере участь у цій реакції та утворюється внаслідок її перебігу.
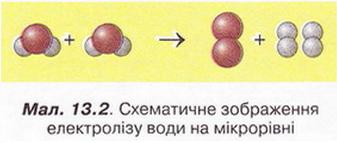
Продуктами реакцій розкладу можуть бути як прості, так і складні речовини. Приміром, внаслідок термічного розкладання амоній дихромату утворюється одна проста (назвіть її) і дві складні (назвіть їх) речовини:
(NH4)2Cr2O7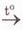 N2↑ + Cr2O3 + H2O N2↑ + Cr2O3 + H2O
Завдання
Перетворіть схему цієї реакції на хімічне рівняння.
Ви, звичайно, пам'ятаєте, що внаслідок нагрівання купрум(ІІ) гідроксиду утворюються дві складні речовини: купрум(ІІ) оксид і вода.
Завдання
Запишіть хімічне рівняння реакції термічного розкладання купрум(ІІ) гідроксиду.
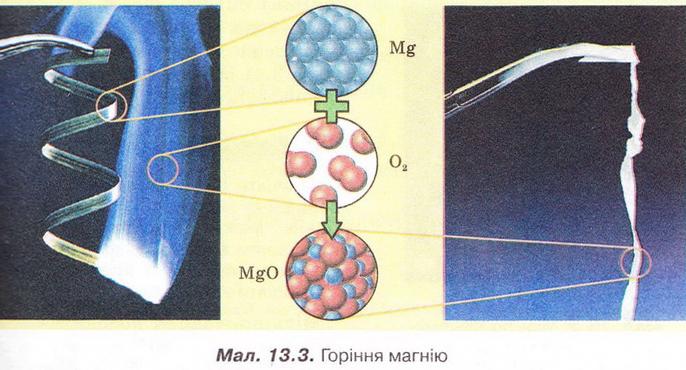
• Реакції сполучення є протилежністю реакцій розкладу (поясніть, чому). Вони можуть відбуватися за участю як простих, так і складних речовин. Продукт реакції між простими речовинами - магнієм і киснем - магній оксид (мал. 13.3).
Завдання
Перетворіть схему реакції горіння магнію на хімічне рівняння.
Гідратація (взаємодія з водою) кислотних оксидів - приклад реакції сполучення за участю двох складних речовин.
Завдання
1. Унаслідок гідратації оксидів Карбону(IV) та Сульфуру(ІV) утворюються шкідливі для довкілля кислотні дощі. Назвіть продукти гідратації цих оксидів.
2. Виберіть частинки, які зумовлюють руйнівну дію кислотних дощів на ліси:
А Карбонат-аніони; Б Катіони Гідрогену; В Гідроксид-аніони; Г Сульфіт-аніони; Д Молекули води.
Продуктом взаємодії карбон(ІІ) оксиду (чадного газу) з киснем є карбон(ІV) - вуглекислий газ.
Завдання
Запишіть рівняння реакції чадного газу з киснем.
• Реакції заміщення ви вивчали, досліджуючи взаємодію металів із кислотами та солями у розчинах. Тож (с. 105, мал. 14.4) умієте за допомогою ряду активності металів (починаючи від магнію кожний член ряду витісняє наступні з розчинів їхніх солей та водень з розчинів кислот) спрогнозувати можливість перебігу цих реакцій. Приміром, алюміній витісняє водень з хлоридної кислоти (мал. 13.4). Натомість мідь, срібло, золото тощо стійкі до дії розчинів кислот.

Завдання
1. Запишіть рівняння реакції алюмінію з хлоридною кислотою. 2. Поясніть, чому водень можна зібрати до посудини витісненням води. 3. Назвіть йони, які зумовлюють властивість хлоридної кислоти взаємодіяти з металами.
Мідь по-різному поводитиметься у розчинах аргентум(І) нітрату та цинк нітрату: реакція відбуватиметься лише з однією із солей (мал. 13.5).

Завдання
Визначте, використовуючи ряд активності металів (с. 105, мал. 14.4) у якій з двох колб (мал. 13.5) до початку реакції містився розчин аргентум(І) нітрату
• Реакції обміну, як ви вже пересвідчилися, здебільшого відбуваються між електролітами у розчинах. Ці реакції проходять до кінця лише за певних умов (назвіть їх, за потреби зверніться до § 12). Загальний вигляд реакцій обміну, які ви вивчали, такий:
Основний оксид + кислота → сіль + вода. Кислотний оксид + луг → сіль + вода.
Луг + кислота → сіль + вода.
Нерозчинна основа + кислота → сіль + вода.
Сіль' + кислота' → сіль" + кислота".
Сіль' + луг → сіль" + основа↓.
*Амфотерний оксид + кислота → сіль + вода.
*Амфотерний оксид + луг → сіль + вода.
*Амфотерний гідроксид + кислота → сіль + вода.
*Амфотерний гідроксид + луг → сіль + вода.
Завдання
До наведених у загальному вигляді записів реакцій обміну доберіть конкретні приклади. Запишіть, користуючись таблицею «Розчинність кислот основ і солей у воді», рівняння реакцій у повній і скороченій йонних формах (завдання* виконувати не обов'язково).
• Значення реакцій сполучення, розкладу, заміщення та обміну важко переоцінити. За допомогою реакцій цих та інших типів людство забезпечує потребу у речовинах, матеріалах і сучасних технологіях розгляньмо кілька прикладів. Приміром, промисловий спосіб добування амоніаку ґрунтується на його синтезі з простих речовин:
N2 + Н2 → NН3
Негашене вапно добувають термічним розкладанням кальцій карбонату головної складової вапняку:
CaCO3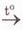 CaO + CO2 CaO + CO2
Один зі способів добування металів - взаємодія їхніх оксидів з алюмінієм:
W03 + Al → W + Аl203
Реакції обміну застосовують для очищення та нейтралізації стічних промислових вод:
NiCl2 + NaOH → Ni(OH)2↓ + NaCl
Завдання
Перетворіть схеми реакцій на хімічні рівняння. Рівняння реакції йонного обміну запишіть у повній і скороченій йонних формах.
Звичайно, класифікація хімічних реакцій на чотири розглянуті типи не є універсальною та всеосяжною. Під час подальшого вивчення хімії, зокрема реакцій за участю органічних сполук, ви розширите й поглибите свої уявлення щодо підходів до класифікації хімічних реакцій за ознакою кількості та складу реагентів і продуктів. Про класифікацію хімічних реакцій за іншими ознаками йтиметься у наступних параграфах.
Стисло про головне
Хімічні реакції класифікують за різними ознаками - кількістю і складом реагентів і продуктів, тепловим ефектом, зміною ступенів окиснення елементів, оборотністю тощо.
За кількістю і складом реагентів і продуктів розрізняють реакції розкладу, сполучення, заміщення, обміну. Аби встановити за цією ознакою приналежність реакції до певного типу, треба проаналізувати її хімічне рівняння.
Реакції розкладу відбуваються за участю одного реагенту з утворенням кількох продуктів:
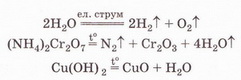
Їхня протилежність - реакції сполучення. У них беруть участь кілька реагентів й утворюється один продукт:
2Mg + 02 = 2MgO
С02 + Н20 = Н2С03
SO2 + Н20 = H2S03
2СО + 02 = 2С02
N2 + 3H2 = 2NH3
СаО + С02 = СаС03
У реакціях заміщення реагенти - проста і складна речовини. Під час реакції атоми простої речовини заміщують атоми одного з хімічних елементів у складній речовині. Продукти - нові проста і складна речовини:
2Аl + 6НСl = 2АlСl3 + ЗН2↑
Сu + 2АgNO3 = Сu(NO3)2 + 2Аg↓
У реакціях обміну реагенти - дві складні речовини. Під час реакції вони обмінюються складовими частинами - утворюються дві нові складні речовини.
СаО + 2HNО3 = Са(NO3)2 + Н20
КОН + НВг = КВг + Н20
РЬ(ОН)2 + 2НNO3 = РЬ(NO3)2 + 2Н20
Nа2S + 2НСl = 2NаСl + Н2S↑
К2S04 + Ва(ОН)2 = 2КОН +ВаS04↓
NіСl2 + 2Na0Н = Ni(ОН)2↓ + 2NаСl
Застосуйте свої знання й уміння
1.Виберіть схему реакції заміщення:
А CО + СІ2 → СОСІ2;
Б СН4 → С + Н2;
В MgO + HNO3 → Mg(N03)2 + Н20;
Г MnO2 + AI → Al2O3 + Mn.
2.Встановіть відповідність між схемами хімічних реакцій та їхніми типами:
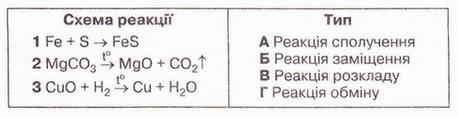
3. а) Виберіть реакцію, яка є різновидом реакції обміну:
А Горіння кальцію; Б Взаємодія хлору з воднем; В Реакція нейтралізації; Г Добування кисню з гідроген пероксиду.
б) Наведіть приклад такої реакції, запишіть її рівняння у повній і скороченій йонних формах.
4. Виберіть реакцію сполучення, у хімічному рівнянні якої сума коефіцієнтів становить 5:
А Прожарювання міді; Б Нагрівання калій перманганату; В Прожарювання ферум(ІІІ) гідроксиду; Г Спалювання сірки.
5.Визначте, про яку реакцію йдеться в уривку літературного твору. Запишіть її хімічне рівняння. Класифікуйте цю реакцію за кількістю та складом реагентів і продуктів.
«Шипить та куриться вапно, що його гасять у великих дощаних скринях» (І. Франка).
6. До складу антацидних (проти печії) лікарських препаратів «Маалокс» і «Алмагель» входять магній гідроксид і алюміній гідроксид. Складіть рівняння реакцій цих сполук із хлоридною кислотою - головною складовою шлун-кового соку. Класифікуйте реакції за кількістю та складом реагентів і продуктів. Запишіть їхні рівняння у повній і скороченій йонній формах. Визначте, які йони у складі шлункового соку є причиною печії.
7. Художнику доручили ілюструвати підручник хімії для дев'ятикласників. Хімічні реакції розкладу, сполучення, заміщення, обміну він зобразив у такий спосіб (мал. 13.6). Оцініть, чи правильно художник змоделював хімічні реакції різних типів. Обґрунтуйте свій експертний висновок.
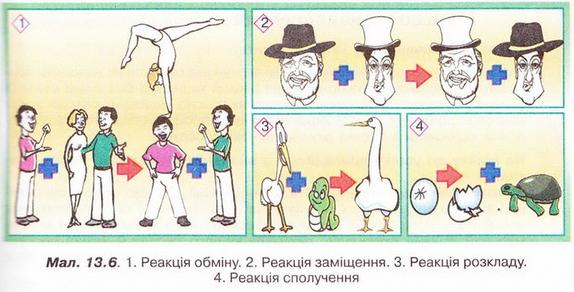
8. Наведіть приклад реакції сполучення, у рівнянні якої сума коефіцієнтів становить 11.
9. Наведіть приклад реакції обміну, у рівнянні якої сума коефіцієнтів становить 12.
10. Наведіть приклад реакції заміщення, у рівнянні якої сума коефіцієнтів становить 7.
11. Використовуючи різноманітні джерела інформації, відшукайте приклади рівнянь хімічних реакцій, які за формальними ознаками не можна віднести до жодного з типів, розглянутих у § 13.
Скарбничка досвіду
Уявіть себе:
• художником, якому доручили ілюструвати підручник хімії для дев'ятикласників. Намалюйте комікси, які зображують хімічні реакції сполучення, розкладу, заміщення, обміну. Якщо вмієте працювати з відповідними комп'ютерними програмами - створіть анімаційний фільм;
• режисером навчального фільму, в якому йдеться про класифікацію хімічних реакцій за кількістю та складом реагентів і продуктів реакції. Жанр фільму - мюзикл. Ролі формульних одиниць речовин можуть виконати ваші однокласники, приятелі, родичі тощо. Вони ж можуть узяти на себе функції художників по костюмах, дизайнерів, відеооператорів, постановників. Напишіть сценарій такого фільму, зніміть його й презентуйте.
Г. А. Лашевська, Хімія, 9 клас
Вислано читачами з інтернет-сайтів
Матеріали з хімії, планування з хімії, завдання та відповіді по класам, плани конспектів уроків з хімії для 9 класу
Зміст уроку
 конспект уроку і опорний каркас конспект уроку і опорний каркас
 презентація уроку презентація уроку
 акселеративні методи та інтерактивні технології акселеративні методи та інтерактивні технології
 закриті вправи (тільки для використання вчителями) закриті вправи (тільки для використання вчителями)
 оцінювання
Практика оцінювання
Практика
 задачі та вправи,самоперевірка задачі та вправи,самоперевірка
 практикуми, лабораторні, кейси практикуми, лабораторні, кейси
 рівень складності задач: звичайний, високий, олімпійський рівень складності задач: звичайний, високий, олімпійський
 домашнє завдання
Ілюстрації домашнє завдання
Ілюстрації
 ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа
 реферати реферати
 фішки для допитливих фішки для допитливих
 шпаргалки шпаргалки
 гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення
 зовнішнє незалежне тестування (ЗНТ) зовнішнє незалежне тестування (ЗНТ)
 підручники основні і допоміжні підручники основні і допоміжні
 тематичні свята, девізи тематичні свята, девізи
 статті статті
 національні особливості національні особливості
 словник термінів словник термінів
 інше
Тільки для вчителів інше
Тільки для вчителів
 ідеальні уроки ідеальні уроки
 календарний план на рік календарний план на рік
 методичні рекомендації методичні рекомендації
 програми програми
 обговорення обговорення
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|