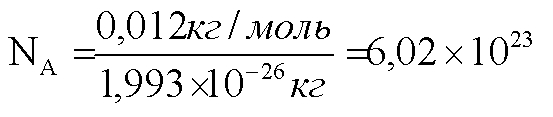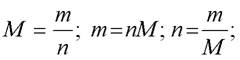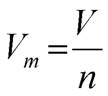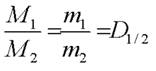Версия 12:49, 6 декабря 2012Гіпермаркет Знань>>Хімія>>Хімія 8 клас. Повні уроки>>Біологія: Узагальнення знань з теми. Повні уроки
Тема
Мета уроку
Задачі уроку
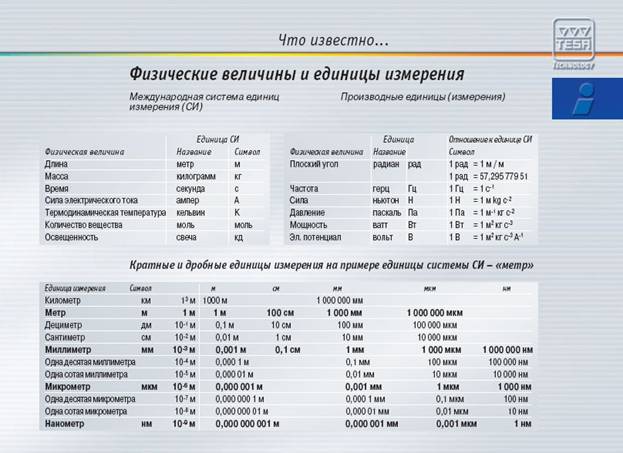
Основні терміниКількість речовини – це кількість однакових частинок у речовині, які характеризують її як певну фізичну величину. Стала Авогадро - число структурних одиниць у молі будь-якої речовини. Молярна маса – маса одного моля даної речовини в грамах. Молярний об’єм газу – це відношення об’єму речовини до кількості цієї речовини. Відносна густина газів - це величина, яка характеризує, у скільки разів більша або нижча за відносну молекулярну маса одного газу відносна молекулярна маса другого газу. Хід урокуПоняття кількості речовини, моль як одиниця кількості речовини, стала АвогадроКількість речовини, як Ви вже вивчили у цій темі – це кількість однакових частинок у речовині, які характеризують її як певну фізичну величину. У Міжнародній системі одиниць (СІ) за одиницю кількості речовини прийнято моль. Мал. 1. Міжнародна система одиниць. Щоб краще зрозуміти механіку міжнародної системи одиниць, пропонуємо вам ознайомитися з наступним відео. Відео 1. Міжнародна система одиниць.
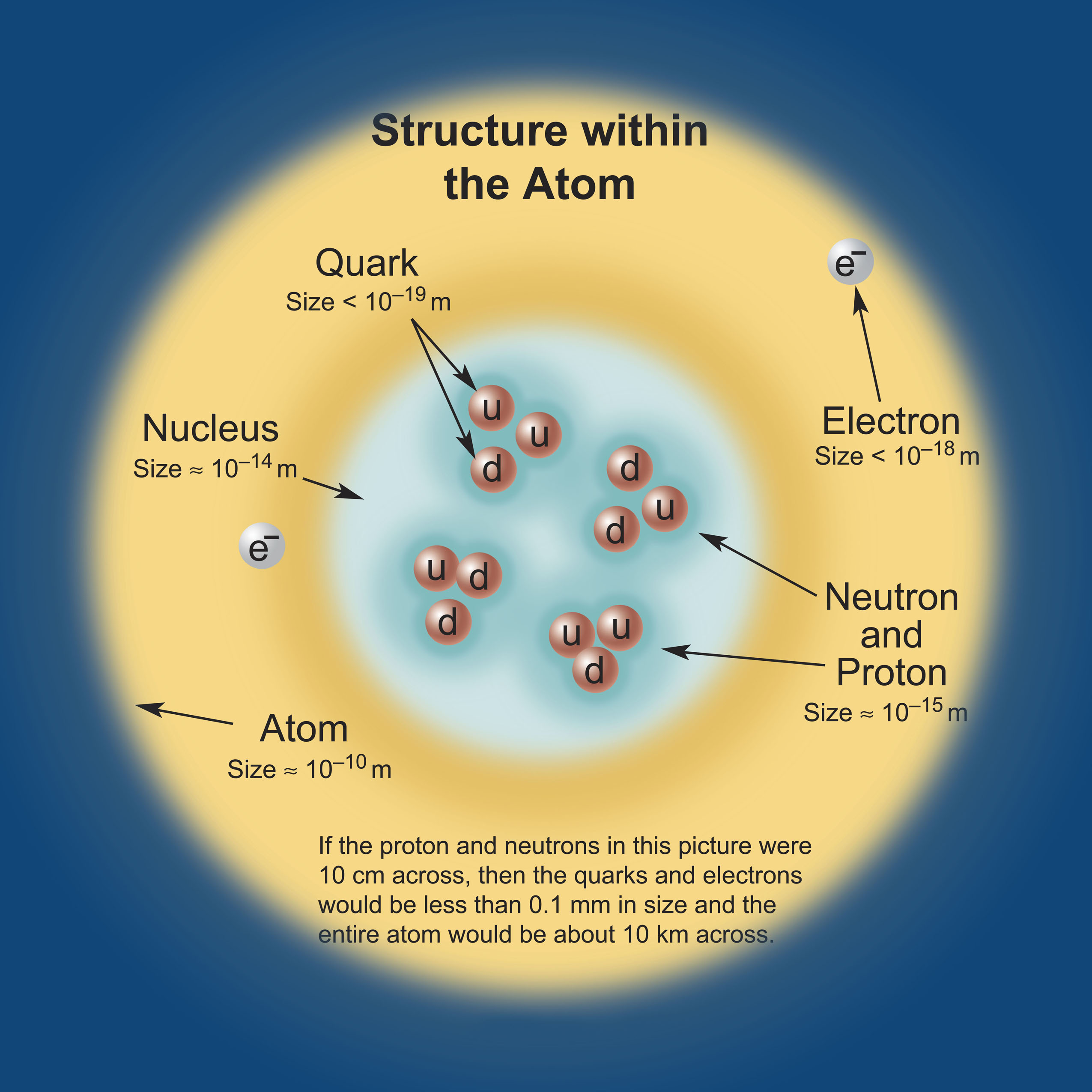
Моль – це та кількість речовини, яка містить стільки структурних одиниць (молекул, атомів, йонів, електронів тощо), скільки атомів міститься у 12 г нукліду Карбону 12С. Мал. 2. Структура атома. Знаючи масу одного атому Карбону (1,993 10-26 кг), можна визначити число атомів NA у 0,012 кг Карбону: Мал.3. Число Авогадро. Це число називається сталою Авогадро (позначається NA, розмірність 1/моль), показує число структурних одиниць у молі будь-якої речовини. Контролюючий блок 1
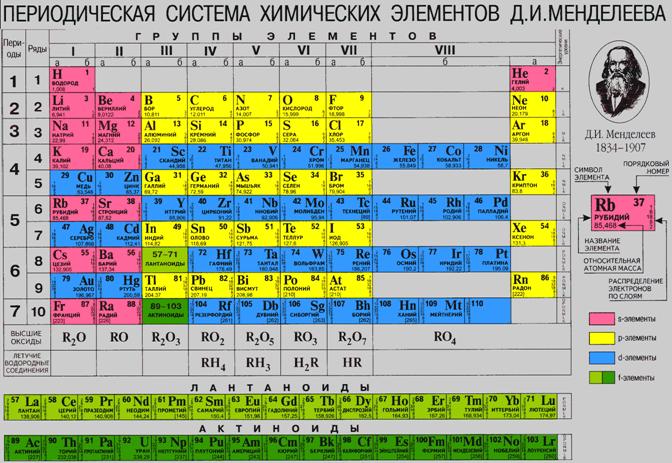
Молярна маса та її обчисленняМолярна маса – маса одного моля даної речовини в грамах. Маса виражається у кілограмах (грамах), кількість речовини – у молях, молярна маса має розмірність кг/моль або г/моль. Існують співвідношення: Де m – маса речовини; n – кількість речовини; М – молярна маса речовини Молярну масу речовини можна легко обчислити, знаючи масу молекули. Так, якщо маса молекули води становить 2,99 10-26 кг, то її молярна маса становить добуток маси молекули на число (сталу) Авогадро, і дорівнює 0,018 кг/Моль, або 18 г/моль. У загальному випадку молярна маса, виражена у г/моль, чисельно дорівнює відносній атомній масі або відносній молекулярній масі цієї речовини. Відносна атомна маса елемента знаходиться у періодичній системі поряд з позначкою потрібного елемента. Мал.4. Періодична система хімічних елементів. Контролюючий блок 2
Закон Авогадро і молярний об’єм та відносна густина газів, їх обчисленняВивчаючи властивості газів, А.Авогадро висунув гіпотезу, яка з часом увійшла у хімію як закон Авогадро: «В рівних об’ємах неоднакових газів при однакових умовах (тиску та температури) існує одна й та сама кількість молекул.» Мал. 5. Амедео Авогадро. Із закону Авогадро випливає важливий наслідок: Можемо спостерігати ці наслідки на наступному відео. Відео 2. Наслідки закону Авогадро.
Молярний об’єм газу – це відношення об’єму речовини до кількості цієї речовини: Де Vm – молярний об’єм газу, м3/моль або л/моль; V – об’єм речовини, л, м3; n – кількість речовини системи, моль. Vmгазу = 22,4 л/моль (н.у.) Із закону Авогадро ми знаємо, що за однакового об’єму газів та при однакових умовах, в них є однаковим число молекул, а отже, і молів газів. А відношення мас заданого об’єму одного газу до ідентичного об’єму іншого (взятого за однакових умов) називають відносною густиною газів за другим (позначається літерою D): Густина газу може спричинювати різноманітні ефекти. Один з них можемо спостерігати на відео. Відео 3. Досліди з сухим льодом.
Контролюючий блок №3
Задачі
Цікаво знати, що…Вуглекислий газ (хімічна назва карбон (IV) оксид) при тискові біля 60 атмосфер перетворюється на рідину. Ця рідина зберігається і транспортується під тиском в стальних балонах. Кожний з вас бачив такі балони у продавців газованої води. Якщо з балона виливати двоокис вуглецю у звичайний мішок, то в ньому утворюватимуться білі, дуже холодні пластівці твердого карбон (IV) оксиду, які нагадують сніг. Ці пластівці, не топлячись, повільно випаровуються. Таке явище, коли тверда речовина перетворюється в газоподібну, минаючи стан рідини, називають возгонкою. Возгонятися можуть багато відомих вам речовин. Так. Наприклад, возгоняється йод, нафталін, бензойна кислота, бромистий кадмій, сулема і багато інших. Перехід твердого карбон (IV) оксиду в газоподібний стан відбувається при низькій (-78) температурі і супроводжується поглиненням тепла. Ці властивості карбон (IV) оксиду в техніці застосовуються для одержання низьких температур. Спресований у кубики твердий карбон (IV) оксид ззовні схожий на лід. Він поволі випаровується, викликаючи значне охолодження (до -78), і не залишає при цьому рідини. Звідси і його технічна назва «сухий лід». «Сухий лід» знайшов широке застосування в холодильній техніці для охолодження харчових продуктів. Кубики «сухого льоду», розміщені серед продуктів, не тільки підтримують низьку температуру, але й створюють атмосферу вуглекислого газу, в якому припиняється розвиток гнильних бактерій та інших шкідників. Твердий карбон (IV) оксид використовується також у пожежній справі. Поводитись з «сухим льодом» треба обережно: брати голими руками його не слід. Список використаної літератури
Дорошенко О.В. Черчик Т.В. Лісняк А. В.
|
|||||||||||||||||||||||||||||
Авторські права | Privacy Policy |FAQ | Партнери | Контакти | Кейс-уроки
© Автор системы образования 7W и Гипермаркета Знаний - Владимир Спиваковский
При использовании материалов ресурса
ссылка на edufuture.biz обязательна (для интернет ресурсов -
гиперссылка).
edufuture.biz 2008-© Все права защищены.
Сайт edufuture.biz является порталом, в котором не предусмотрены темы политики, наркомании, алкоголизма, курения и других "взрослых" тем.
Ждем Ваши замечания и предложения на email: 
По вопросам рекламы и спонсорства пишите на email: