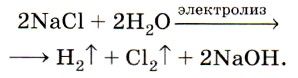|
|
|
| Строка 1: |
Строка 1: |
| | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 9 класс|Химия 9 класс]]>> Химия: Галогены<metakeywords>химия, 9 класс, класс, урок химии, на тему, урок на тему, урок для 9 класса, Галогены</metakeywords>''' | | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 9 класс|Химия 9 класс]]>> Химия: Галогены<metakeywords>химия, 9 класс, класс, урок химии, на тему, урок на тему, урок для 9 класса, Галогены</metakeywords>''' |
| | | | |
| - | <u>''Строение и свойства атомов''</u>. Элементы главной подгруппы VII группы Периодической системы, объединенные под общим названием галогены, фтор P, хлор Сl, бром Вr, иод I, астат Аt (редко встречающийся в природе) — типичные неметаллы. Это и понятно, ведь их атомы содержат на внешнем энергетическом уровне семь электронов, и им недостает лишь одного электрона, чтобы завершить его. Атомы этих элементов при взаимодействии с металлами принимают электрон от атомов металлов. При этом возникает ионная связь и образуются [[Соли,_их_классификация_и_свойства|соли]]. Отсюда общее название «галогены», т. е. «рождающие соли».<br>''<br>Галогены'' — очень сильные окислители. Фтор в химических реакциях проявляет только окислительные свойства, и для него характерна степень окисления -1. Остальные галогены могут проявлять и восстановительные свойства при взаимодействии с более электроотрицательными элементами — фтором, [[Кислород|кислородом]], азотом, при этом степени их окисления могут принимать значения +1, +3, +5, +7. Восстановительные свойства галогенов усиливаются от хлора к иоду, что связано с ростом радиусов их атомов: атомы хлора примерно вдвое меньше, чем у иода.<br><br>''Галогены'' — простые вещества. Все галогены существуют в свободном состоянии в виде двухатомных молекул с ковалент-ной неполярной химической связью между атомами. В твердом состоянии Р2, С12, Вг2,12 имеют молекулярные кристаллические решетки, что и подтверждается их физическими свойствами (табл. 7).
| + | '''Галогены''' |
| | | | |
| - | <br>Физические свойства галогенов Таблица 7 | + | <h2>Общая характеристика</h2> |
| | | | |
| - | [[Image:Ahim09-42.jpg|галогены]]
| + | К галогенам относятся пять основных неметаллических элементов, которые расположены |
| | + | в VII группе таблицы Менделеева. В эту группу входят такие химические элементы, как фтор F, хлор Cl, бром Br, иод I, астат At. |
| | | | |
| - | <br> | + | <br> |
| | + | [[Image:9kl_Galogeny01.jpg|500x500px|галогены]] |
| | + | <br> |
| | + | |
| | + | Свое название галогены получили от греческого слова, которое в переводе обозначает образующий соль или «солеобразующий», так как в принципе большая часть соединений, которые содержат галогены и носят названия солей. |
| | | | |
| - | Как можно заметить, с увеличением молекулярной массы галогенов температуры плавления и кипения повышаются, возрастают плотности: бром — жидкость, иод — твердое вещество, фтор и хлор — газы. Это связано с тем, что с увеличением размеров атомов и молекул галогенов возрастают и силы межмолекулярного взаимодействия между ними.<br><br>От F2 к I2 усиливается интенсивность окраски галогенов.<br><br>Химическая активность галогенов, как [[Неметаллы_(Химия_11_класс)|неметаллов]], от фтора к иоду ослабевает, у кристаллов иода появляется металлический блеск.<br><br>Каждый галоген является самым сильным окислителем в своем периоде. Окислительные свойства галогенов отчетливо проявляются при их взаимодействии с металлами. При этом, как вы уже знаете, образуются соли (отсюда и название подгруппы). Так, фтор уже при обычных условиях реагирует с большинством металлов, а при нагревании и с золотом, серебром, платиной, известными своей химической пассивностью. Алюминий и цинк в атмосфере фтора воспламеняются.
| + | Галогены вступают в реакцию практически со всеми простыми веществами, за исключением только нескольких металлов. Они являются довольно таки энергичными окислителями, имеют очень сильный и резкий запах, прекрасно взаимодействуют с водой, а также имеют большую летучесть и высокую электроотрицательность. А вот в природе их можно встретить лишь в качестве соединений. |
| | | | |
| - | <br> | + | <h2>Физические свойства галогенов</h2> |
| | | | |
| - | Остальные галогены реагируют с металлами в основном при нагревании. Так, в колбе, наполненной хлором, красиво вспыхивают и сгорают кристаллики измельченной сурьмы (рис. 17), образуя при этом смесь двух хлоридов сурьмы(ІІІ) и (V):<br><br>[[Image:Ahim09-43.jpg|химия 9 класс]]
| + | 1. Такие простые химические вещества, как галогены, состоят из двух атомов;<br> |
| | + | 2. Если рассматривать галогены в обычных условиях, то следует знать, что фтор и хлор, находятся в газообразном состоянии, тогда как бром является жидким веществом, а йод и астат относятся к твердым веществам.<br> |
| | | | |
| - | Нагретый порошок [[Железо_(Химия_9_класс)|железа]] также загорается при взаимодействии с хлором. Опыт можно провести, как с сурьмой, но только железные опилки нужно предварительно накалить в железной ложечке, а затем высыпать их небольшими порциями в колбу с хлором. Так как хлор является сильным окислителем, то в результате реакции образуется хлорид железа(ІІІ).
| + | <br> |
| | + | [[Image:9kl_Galogeny02.jpg|500x500px|галогены]] |
| | + | <br> |
| | | | |
| - | <br> | + | 3. У галогенов температура плавления, кипения и плотность повышаются с увеличением атомной массы. Также при этом и меняется их окраска, она становиться более темной.<br> |
| - | | + | 4. При каждом увеличении порядкового номера, уменьшается химическая активность, электроотрицательность и более слабыми становятся неметаллические свойства.<br> |
| - | В парах брома сгорает раскаленная медная проволока:<br>
| + | 5. Галогены обладают способностью образовывать соединения между собой, как например BrCl.<br> |
| | + | 6. Галогены при комнатной температуре могут находиться во всех трех состояниях материи.<br> |
| | + | 7. Так же важно запомнить то, что галогены относятся к довольно таки токсичным химическим веществам.<br> |
| | | | |
| - | [[Image:Ahim09-44.jpg|химия 9 класс]]
| + | <h2>Химические свойства галогенов</h2> |
| | + | |
| | + | При химической реакции с металлами, галогены действуют, как окислители. Если, к примеру, взять фтор, то даже в обычных условиях он дает реакцию с большинством металлов. А вот алюминий и цинк воспламеняется даже в атмосфере: +2-1:ZnF2. |
| | | | |
| | + | <br> |
| | + | [[Image:9kl_Galogeny03.jpg|500x500px|галогены]] |
| | <br> | | <br> |
| | | | |
| - | Реакция сопровождается выделением фиолетовых паров иода (почему?).<br><br>Об уменьшении окислительных и увеличении восстановительных свойств галогенов от фтора к иоду можно судить и по их способности вытеснять друг друга из растворов солей.<br><br>Так, хлор вытесняет бром и иод из растворов их солей.
| + | <h2>Получение галогенов</h2> |
| | | | |
| - | <br>
| + | При получении фтора и хлора в масштабах промышленности используют электролиз или растворы солей. |
| | | | |
| - | Свободный бром вытесняет иод из солей:<br>[[Image:Ahim09-45.jpg|химия 9 класс]]
| + | Если вы внимательно рассмотрите рисунок, изображенный внизу, то увидите, как в лабораторных условиях с помощью установки для электролиза можно получить хлор: |
| | | | |
| | + | <br> |
| | + | [[Image:9kl_Galogeny04.jpg|500x500px|галогены]] |
| | <br> | | <br> |
| | | | |
| - | Для фтора эта реакция не характерна, так как она протекает в растворе, а фтор взаимодействует с водой, вытесняя из нее кислород.
| + | На первом рисунке изображена установка для расплава хлорида натрия, а на втором уже для получения раствора хлорида натрия. |
| | | | |
| | + | Такой процесс электролиза расплава хлорида натрия можно представить в виде даного уравнения: |
| | + | |
| | + | <br> |
| | + | [[Image:9kl_Galogeny05.jpg|500x500px|галогены]] |
| | <br> | | <br> |
| | | | |
| - | Здесь кислород выступает в непривычной для себя роли восстановителя, это единственный, пожалуй, случай, когда кислород является не одним из исходных веществ, а продуктом горения.<br><br>Ослабление окислительных свойств галогенов от фтора к иоду наглядно проявляется при взаимодействии их с водородом. Уравнение этой реакции можно записать в общем виде так:<br><br>Н2 + Г2 = 2НГ<br><br>(Г — условное химическое обозначение галогенов).<br><br>Если фтор взаимодействует с водородом в любых условиях со взрывом, то смесь хлора с водородом реагирует со взрывом только при поджигании или облучении прямым солнечным светом, бром взаимодействует с водородом при нагревании и без взрыва. Эти реакции экзотермические. Реакция же соединения иода с [[Квантовые_постулаты_Бора._Модель_атома_водорода_по_Бору|водородом]] слабо эндотермическая, она протекает медленно даже при нагревании.<br><br>В результате этих реакций образуются соответственно фтороводород НF, хлороводород НСl, бромоводород НВr и иодово-дород НI.<br><br><u>''Открытие галогенов.''</u>Фтор в свободном виде получил впервые в 1866 г. французский химик Анри Муассан, который был удостоен за это Нобелевской премии. Свое название элемент получил от греч. фторос — разрушающий.<br><br>Хлор открыт шведским химиком К. Шееле в 1774 г. Элемент получил название за свой цвет (греч. хлорос — желто-зеленый).<br>
| + | При помощи такого электролиза, кроме получения хлора еще образуются также водород и гидроксид натрия: |
| | | | |
| - | ''Карл Вильгельм Шееле''
| + | <br> |
| | + | [[Image:9kl_Galogeny06.jpg|500x500px|галогены]] |
| | + | <br> |
| | + | |
| | + | Конечно же, водород получают более простым и дешевым способом, чего не скажешь об гидроксиде натрия. Его, так же, как и хлор получают практически всегда только с помощью электролиза раствора поваренной соли. |
| | | | |
| - | (1742-1786)
| + | <br> |
| | + | [[Image:9kl_Galogeny07.jpg|500x500px|галогены]] |
| | + | <br> |
| | + | |
| | + | Если вы рассмотрите рисунок, изображенный вверху, то увидите, как лабораторным способом можно получить хлор. А получают его с помощью взаимодействия соляной кислоты с оксидом марганца: |
| | | | |
| - | [[Image:Ahim09-46.jpg|Карл Вильгельм Шееле]] | + | <br> |
| | + | [[Image:9kl_Galogeny08.jpg|500x500px|галогены]] |
| | + | <br> |
| | + | |
| | + | В промышленности бром и йод получают с помощью реакции вытеснения этих веществ хлором из бромидов и йодидов. |
| | | | |
| - | <br> | + | <h2>Применение галогенов</h2> |
| | | | |
| - | Шведский химик. В 1772 г. установил, что воздух состоит из кислорода и азота. Открыл и получил много неорганических и ор-; ганических веществ (кислород, хлор, фторо-водородную кислоту, глицерин и др.).
| + | Фтор или правильнее будет назвать фторид меди (CuF2) имеет довольно таки широкое применение. Его используют при изготовлении керамики, эмалей и различных глазурей. |
| | + | Имеющая в каждом доме тефлоновая сковородка и хладагент в холодильниках и кондиционере, также появились благодаря фтору. |
| | | | |
| - | <br>Бром открыт в 1826 г. французским химиком А. Баларом. Элемент назван так за свой запах (греч. бромос — зловонный).<br><br>Иод получен в 1811 г. французским ученым Б. Куртуа, а название получил за цвет своих паров (греч. иодэс — фиолетовый).<br><br>1. Строение атомов галогенов и их степени окисления.
| + | Кроме бытовых нужд тефлон также используют в медицинских целях, так как его применяют при производстве имплантатов. Фтор необходим при изготовлении лизн в оптике и в зубных пастах. |
| | | | |
| - | 2. Физические свойства галогенов.
| + | Хлор также в нашей жизни встречается буквально на каждом шагу. Самым массовым и распространенным применением хлора, является, конечно же, поваренная соль NaCl. Она так же выступает в роли дезинтоксикационного средства и используется в борьбе с гололедом. |
| | | | |
| - | 3. Химические свойства галогенов: взаимодействие с металлами, водородом, растворами солей.
| + | Кроме этого, хлор незаменим в производстве пластика, синтетического каучука и поливинилхлорида, благодаря которым мы получаем одежду, обувь и другие, нужные в нашей повседневной жизни вещи. Его используют при производстве отбеливателей, порошков, красителей, а также другой бытовой химии. |
| | | | |
| - | 4. Изменение окислительно-восстановительных свойств галогенов от фтора к иоду.<br><br>Рассчитайте, какую массу будет иметь 1 л фтора и хлора при н. у. Найдите их относительную плотность по водороду и воздуху.<br><br>Растворы хлора, брома и иода в воде соответственно называются хлорной, бромной и йодной водой. Почему нет фторной воды?<br><br>Проведите аналогию между реакциями щелочных металлов и галогенов с растворами солей.<br><br>Рассчитайте степени окисления атомов химических элементов в следующих соединениях: КСlO3 (бертолетова соль), НСlO (хлорноватистая кислота), НСlO4 (хлорная кислота). Напишите формулы оксидов, соответствующих кислотам.<br>
| + | Бром, как правило, необходим, как светочувствительное вещество при печатании фотографий. В медицине он применяется, как успокаивающее средство. Также бром используют при производстве инсектицидов и пестицидов и т.д. |
| | | | |
| - | Укажите, изменением каких условий можно сместить химическое равновесие процесса вправо:<br><br>H2 + I2 (гaз) <-> 2HI + Q<br><br>Рассмотрите зависимость скорости химической реакции от природы реагирующих веществ на примере взаимодействия галогенов с водородом.<br><br>Какой объем хлора (н. у.) потребуется для вытеснения всего иода из 300 г 15%-ного раствора иодида калия? Какое количество новой соли при этом образуется?<br><br>Какой объем хлороводорода образуется при взаимодействии 150 л хлора с 200 л водорода? Какой газ взят в избытке? Какой объем займет избыток этого [[Давление_газа|газа]]?<br><br>Во многих странах фтор носит другое название — флюор, что в переводе с лат. означает «текучий». Найдите объяснение этому названию, используя химические словари и другую [[Литература|литературу]].<br>
| + | Ну, а всем известный йод, который имеется в аптечке у каждого человека, в первую очередь используется, как антисептик. Кроме своих антисептических свойств, йод присутствует в источниках света, а также является помощником для обнаружения отпечатков пальцев на бумажной поверхности. |
| | | | |
| - | <sub>анекдоты к уроку [[Химия 9 класс|химии 9 класса]], практикум к [[Химия|уроку химии]], всё [[Гипермаркет знаний - первый в мире!|для учеников]] для подготовки домашнего задания </sub> | + | <h2>Роль галогенов и их соединений для организма человека</h2> |
| | | | |
| - | '''<u>Содержание урока</u>'''
| + | Выбирая в магазине зубную пасту, наверное, каждый из вас обращал внимание на то, что на ее этикетке указывается содержание соединений фтора. И это неспроста, так как этот компонент участвует в построении зубной эмали и костей, повышает устойчивость зубов к кариесу. Также он играет важную роль в процессах обмена веществ, участвует в построении скелета костей и предупреждает появление такого опасного заболевания, как остеопороз. |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] конспект урока '''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] опорный каркас
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] презентация урока
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] акселеративные методы
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] интерактивные технологии
| + | |
| - |
| + | |
| - | '''<u>Практика</u>'''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] задачи и упражнения
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] самопроверка
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] практикумы, тренинги, кейсы, квесты
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] домашние задания
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] дискуссионные вопросы
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] риторические вопросы от учеников
| + | |
| - |
| + | |
| - | '''<u>Иллюстрации</u>'''
| + | |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] аудио-, видеоклипы и мультимедиа '''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фотографии, картинки
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] графики, таблицы, схемы
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] юмор, анекдоты, приколы, комиксы
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] притчи, поговорки, кроссворды, цитаты
| + | |
| - |
| + | |
| - | '''<u>Дополнения</u>'''
| + | |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] рефераты'''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] статьи
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фишки для любознательных
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] шпаргалки
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] учебники основные и дополнительные
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] словарь терминов
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] прочие
| + | |
| - | '''<u></u>'''
| + | |
| - | <u>Совершенствование учебников и уроков
| + | |
| - | </u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] исправление ошибок в учебнике'''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обновление фрагмента в учебнике
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] элементы новаторства на уроке
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] замена устаревших знаний новыми
| + | |
| - |
| + | |
| - | '''<u>Только для учителей</u>'''
| + | |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] идеальные уроки '''
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] календарный план на год
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] методические рекомендации
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] программы
| + | |
| - | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обсуждения
| + | |
| - |
| + | |
| - |
| + | |
| - | '''<u>Интегрированные уроки</u>'''<u>
| + | |
| - | </u>
| + | |
| | | | |
| - | <br>
| + | Важная роль в организме человека отведена и хлору, так как он принимает активное участие в сохранении водно-солевого баланса и поддерживание осмотического давления. Хлор участвует в обмене веществ человеческого организма, построении тканей, ну и что тоже немаловажно – в избавление от лишнего веса. Соляная кислота, находящаяся в составе желудочного сока большое значение имеет для пищеварения, так как без нее невозможен процесс переваривания пищи. |
| | + | |
| | + | Хлор необходим нашему организму и должен ежедневно в необходимых дозах поступать в него. Но если, же его норму поступления в организм превысить или резко снизить, то мы |
| | + | сразу же это ощутим в виде отеков, головных болей и других неприятных симптомов, которые способны не только нарушить обмен веществ, но и вызвать заболевания кишечника. |
| | + | |
| | + | У человека в мозге, почках, крови и печени присутствует небольшое количество брома. В медицинских целях бром применяют, как успокоительное средство. Но при его передозировке могут быть неблагоприятные последствия, которые могут привести к угнетенному состоянию нервной системы, а в некоторых случаях и к психическим расстройствам. А недостаток брома в организме ведет к дисбалансу между процессами возбуждения и торможения. |
| | | | |
| - | Если у вас есть исправления или предложения к данному уроку, [http://xvatit.com/index.php?do=feedback напишите нам].
| + | Без йода наша щитовидная железа не может обходиться, так как он способен убивать микробы, поступающие в наше тело. При дефиците йода в организме человека может начаться заболевание щитовидной железы, под названием зоб. При этом заболевании появляются довольно неприятные симптомы. Человек, у которого появился зоб, чувствует слабость, сонливость, повышение температуры, раздражительность и упадок сил. |
| | | | |
| - | Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - [http://xvatit.com/forum/ Образовательный форум].
| + | Из всего этого можно сделать вывод, что без галогенов человек мог бы не только лишиться многих необходимых в повседневной жизни вещей, но без них и не смог бы нормально функционировать наш организм. |
Версия 08:50, 31 июля 2015
Гипермаркет знаний>>Химия>>Химия 9 класс>> Химия: Галогены
Галогены
Общая характеристика
К галогенам относятся пять основных неметаллических элементов, которые расположены
в VII группе таблицы Менделеева. В эту группу входят такие химические элементы, как фтор F, хлор Cl, бром Br, иод I, астат At.

Свое название галогены получили от греческого слова, которое в переводе обозначает образующий соль или «солеобразующий», так как в принципе большая часть соединений, которые содержат галогены и носят названия солей.
Галогены вступают в реакцию практически со всеми простыми веществами, за исключением только нескольких металлов. Они являются довольно таки энергичными окислителями, имеют очень сильный и резкий запах, прекрасно взаимодействуют с водой, а также имеют большую летучесть и высокую электроотрицательность. А вот в природе их можно встретить лишь в качестве соединений.
Физические свойства галогенов
1. Такие простые химические вещества, как галогены, состоят из двух атомов;
2. Если рассматривать галогены в обычных условиях, то следует знать, что фтор и хлор, находятся в газообразном состоянии, тогда как бром является жидким веществом, а йод и астат относятся к твердым веществам.
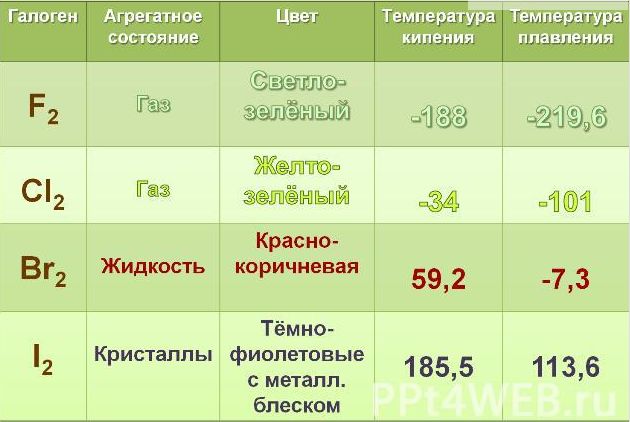
3. У галогенов температура плавления, кипения и плотность повышаются с увеличением атомной массы. Также при этом и меняется их окраска, она становиться более темной.
4. При каждом увеличении порядкового номера, уменьшается химическая активность, электроотрицательность и более слабыми становятся неметаллические свойства.
5. Галогены обладают способностью образовывать соединения между собой, как например BrCl.
6. Галогены при комнатной температуре могут находиться во всех трех состояниях материи.
7. Так же важно запомнить то, что галогены относятся к довольно таки токсичным химическим веществам.
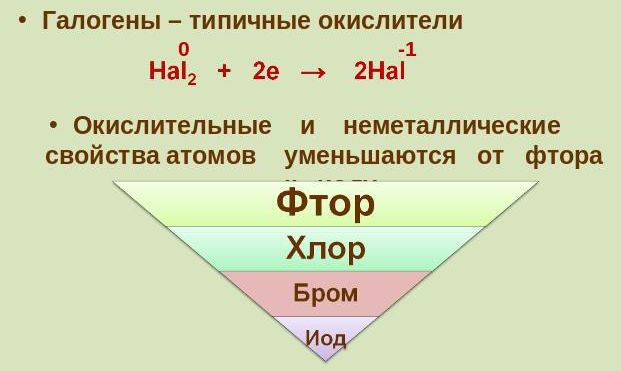
Химические свойства галогенов
При химической реакции с металлами, галогены действуют, как окислители. Если, к примеру, взять фтор, то даже в обычных условиях он дает реакцию с большинством металлов. А вот алюминий и цинк воспламеняется даже в атмосфере: +2-1:ZnF2.
Получение галогенов
При получении фтора и хлора в масштабах промышленности используют электролиз или растворы солей.
Если вы внимательно рассмотрите рисунок, изображенный внизу, то увидите, как в лабораторных условиях с помощью установки для электролиза можно получить хлор:
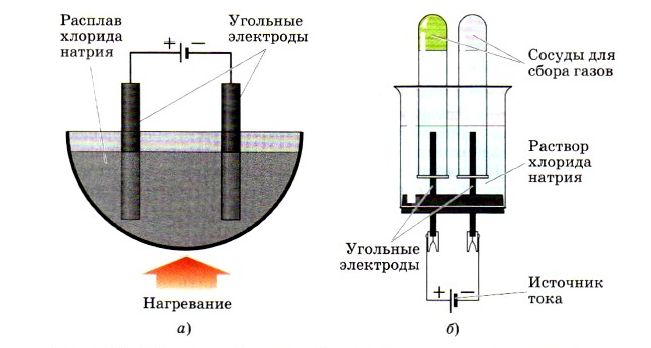
На первом рисунке изображена установка для расплава хлорида натрия, а на втором уже для получения раствора хлорида натрия.
Такой процесс электролиза расплава хлорида натрия можно представить в виде даного уравнения:
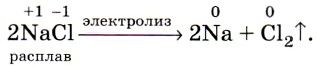
При помощи такого электролиза, кроме получения хлора еще образуются также водород и гидроксид натрия:
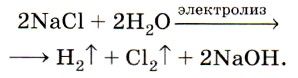
Конечно же, водород получают более простым и дешевым способом, чего не скажешь об гидроксиде натрия. Его, так же, как и хлор получают практически всегда только с помощью электролиза раствора поваренной соли.
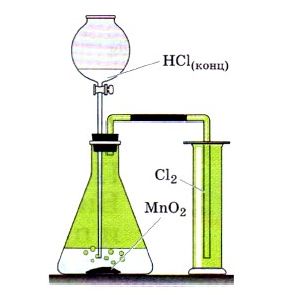
Если вы рассмотрите рисунок, изображенный вверху, то увидите, как лабораторным способом можно получить хлор. А получают его с помощью взаимодействия соляной кислоты с оксидом марганца:
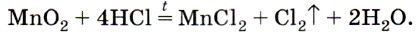
В промышленности бром и йод получают с помощью реакции вытеснения этих веществ хлором из бромидов и йодидов.
Применение галогенов
Фтор или правильнее будет назвать фторид меди (CuF2) имеет довольно таки широкое применение. Его используют при изготовлении керамики, эмалей и различных глазурей.
Имеющая в каждом доме тефлоновая сковородка и хладагент в холодильниках и кондиционере, также появились благодаря фтору.
Кроме бытовых нужд тефлон также используют в медицинских целях, так как его применяют при производстве имплантатов. Фтор необходим при изготовлении лизн в оптике и в зубных пастах.
Хлор также в нашей жизни встречается буквально на каждом шагу. Самым массовым и распространенным применением хлора, является, конечно же, поваренная соль NaCl. Она так же выступает в роли дезинтоксикационного средства и используется в борьбе с гололедом.
Кроме этого, хлор незаменим в производстве пластика, синтетического каучука и поливинилхлорида, благодаря которым мы получаем одежду, обувь и другие, нужные в нашей повседневной жизни вещи. Его используют при производстве отбеливателей, порошков, красителей, а также другой бытовой химии.
Бром, как правило, необходим, как светочувствительное вещество при печатании фотографий. В медицине он применяется, как успокаивающее средство. Также бром используют при производстве инсектицидов и пестицидов и т.д.
Ну, а всем известный йод, который имеется в аптечке у каждого человека, в первую очередь используется, как антисептик. Кроме своих антисептических свойств, йод присутствует в источниках света, а также является помощником для обнаружения отпечатков пальцев на бумажной поверхности.
Роль галогенов и их соединений для организма человека
Выбирая в магазине зубную пасту, наверное, каждый из вас обращал внимание на то, что на ее этикетке указывается содержание соединений фтора. И это неспроста, так как этот компонент участвует в построении зубной эмали и костей, повышает устойчивость зубов к кариесу. Также он играет важную роль в процессах обмена веществ, участвует в построении скелета костей и предупреждает появление такого опасного заболевания, как остеопороз.
Важная роль в организме человека отведена и хлору, так как он принимает активное участие в сохранении водно-солевого баланса и поддерживание осмотического давления. Хлор участвует в обмене веществ человеческого организма, построении тканей, ну и что тоже немаловажно – в избавление от лишнего веса. Соляная кислота, находящаяся в составе желудочного сока большое значение имеет для пищеварения, так как без нее невозможен процесс переваривания пищи.
Хлор необходим нашему организму и должен ежедневно в необходимых дозах поступать в него. Но если, же его норму поступления в организм превысить или резко снизить, то мы
сразу же это ощутим в виде отеков, головных болей и других неприятных симптомов, которые способны не только нарушить обмен веществ, но и вызвать заболевания кишечника.
У человека в мозге, почках, крови и печени присутствует небольшое количество брома. В медицинских целях бром применяют, как успокоительное средство. Но при его передозировке могут быть неблагоприятные последствия, которые могут привести к угнетенному состоянию нервной системы, а в некоторых случаях и к психическим расстройствам. А недостаток брома в организме ведет к дисбалансу между процессами возбуждения и торможения.
Без йода наша щитовидная железа не может обходиться, так как он способен убивать микробы, поступающие в наше тело. При дефиците йода в организме человека может начаться заболевание щитовидной железы, под названием зоб. При этом заболевании появляются довольно неприятные симптомы. Человек, у которого появился зоб, чувствует слабость, сонливость, повышение температуры, раздражительность и упадок сил.
Из всего этого можно сделать вывод, что без галогенов человек мог бы не только лишиться многих необходимых в повседневной жизни вещей, но без них и не смог бы нормально функционировать наш организм.
|