|
|
|
| Строка 1: |
Строка 1: |
| - | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 8 клас|Химия 8 класс]]>> Химия: Основания, их классификация и свойства<metakeywords>химия, 8 класс, класс, урок химии, на тему, урок на тему, урок для 8 класса, Основания, их классификация и свойства, свойства оснований</metakeywords>''' | + | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 8 клас|Химия 8 класс]]>> Химия: Основания, их классификация и свойства<metakeywords>химия, 8 класс, класс, урок химии, на тему, урок на тему, урок для 8 класса, Основания, их классификация и свойства, свойства оснований</metakeywords>''' Все основания, кроме раствора аммиака в воде, представляют собой твердые вещества, имеющие различную окраску. Например, гидроксид кальция Са(ОН)2 белого цвета, гидроксид меди (II) Сu(ОН)2 голубого цвета, гидроксид никеля (II) Ni(OH)2 зеленого цвета, гидроксид железа (III) Fе(ОН)3 красно-бурого цвета и т. д. |
| - | Все основания, кроме раствора аммиака в воде, представляют собой твердые вещества, имеющие различную окраску. Например, гидроксид кальция Са(ОН)2 белого цвета, гидрокснд меди (II) Сu(ОН)2 голубого цвета, гидроксид никеля (II) Ni(OH)2 зеленого цвета, гидроксид железа (III) Fе(ОН)3 красно-бурого цвета и т. д. | + | |
| | | | |
| - | <br>Водный раствор аммиака NH3 * H2O в отличие от других ос-иований содержит не катионы металла, а сложный однозарядный катион аммония NH4 и существует только в растворе (этот раствор вам известен под названием нашатырного спирта). Он легко разлагается на аммиак и воду:<br>[[Image:him8-132.jpg]] | + | <br>Водный раствор аммиака NH3 * H2O в отличие от других оснований содержит не катионы металла, а сложный однозарядный катион аммония NH4 и существует только в растворе (этот раствор вам известен под названием нашатырного спирта). Он легко разлагается на аммиак и воду:<br>[[Image:Him8-132.jpg]] |
| | | | |
| | + | <br> |
| | | | |
| | + | Разделение оснований на группы по различным признакам представлено в таблице 11. |
| | | | |
| - | Разделение оснований на группы по различным признакам представлено в таблице 11.
| + | <br> |
| | | | |
| | + | [[Image:Him8-133.jpg]] |
| | | | |
| | + | <br> |
| | | | |
| - | [[Image:him8-133.jpg]]
| + | Все основания, и в первую очередь щелочи (сильные электролиты), образуют при диссоциации гидроксид-ионы ОН-, которые и обусловливают ряд общих свойств: мылкость на ощупь, изменение окраски индикаторов (лакмуса, метилового оранжевого и фенолфталеина), взаимодействие с другими веществами. |
| | | | |
| | + | <br> |
| | | | |
| | + | <u>''Типичные реакции оснований''</u> |
| | | | |
| - | Все основания, и в первую очередь щелочи (сильные электролиты), образуют при диссоциации гидроксид-ионы ОН-, которые и обусловливают ряд общих свойств: мылкость на ощупь, изменение окраски индикаторов (лакмуса, метилового оранжевого и фенолфталеина), взаимодействие с другими веществами.
| + | [[Image:Him8-134.jpg]] |
| | | | |
| | + | <br> |
| | | | |
| | + | Нерастворимые основания разлагаются при нагревании на оксид металла и воду, что нехарактерно для щелочей, например: |
| | | | |
| - | <u>''Типичные реакции оснований''</u>
| + | Fe(OH)2 = FeO + H2O |
| - | | + | |
| - | [[Image:him8-134.jpg]]
| + | |
| - | | + | |
| - | | + | |
| - | | + | |
| - | Нерастворимые основания разлагаются при нагревании на оксид металла и воду, что нехарактерно для щелочей, например:
| + | |
| - | | + | |
| - | Fe(OH)2 = FeO + H2O | + | |
| - | | + | |
| | | | |
| | + | <br> |
| | | | |
| | 1. Классификация оснований. | | 1. Классификация оснований. |
| Строка 36: |
Строка 35: |
| | 3. Типичное свойство нерастворимых оснований: разложение при нагревании. | | 3. Типичное свойство нерастворимых оснований: разложение при нагревании. |
| | | | |
| - | 4. Условия протекания типичных реакций оснований. | + | 4. Условия протекания типичных реакций оснований. |
| - | | + | |
| - | <br>Какое основание является сильным: а) NH40H; б) Си(0Н)2; в) КОН?
| + | |
| - | | + | |
| - | <br>Дайте характеристику гидроксида бария, используя различные признаки классификации оснований.
| + | |
| | | | |
| - | <br>Закончите молекулярные уравнения возможных химических реакций, запишите соответствующие им ионные уравнения:<br>[[Image:him8-135.jpg]] | + | <br>Какое основание является сильным: а) NH40H; б) Си(0Н)2; в) КОН? |
| | | | |
| | + | <br>Дайте характеристику гидроксида бария, используя различные признаки классификации оснований. |
| | | | |
| | + | <br>Закончите молекулярные уравнения возможных химических реакций, запишите соответствующие им ионные уравнения:<br>[[Image:Him8-135.jpg]] |
| | | | |
| - | Если реакция не будет протекать, укажите причину этого.
| + | <br> |
| | | | |
| | + | Если реакция не будет протекать, укажите причину этого. |
| | | | |
| | + | <br> |
| | | | |
| - | Какой объем аммиаки (н. у.) выделится при взаимодействии 890 г нитрита аммония, содержащего 20% примесей, с раствором гидроксида натрия? Сколько граммов 80%-го раствора щелочи потребуется для реакции? | + | Какой объем аммиаки (н. у.) выделится при взаимодействии 890 г нитрита аммония, содержащего 20% примесей, с раствором гидроксида натрия? Сколько граммов 80%-го раствора щелочи потребуется для реакции? |
| | | | |
| - | <br>Запишите формулы оксидов, которые будут соответствовать следующим гидроксидам: Си(0Н)2; СиОН; Fе(ОН)3,: Fе(0Н)2; NаОН.<br> | + | <br>Запишите формулы оксидов, которые будут соответствовать следующим гидроксидам: Си(0Н)2; СиОН; Fе(ОН)3,: Fе(0Н)2; NаОН.<br> |
| | | | |
| - | <br> <sub>элементы новаторства [[Гипермаркет_знаний_-_первый_в_мире!|на уроке]], статьи [[Химия|по химии]], дополнения к уроку [[Химия_8_класс|химии 8 класса]]</sub> | + | <br> <sub>элементы новаторства [[Гипермаркет знаний - первый в мире!|на уроке]], статьи [[Химия|по химии]], дополнения к уроку [[Химия 8 класс|химии 8 класса]]</sub> |
| | | | |
| | '''<u>Содержание урока</u>''' | | '''<u>Содержание урока</u>''' |
Версия 08:36, 15 июня 2010
Гипермаркет знаний>>Химия>>Химия 8 класс>> Химия: Основания, их классификация и свойства Все основания, кроме раствора аммиака в воде, представляют собой твердые вещества, имеющие различную окраску. Например, гидроксид кальция Са(ОН)2 белого цвета, гидроксид меди (II) Сu(ОН)2 голубого цвета, гидроксид никеля (II) Ni(OH)2 зеленого цвета, гидроксид железа (III) Fе(ОН)3 красно-бурого цвета и т. д.
Водный раствор аммиака NH3 * H2O в отличие от других оснований содержит не катионы металла, а сложный однозарядный катион аммония NH4 и существует только в растворе (этот раствор вам известен под названием нашатырного спирта). Он легко разлагается на аммиак и воду:
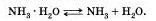
Разделение оснований на группы по различным признакам представлено в таблице 11.
Все основания, и в первую очередь щелочи (сильные электролиты), образуют при диссоциации гидроксид-ионы ОН-, которые и обусловливают ряд общих свойств: мылкость на ощупь, изменение окраски индикаторов (лакмуса, метилового оранжевого и фенолфталеина), взаимодействие с другими веществами.
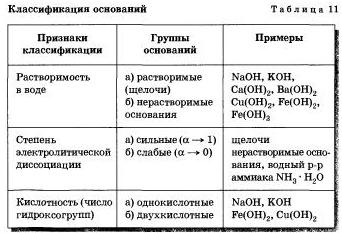
Типичные реакции оснований

Нерастворимые основания разлагаются при нагревании на оксид металла и воду, что нехарактерно для щелочей, например:
Fe(OH)2 = FeO + H2O
1. Классификация оснований.
2. Типичные свойства основании: взаимодействие их с кислотами, оксидами неметаллов, солями.
3. Типичное свойство нерастворимых оснований: разложение при нагревании.
4. Условия протекания типичных реакций оснований.
Какое основание является сильным: а) NH40H; б) Си(0Н)2; в) КОН?
Дайте характеристику гидроксида бария, используя различные признаки классификации оснований.
Закончите молекулярные уравнения возможных химических реакций, запишите соответствующие им ионные уравнения:
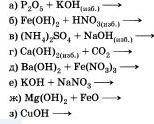
Если реакция не будет протекать, укажите причину этого.
Какой объем аммиаки (н. у.) выделится при взаимодействии 890 г нитрита аммония, содержащего 20% примесей, с раствором гидроксида натрия? Сколько граммов 80%-го раствора щелочи потребуется для реакции?
Запишите формулы оксидов, которые будут соответствовать следующим гидроксидам: Си(0Н)2; СиОН; Fе(ОН)3,: Fе(0Н)2; NаОН.
элементы новаторства на уроке, статьи по химии, дополнения к уроку химии 8 класса
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|













