|
Гіпермаркет Знань>>Хімія>>Хімія 8 клас>>Хімія: Оксиди, їх склад, назви
Тобі треба
знати: назви і визначення оксидів; їх поширеність у природі й застосування; значення води;
описувати: колообіг води в природі;
вміти: наводити приклади оксидів; складати формули оксидів за валентністю; називати оксиди за їх формулами.
Склад і назви оксидів. Ти вже знаєш, що метали і неметали з киснем утворюють оксиди.
• Наведи один-два приклади рівнянь реакцій між:
а) металом і киснем;
б) неметалом і киснем.
Отже, внаслідок взаємодії багатьох простих речовин з киснем утворюються оксиди металів і оксиди неметалів.
Оксиди — це складні речовини, утворені двома елементами, одним з яких є Оксиген з валентністю 2.
За складом оксиди поділяються на оксиди металів і оксиди неметалів
Не кожна сполука хімічного елемента з Оксигеном є оксидом. Наприклад, гідроген пероксид H2O2, оксиген дифлуорид OF2 до оксидів не належать. Про причини цього ти дізнаєшся в наступних класах.
Назви оксидів складаються з назви елемента та слова «оксид». Якщо елемент утворює кілька оксидів, то після назви елемента в дужках римською цифрою зазначають його валентність: CuO — купрум(ІІ) оксид, Сu2O — купрум(І) оксид.
Сталу валентність у назві оксиду не зазначають. Наприклад, Na2O — натрій оксид, Аl2O3 — алюміній оксид. Вживаються також назви, в яких акцентується увага на кількості атомів Оксигену, що припадає на один атом іншого елемента: SO2 — сульфур діоксид, SO3 — сульфур триоксид. Для окремих оксидів як синоніми зберігаються назви, що склалися історично і поширені в народній мові. Деякі з таких назв наведено в табл. 1.
Таблиця 1. Назви оксидів

За стандартних умов оксиди можуть перебувати в різних агрегатних станах.
Стандартні умови — це фізичні умови, що визначаються тиском 100 кПа (1 атм) і температурою 298 К (25 °С).
• Наведи приклади оксидів, які являють собою: а) тверді речовини; б) рідини; в) гази. Запиши їх формули і зазнач назви.
Поширення у природі. Оксиди багатьох елементів дуже поширені в природі. Як ти гадаєш, чому? Наприклад, така добре відома сполука, як звичайний
річковий пісок (з деякими домішками) є оксидом з формулою SiO2 — силіцій(IV) оксид (кремнезем). Майже чистим кремнеземом є гірський кришталь. Цей оксид разом з алюміній оксидом Аl2O3 входить до складу глин та багатьох інших мінералів. З руд, які містять алюміній оксид Аl2O3, виплавляють алюміній. Звичайний наждак — це також алюміній оксид з домішками. Алюміній оксид з невеликим вмістом різних домішок може бути і коштовним каменем (рубін, сапфір).
Дуже поширені в природі й оксиди Феруму — це різні залізні руди. Україна має великі запаси залізних руд (Криворізьке та Керченське родовища). До складу повітря входить карбон(IV) оксид СO2 (вуглекислий газ), об'ємна частка якого в повітрі становить 0,3 %. Однак найпоширенішим оксидом у природі є гідроген оксид Н20 (вода).
Вода — природний оксид. Вода — це найдивовижніша, найпоширеніша і най-необхідніша речовина на нашій планеті. Три чверті земної поверхні вкрито водою, вона утворює океани, моря, ріки й озера. У вигляді великих мас снігу і криги лежить вода цілорічно на вершинах високих гір і в полярних країнах. У надрах Землі також є вода, що просочує ґрунт і гірські породи. Воді належить найважливіша роль у геологічній історії нашої планети.
Вода впливає на клімат, оскільки має велику теплоємність. Нагріваючись, вона поглинає теплоту, а охолоджуючись, віддає її і тим самим «вирівнює» клімат. Багато води перебуває у газуватому стані в атмосфері. Молекули води, що розсіяні там (у хмарах у вигляді пари), захищають Землю від космічного холоду.
Вода мас велике значення в житті людини, рослин і тварин. Взагалі без води неможливе існування живих організмів в умовах Землі. Вода є середовищем, в якому відбуваються хімічні процеси в усякому організмі. Вона визначає об'єм і пружність клітин, транспортує в клітину і з неї розчини речовин, охороняє клітину від різких коливань температури і сама бере участь у багатьох біохімічних реакціях, що забезпечують життєдіяльність організму. Відомо, що тіло людини приблизно на 65 % складається з води.
Велике значення вода має у промисловості, для транспорту, у будівництві. Особливо багато води потребують хімічна промисловість, металургійні підприємства, текстильні фабрики, цукрові й крохмале-патокові заводи. Так, на виробництво 1 т сталі витрачається 300 м3 води, 1 т паперу — 900 м3, 1 т хімічного волокна — понад 2000 м3.
Багато води потребує сільське господарство. Одній рослині соняшника треба за літо до 300 л води. На вирощування 1 т картоплі необхідно 100 м3, а 1 т зерна — 1000 м3 води.
Багато води витрачається у побуті. Кожна доросла людина щоденно споживає з їжею майже 2 л води. Значно більше вона витрачає її на побутові потреби. У великих містах витрати води становлять близько 100 л на людину щодоби. Не дивно, що загальний об'єм водовитра-чання в Україні з урахуванням втрат досягає 30 км3 на рік, що становить 60 % усього стоку її річок. Тому кожний з нас і ти особисто маєш усвідомити, що воду необхідно берегти.
Чи знаєш ти, що найбагатша водою тканина організму людини — склисте тіло ока? Воно містить 99 % води, а найбід-ніша — зубна емаль, 0,2 % Н20
Вода — джерело життя на Землі, сировина для промисловості, джерело енергії, чинник, що визначає погоду, клімат Землі
Колообіг води в природі. Вода в природі постійно рухається, здійснюючи колообіг. Його рушійною силою є Сонце, а головним джерелом води — Світовий океан. Майже чверть усієї сонячної енергії витрачається на випаровування води з поверхні водойм. Близько 2/3 атмосферної води повертається у вигляді опадів знову у Світовий океан, а 1/3 випадає на сушу. Ця вода поповнює льодовики, ріки й озера. У свою чергу, поверхневі води знову стікають у моря й океани. Вода, що зволожує ґрунт, всмоктується корінням рослин. Разом з водою рослини одержують розчинні поживні речовини. В рослинах вода піднімається по стеблах і у вигляді пари надходить в атмосферу через листя, і все повторюється знову (мал. 2).
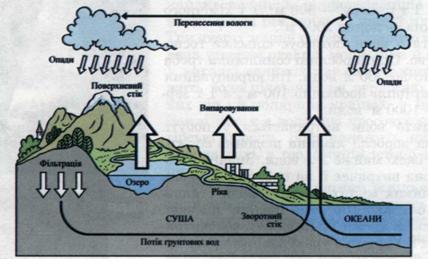
Мал. 2. Колообіг води
Колообіг — процес, що завершується поверненням до вихідного стану й первісної форми
Колообіг води — винятково важливий процес. Він забезпечує сушу прісною водою, яка постійно оновлюється. Заміна води в річках відбувається в середньому 30 разів на рік, тобто кожні 12 діб. Волога, яка міститься в ґрунті, оновлюється за 1 рік. Води проточних озер повністю обмінюються за десятки років, а непроточних — за 200—300 років. Води Світового океану оновлюються в середньому за 3000 років.
Наведені дані дають уявлення про те, як багато часу потрібно для самоочищення водойм. Тому проблема охорони водних ресурсів від забруднення — це державна проблема. На підприємствах будують очисні споруди, аби забруднена вода не потрапляла у природні водойми. Розчинні у воді відходи вилучають і намагаються переробляти, а очищену воду знову використовують на тому самому виробництві (замкнений цикл водопостачання).
В Україні прийнято Закон про охорону й раціональне використання природних ресурсів, у тім числі й водних. Від кожного з нас і від тебе також залежить чистота природних водойм.
Застосування оксидів. Оксиди широко використовують у промисловості. Оксиди Феруму, Алюмінію, Урану тощо — джерела добування металів. Прозорі кристали корунду Аl2O3 використовують в ювелірній промисловості як дорогоцінні камені: рубін — червоного, сапфір — синього кольору. Непрозорі кристали корунду застосовують для виготовлення шліфувальних брусків та інших абразивних матеріалів. SiO2 — річковий пісок використовують у будівництві та для виготовлення скла. CO — як паливо, а також відновник під час виплавляння сталі. ZnO — для виготовлення білої фарби, Fe2O3 — коричневої, Сr2O3 — зеленої, СO2 — для газування фруктової води.
ВИСНОВКИ
Оксиди — це складні речовини, що складаються з двох хімічних елементів, одним з яких є Оксиген із валентністю 2. За складом оксиди поділяють на оксиди металів і оксиди неметалів.
Оксиди дуже поширені в природі, оскільки кисень є однією з найактивніших речовин.
Найважливішим природним оксидом є вода — джерело життя на Землі, сировина для промисловості, джерело енергії, чинник, що визначає погоду, клімат Землі. Основні джерела води — моря й океани, річки й озера. Для усіх господарських потреб використовується прісна природна вода після її очищення. Прісної води на Землі мало. Воду потрібно берегти.
Завдання для самоконтролю
1. Користуючись періодичною системою, напиши формули вищих оксидів Гідрогену, Магнію, Натрію, Карбону, Алюмінію, Силіцію, Фосфору, Сульфуру, Барію. Зазнач назву кожного оксиду.
2. Із наведеного переліку формул сполук Н2O, NaOH, H2SO4, SO3, SiO2, H3PO4, CaO випиши формули оксидів. Зазнач їх назви.
3. Як ти думаєш, чому колообіг води в природі є винятково важливим процесом?
4. Обчисли, в якому з оксидів — у нітроген(ІV) оксиді чи у нітроген(V) оксиді — масова частка Нітрогену більша.
5. Яка кількість речовини алюміній оксиду містить Оксиген кількістю речовини 1,5 моль?
6*. Ферум утворює два оксиди, масова частка Феруму в яких становить 77,8 % і 70,0 %. Визнач формули цих оксидів і зазнач їх назви.
Н.М. Буринська, Хімія, 8 клас
Вислано читачами інтернет-сайту.
Допомога школяру 8 класу, підручники онлайн, конспекти та домашнє завдання з хімії
Зміст уроку
 конспект уроку і опорний каркас конспект уроку і опорний каркас
 презентація уроку презентація уроку
 акселеративні методи та інтерактивні технології акселеративні методи та інтерактивні технології
 закриті вправи (тільки для використання вчителями) закриті вправи (тільки для використання вчителями)
 оцінювання
Практика оцінювання
Практика
 задачі та вправи,самоперевірка задачі та вправи,самоперевірка
 практикуми, лабораторні, кейси практикуми, лабораторні, кейси
 рівень складності задач: звичайний, високий, олімпійський рівень складності задач: звичайний, високий, олімпійський
 домашнє завдання
Ілюстрації домашнє завдання
Ілюстрації
 ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа
 реферати реферати
 фішки для допитливих фішки для допитливих
 шпаргалки шпаргалки
 гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення
 зовнішнє незалежне тестування (ЗНТ) зовнішнє незалежне тестування (ЗНТ)
 підручники основні і допоміжні підручники основні і допоміжні
 тематичні свята, девізи тематичні свята, девізи
 статті статті
 національні особливості національні особливості
 словник термінів словник термінів
 інше
Тільки для вчителів інше
Тільки для вчителів
 ідеальні уроки ідеальні уроки
 календарний план на рік календарний план на рік
 методичні рекомендації методичні рекомендації
 програми програми
 обговорення обговорення
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|












