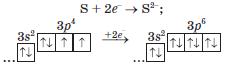|
Гіпермаркет Знань>>Хімія>>Хімія 10 клас>> Загальна характеристика неметалічних елементів. Поширення неметалічних елементів у природі. Застосування неметалів
Загальна характеристика Оксигену і Сульфуру Історичні відомості Про історію відкриття кисню, молекули якого складаються з елемента Оксигену, ви довідалися ще у 8 класі. Тепер ознайомтеся з деякими історичними відомостями про сірку, що складається з елемента Сульфуру. Сірка відома людині з давніх-давен. Легендарний давньогрецький поет Гомер, який жив між XII і VIII ст. до н. є. і вважається автором епічних поем «Іліада» і «Одіссея», зазначає, що сірка застосовувалась для куріння під час релігійних обрядів. Вона входила до складу славнозвісного в історії стародавнього світу грецького вогню. Секретом його виготовлення володіли грецькі царі протягом чотирьох віків. У 941 р. під стінами Царграду було знищено флот київського князя Ігоря. Літописець, розповідаючи про цю подію, зазначає, що греки пускали вогонь, ніби блискавку на небі, яка спалювала воїнів Ігоря, через що вони не змогли подолати греків. Про найдавніше знайомство людини з сіркою свідчить і походження її назви (від санскритського1 слова «сіра», що означає світло-жовтий).
Оксиген і Сульфур — елементи VI групи періодичної системи, входять до складу головної підгрупи.
Електронна будова Що ж видно з електронних формул Оксигену 1s22s22р4 і Сульфуру 1s22s22р63s23р4, які ви щойно записали? Вони показують, що в атомах Оксигену і Сульфуру на зовнішньому електронному шарі міститься по 6 електронів (див. підкреслене в електронних формулах) — ns2np4. В атомах Оксигену ці 6 зовнішніх електронів розміщуються на орбіталях двох типів — s i p (одна s- і три р- орбіталі): 8O n = 2
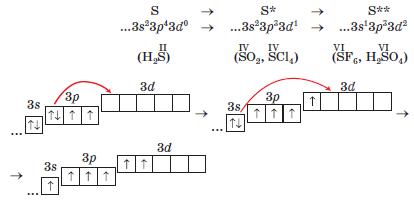
У сполуках з найбільш електронегативним елементом — Флуором Оксиген виявляє позитивний ступінь окиснення, наприклад у фториді Існують сполуки, що містять зв'язок Оксиген — Оксиген (О—О), на приклад пероксид гідрогену Н2 02 або пероксид барію 'Ва O2. Ступінь окиснення Оксигену в таких сполуках дорівнює, як вважається, -1. На відміну від Оксигену, який міститься у другому періоді періодичної системи і електрони в його атомах розміщені на двох електронних шарах (а електрони другого шару — на s- і р- орбіталях), Сульфур міститься у третьому періоді. Це означає, що електрони в атомах Сульфуру розміщені на трьох електронних шарах, а електрони третього шару можуть розміщуватись на s-, p- і d- орбіталях (якщо атом перебуває у збудженому стані). Отже, на відміну від атома Оксигену атом Сульфуру (ізольований, хімічно не зв'язаний) на зовнішньому електронному шарі має вільні орбіталі, на які можуть переходити електрони під час збудження атома, коли із затратою деякої енергії відбувається розпаровування електронних пар для утворення хімічних зв'язків з іншими атомами. Таким чином, в атомі Сульфуру електрони на зовнішньому електронному шарі можуть розмішуватися так: збуджені стани атома Атом Сульфуру, в якому є 2, 4 або 6 неспарених електронів, може виявляти у сполуках ступінь окиснення -2, +4, +6. -2 +4 +6 +6 +6 Наприклад: H2S; S02; S03; H2S04; Na2S04. Атом Сульфуру порівняно з атомом Оксигену має більший радіус (чому?) і виявляє меншу електронегативність. Поясніть, як ви розумієте поняття «радіус атома». Від чого залежать розміри атомів? Пригадайте, що таке електронегативність. Порівняйте елементи Оксиген і Сульфур за електронегативністю. Обґрунтуйте її відмінність.
Занальна характеристика Нітрогену і Фосфору Історичні відомості Відкриття азоту N2, молекули якого складаються з елемента Нітрогену N. приписують шотландському вченому Даніслю Резерфорду, який у 1772 р., досліджуючи частину повітря, що залишилася під дзвоном, декілька днів жила миша, встановив, шо це «повітря» не підтримує ні дихання, ні горіння. Він вважав, що воно насичене флогістоном, і назвав його «отруйним повітрям». Майже у цей самий час азот добули К. Шеєле, Дж. Прістлі, Г. Кавендіш. Проте всі ці видатні вчені були переконаними прихильниками теорії флогістону і з ним пов'язували властивості «отруйного повітря». Лише А. Лавуазьє, який вів наступ на флогістон, у 1776 р. дослідив цей газ і довів, що він є простою речовиною, а згодом і запропонував для нього назву азот — «безжиттєвий» (від грец. слів «а» — заперечення і «зое» — життя). Фосфор було відкрито у 1669 р. Хеннінгом Брандом, алхіміком з Гамбурга, який намагався відшукати філософський камінь, за допомогою якого старі люди нібито молодшають, хворі видужують, а неблагородні метали перетворюються на золото. Під час одного з дослідів X. Бранд випарив сечу, залишок змішав з вугіллям та піском і продовжував випарювати. Невдовзі у колбі утворилася речовина, що світилася у темряві (фосфор — від грец. світлоносний).
Нітроген і Фосфор — типові елементи V групи періодичної системи, належать до головної підгрупи. • Пригадайте будову атомів Нітрогену і Фосфору на основі положення цих елементів у періодичній системі й запишіть їхні електронні формули.
Електронна будова Електронні формули Нітрогену 1s22s22p3 і Фосфору 1s22s22p63s23p3 показують, що в їхніх атомах на зовнішньому електронному шарі міститься по 5 електронів. В атомі Нітрогену вони розміщені на орбіталях у такий спосіб: 7N n = 2 Ступінь окиснення Нітрогену в сполуках може бути від -3 (коли атом відтягує 3 електрони від атома менш електронегативного елемента) до +5 (коли 1, 2, 3, 4 або всі 5 валентних електронів відтягуються до атомів більш електронегативних елементів, ніж Нітроген).
• Напишіть формули сполук Нітрогену з Гідрогеном і Оксигеном, де Нітроген виявляє різні ступені окиснення, і в кожному з випадків поясніть, чим зумовлений даний ступінь окиснення атома Нітрогену. Атом Фосфору має подібну електронну будову зовнішнього електронного шару: 15P n = 3
основний стан атома Відмінність полягає у тому, що в атомі Фосфору на зовнішньому електронному шарі є вільні d-орбіталі, це дає можливість йому переходити у збуджений стан (порівняйте з Сульфуром): 15P n = 3
збуджений стан атома
• Напишіть формули сполук Фосфору з Гідрогеном і Оксигеном, де Фосфор виявляє зазначені ступені окиснення, і поясніть, чим вони зумовлені.
Утворення фосфором кількох алотропних форм пояснюється різним розміщенням атомів один відносно одного у кристалічних ґратках.
У природі Нітроген зустрічається як у вільному стані, так і у зв'язаному. У вільному стані Нітроген у вигляді азоту входить до складу повітря (об'ємна частка N2 становить 78 %, масова — 75,6 %). Оскільки азот з повітря витрачається мало, його запаси в атмосфері залишаються сталими. У вигляді неорганічних сполук Нітроген у невеликих кількостях є в ґрунті. Проте у вигляді складних органічних сполук — білків — він увіходить до складу всіх живих організмів, беручи участь у їх життєдіяльності.
На відміну від Нітрогену Фосфор зустрічається в природі тільки в сполуках (чому?). Найважливіші мінерали, до складу яких уходить фосфат кальцію Са3(Р04)2, — це фосфорити и апатити. Найбільше у світі родовище апатитів на Кольському півострові у Хібінських горах.
В Україні родовища фосфоритів зустрічаються у Придністров'ї, на Харківщині, в Чернігівській та Запорізькій областях.
Елемент Фосфор — важлива складова частина організму людини, тварин і рослин. З рослин найбагатші на Фосфор бобові, соняшник і горіхи. В організмі людини Фосфор виявлений в усіх тканинах, особливо у нервовій і кістковій. Він входить до складу деяких ферментів, міститься в зубах, фосфор — життєво важливий елемент для всіх організмів.
Загальна характеристика Карбону і Силіцію
Історичні відомості Ім'я першовідкривача вуглецю, що гадається в основному з Карбону, невідоме. Невідомо й те, яка з алотропних форм Карбону — алмаз чи графіт — була відкрита раніше. Історія використання людиною цієї речовини сягає у глибочінь століть, у доісторичні часи. Напевно твердити можна лише те, що до алмазу й графіту людина вже знала вугілля. А визнання Карбону хімічним елементом сталося лише у 1775 p., завдяки роботам французького вченого А. Лавуазьє.
Силіцій, незважаючи на велику поширеність його у природі, відкрили порівняно пізно. У 1811 р. французькі хіміки Ж. Л. Гей-Люссак і Л. Ж. Тенар добули чистий силіцій (проста речовина, що складається з елемента Силіцію). Новий елемент назвали Силіцієм (від лат. silex — кремінь), що означає «камінь, який дає вогонь». Так назвали твердий камінь, що під час удару викресав іскру. Тривалий час його використовували замість сірників для добування вогню.
Карбон і Силіцій — типові елементи IV групи періодичної системи, належать до головної підгрупи. • Пригадайте будову атомів Карбону і Силіцію на основі розміщення цих елементів у періодичній системі й запишіть їхні електронні формули.
Електронна будова Електронні формули Карбону 1s22s22p2 і Силіцію 1s22s22p63s23p2 показують, що в їхніх атомах на зовнішньому електронному шарі міститься по 4 електрони. Вони розміщені на орбіталях у такий спосіб: 6С n = 2 • Покажіть графічно розміщення на орбіталях електрод зовнішнього шару атома Силіцію. Зверніть увагу: в атомах Карбону і Силіцію на зовнышньому електронному шарі є вільна p-орбіталь. Тому один s-електрон зовнішнього шару під час збудження атома може переходити на цюp-орбіталь (збуджений стан атома): 6С* n = 2
• Напишіть формули сполук Карбону з Оксигеном і Гідрогеном. Зазначте ступені окиснення елементів і назвіть сполуки. Поясніть у кожному з випадків, чим зумовлений даний ступінь окиснення.
Поняття про олотропію. Озон Хімічні елементи у вільному стані існують у формі простих речовин. Так, елемент Оксиген утворює дві прості речовини — кисень 02 та озон 03. • Пригадайте, що являє собою кисень 02, які характерні властивості він має, для чого використовується і яку роль відіграє у природі.
302 ⇔203; ΔH = 283,6 кДж.
Кисень поглинає енергію і перетворюється на озон, а озон самовільно розкладається, утворюючи кисень. Обидві прості речовини — кисень 02 і озон 03 — утворені одним і тим самим хімічним елементом — Оксигеном, а властивості у них різні (табл. 1).
Явище існування хімічного елемента у вигляді двох або кількох простих речовин, різних за властивостями і будовою, називається алотропією, а самі прості речовини — алотропними формами (модифікаціями). Отже, кисень 02 і озон 03 — алотропні форми елемента Оксигену. Порівняння властивостей кисню 02 й озону 03 засвідчує, що окисна активність озону вища, ніж кисню. Наприклад, вже за звичайних умов він окиснює багато які малоактивні прості речовини (срібло, ртуть тощо): 8Ag + 203 = 4Ag20 + 02↑
Таблиця 1. Властивості кисню й озону
Застосування озону зумовлене його винятковими окисними властивостями. Озон використовується для озонування питної води, що значно ефективніше, ніж хлорування; для знешкодження промислових стічних вод; вибілювання тканин, мінеральних масел; як дезінфікуючий засіб у медицині; як окисник ракетного палива. Зверніть увагу на фізіологічну дію озону: він отруйний для людини, тварин і рослин. Невеликі концентрації озону в повітрі створюють відчуття свіжості, але вдихання повітря навіть із зовсім малою концентрацією озону викликає подразнення дихальних шляхів, кашель, блювоту, запаморочення, стомленість. Проте озон може бути не лише шкідливим, а й корисним.
Роль озону в збереженні життя на Землі Біля поверхні Землі озону мало. Його концентрація у повітрі коливається (вночі менша, вдень більша). Влітку і навесні його в повітрі у 3,5 раза більше, ніж узимку і восени. Над полярними частинами Землі вміст озону в повітрі вищий, ніж над екватором, в атмосфері міст — вищий, ніж у сільській місцевості. 3 віддаленням від поверхні Землі концентрація озону збільшується і досягає максимуму на висоті 20 — 25 км. Там утворюється так званий озоновий шар. Озоновий шар відіграє значну роль у збереженні життя на нашій планеті. Він затримує найбільш згубну для людини, тварин і рослин частину ультрафіолетової радіації Сонця, яка спричинює онкологічні (ракові) захворювання шкіри. Окрім того, озоновий шар разом з вуглекислим газом С02 поглинає інфрачервоне випромінювання Землі і тим самим запобігає її охолодженню. Так озоновий шар забезпечує збереження життя на Землі. Виникає запитання, звідки ж береться озон в атмосфері і як саме він захищає нас. Озон утворюється у верхніх шарах атмосфери внаслідок поглинання киснем ультрафіолетового випромінювання Сонця: 02 + hv → О + О О + 02 → 03 Крім того, поглинаючи променисту енергію Сонця (фотони), молекули кисню переходять у збуджений стан (помічено зірочкою) і під час дальшої взаємодії зі звичайним киснем також утворюють озон: 02 + hv → 0*2 02 + 02 → 03 + 0 О + 02 → 03 Озон, що утворився, огортає Землю з усіх боків. Але молекули озону існують недовго. Відбувається зворотна реакція фотохімічного розкладу озону, яка, власне, являє собою поглинання озоном фотонів: 03 + hv → 02 + О Отже, в атмосфері існує цикл озону — збалансовані утворення і розклад його. Результатом існування цього циклу є перетворення ультрафіолетового випромінювання Сонця на теплову енергію. Але для нас головна «заслуга» озону полягає в тому, що він, «жертвуючи собою», поглинає ультрафіолетове випромінювання і тим самим не допускає високоенергетичні фотони Сонця до Землі. Озоновий шар не є стабільним. Він може самовільно то збільшуватись, то зменшуватись над певною місцевістю по кілька разів на рік. Під впливом природних факторів (фото-хімічного розкладу, виверження вулканів, значного переміщення великих повітряних мас), а більшою мірою під впливом забруднення навколишнього середовища він зазнає руйнування, внаслідок чого утворюються так звані «озонові дірки», які збільшують ультрафіолетове навантаження на все живе на Землі. Причиною техногенного руйнування озонового шару є забруднення атмосфери оксидами нітрогену, наявність яких у 20 разів збільшує токсичність озону. Так, масове викидання в атмосферу вихлопних газів реактивних літаків, що містять оксиди нітрогену, руйнує озоновий шар. Окрім того, використання хлоро- і флуоровмісних речовин (фреонів) у холодильних машинах також спричинює руйнування озонового шару. Адже фреони, якщо потрапляють в атмосферу, реагують лише з озоном, бо відносно інших речовин вони інертні. Внаслідок цього над місцевістю може утворитися «озонова дірка». Над Україною (окрім південної частини) загальний вміст озону за останні 20 років зменшився на 6 %, і утворилася і аномальна зона. Вам про це слід пам'ятати! Особливо небезпечна «озонова дірка» влітку. У цей період дуже потерпають очі, тому треба користуватися сонцезахисними окулярами. Варто утримуватися і від загару, щоб не зашкодити шкірі. Як ви гадаєте, чому кисень і озон, що складаються з одного й того самого хімічного елемента, мають різні властивості, тобто у чому полягає суть алотропії? Алотропія кисню й озону зумовлена різною кількістю атомів Оксигену в молекулах речовин — 02 і 03. Проте буває й інша причина алотропії — різна структура кристалів. З таким типом алотропії ви ознайомитеся на прикладі сірки. Сірка за звичайних умов — крихка кристалічна речовина жовтого кольору. Погано проводить теплоту і не проводить електричного струму. У воді не розчиняється, краще розчиняється в деяких розчинниках (у сірковуглеці CS2, бензині, ефірі та ін.). І в розчинах, і в кристалах сірка складається з циклічних молекул S8, які за формою нагадують корону. Але в кристалах ці молекули можуть бути упаковані по-різному. Якщо молекули розташовані щільно, утворюється алотропна форма ромбічна сірка. Менш щільне упакування молекул спричинює виникнення іншої алотропної форми — моноклінної сірки. Різна будова кристалів ромбічної і моноклінної сірки зумовлює різні їхні фізичні властивості. Деякі з них наводяться у таблиці 2. Якщо сірку розплавити і швидко охолодити, утворюється ще одна алотропна форма: пластична сірка — коричнева гумоподібна маса. Їй можна надати будь-якої форми, навіть розтягнути в нитку. Ця властивість пластичної сірки пояснюється тим, що вона не містить молекул S8, а складається з довгих ланцюжків атомів Сульфуру. Ці ланцюжки безладно переплутані між собою. Під час розтягування вони розпрямляються, а якщо випустити — знову скручуються. Цим пояснюється еластичність даної форми. Але пластична сірка дуже нестійка, швидко загусає, твердне, стає крихкою і перетворюється на ромбічну. Отже, у сірки є дві основні алотропні форми: ромбічна і моноклінна. Обидві вони складаються з молекул S8, a різняться кристалічною будовою. Таблиця 2. Властивості ромбічної і моноклітинної сірки
• Згадайте, як утворюється в атмосфері озон, і обґрунтуйте його значення. У чому ви вбачаєте подвійну роль озону в природі — його користь і шкоду? Сірка зустрічається в природі у вільному стані (самородна сірка), а також у вигляді різних сполук — сульфідів металів, сульфатів тощо.
Лабораторна робота 1 Ознайомлення із зразками сірки та її природних сполук Розгляньте видані вам зразки сірки та її природних сполук. Для кожного з них запишіть у зошит: 1) назву, 2) хімічну формулу, 3) агрегатний стан, 4) колір, 5) твердість. Ви довідались, що в природі дуже поширені сполуки сульфуру з різними металами. Багато з них є цінними рудами: РЬS — свинцевий блиск, ZnS — цинкова обманка, Cu2S — мідний блиск, FeS2 — залізний колчедан, або пірит. Поширені в природі й інші мінерали Сульфуру, в основному сульфати кальцію і магнію. Поклади сполук Сульфуру є в Україні (Львівська область), Туркменістані, Італії, Японії, США та ін.
Алотропія Карбону У природі зустрічаються три алотропні форми Карбону: алмаз, графіт і карбін. Алмаз (від грец. adamas — непохитний, твердий) — кристалічна речовина, тугоплавка, хімічно малоактивна, діелектрик, практично не проводить електричного струму. Кристалічні ґратки атомні (мал. 10.). Мал. 10. Кристалічні ґратки. Приклади застосування алмазу
Зустрічаються кристали безбарвні або забарвлені у жовтий, коричневий, рожево-бузковий, зелений, голубий, синій і чорний колір. Кристали можуть бути прозорі і непрозорі, для них характерний сильний блиск. У кристалі алмазу кожний атом Карбону з'єднується міцними ковалентними зв'язками з чотирма сусідніми атомами. Такою будовою кристалів пояснюється виключна твердість алмазу. Він найтвердіший з усіх відомих речовин. Завдяки твердості алмаз широко використовується для свердління твердих порід, виготовлення шліфувальних дисків, різців, свердел, різання скла (див. мал.10) тощо. Для цього застосовують технічні алмази, тобто такі, що містять різні домішки. Чисті алмази — безбарвні прозорі кристали. Їх гранують, шліфують (алмазним порошком) і виготовляють з них діаманти. Прозорі алмази красивого синього, зеленого, червонуватого кольору надто рідкісні й оцінюються дуже високо. Чим більше граней має кристал, тим краще він «грає». Маса діамантів вимірюється каратами (1 карат = 0,2 г). Найбільший з будь-коли знайдених на Землі алмазів — це алмаз «Куллінан». Його знайшли у 1905 р. Назву він здобув від імені одного із володарів. До огранювання його розмір був з жіночий кулак і маса 3106 каратів, тобто 621 г. Під час обробки алмаз розкололи за напрямом тріщин, що були у ньому, і вирізали 105 діамантів. Найбільший серед них назвали «Зоряна Африка». Він має форму краплі і масу 530 каратів. Цікаво, що серед індійських алмазів є славнозвісний «Шах» масою 89 каратів, яким перський уряд, щоб «уласкавити білого царя», розплатився за кров відомого російського дипломата і видатного письменника О. С. Грибоєдова, полеглого від рук розлюченого натовпу перських фанатиків у 1829 р. у Тегерані — столиці Персії. Розроблено штучне добування алмазів (1954 p., США) з графіту в умовах високих тисків і температур. Як правило, утворюються дрібні кристали. Їх використовують для виготовлення різальних інструментів і як опору для підшипників та інших рухливих частин у точних вимірювальних інструментах. Нині виробляються й синтетичні алмази ювелірної якості. Промисловий синтез алмазів — велике досягнення науки і техніки. Графіт (від грец. grapho — пишу) — кристалічна речовина, жирна на дотик, сірого або чорного кольору з металічним блиском. Структура графіту шарувата (мал. 11): атоми карбону розміщені шарами, що складаються з шестичленних кілець. У межах одного шару кожний атом Карбону утворює три хімічні зв'язки з трьома сусідніми атомами. Усі атоми Карбону об'єднуються у макромолекули, які являють собою нескінченні шари із шестичленних кілець. За рахунок четвертих електронів зовнішнього електронного шару кожного атома Карбону, що не беруть участі в утворенні хімічних зв'язків у площині, виникає загальна система хімічного зв'язку, делокалізованого у межах всієї макромолекули. Цим саме і визначається електрична провідність графіту, темно-сірий колір і металічний блиск. Шари атомів Карбону об'єднуються у кристалічні ґратки за рахунок міжмолекулярних сил. Всередині шару графіту зв'язки між атомами ковалентні, доволі міцні, а між шарами діють міжмолекулярні сили, доволі слабкі. Тому графіт легко розшаровується на лусочки. Це робить кристали графіту неміцними, а сам мінерал м'яким. Навіть під час слабкого тертя графіту по паперу на ньому залишається сірий слід. Графіт тугоплавкий (tпл. = 3800 °С), хімічно дуже стійкий. З нього виготовляють вогнетривкі тиглі, мастила, синтетичні алмази, електроди, обкладки для електролітичних ванн, труби теплообмінників (див. мал. 11). В ядерних реакторах графіт використовують як уповільнювач нейтронів. З графіту роблять грифелі для олівців. У промисловості, крім природного, використовують штучний графіт. Його добувають з кращих сортів кам'яного вугілля (кокс, антрацит). Процес відбувається в електропечах за температури 2600 — 3000 °С і тиску 250 МПа без доступу повітря. Карбін — чорна речовина. Складається з довгих ланцюгів атомів Карбону — С = С — С = С — С = С —, виявляє властивості напівпровідника. Існують ще так звані вуглецеві матеріали (раніше називали «аморфний вуглець»). До них належать вугілля (кокс, деревне вугілля), технічний вуглець (сажа) та ін. Вони не є самостійними алотропними формами Карбону, як це раніше вважалось, бо мікрокристалічна структура їх така сама, як у графіту, але кристали розміщені безладно. Сажу використовують як наповнювач для гуми і пластмас, пігмент для друкарської фарби, копіювального паперу, стрічки для друкарських машинок та ін. Кокс використовують у металургії як паливо і відновник. Застосування деревного вугілля ґрунтується на його здатності притягувати до своєї поверхні молекули речовин з навколишнього середовища (вбирання на поверхні). Таке явище називають адсорбцією. Зрозуміло, що чим більша поверхня, тим сильніша адсорбція. Щоб збільшити поверхню вугілля, його активують — обробляють перегрітою водяною парою для видалення з його nop сторонніх домішок і збільшення поруватості. Таке вугілля називають активованим. Активоване вугілля чудовий адсорбент (вбирник). Саме тому його використовують у промисловості для очищення газів, вловлювання цінних органічних розчинників, виготовлення протигазів, у медицині — для очищення крові і вбирання шкідливих
Завдання для самоконтролю 1. Яке місце у періодичній системі елементів займають Оксиген і Сульфур? Як це пов'язано з будовою їхніх атомів? 2. Чим відрізняється основний стан атома Сульфуру від його збудженого стану? 3. Порівняйте будову атомів елементів Оксигену і Сульфуру, зазначте їхні спільні й відмінні ознаки. 4. Чому атоми Оксигену й Сульфуру здатні виявляти ступінь окислення -2, а ступінь окиснення +4 і +6 — тільки атоми Сульфуру? 5. Напишіть формули сполук Оксигену та Сульфуру з Кальцієм, Калієм, Алюмінієм. Зазначте ступінь окиснення кожного з елементів і назви сполук. 6. Яке місце у періодичній системі елементів займають Hітроген і Фосфор? Як це пов'язано з будовою їхніх атомів? 7. Запишіть електронну формулу атома Нітрогену. В чому подібність і відмінність будови атома Нітрогену й атомів Оксигену та Флуору? 8. Покажіть графічно будову зовнішнього електронного шару атома Нітрогену та атома Фосфору. Що ви вбачаєте спільного і чим вони різняться між собою? 9. Які ступені окиснення властиві Нітрогену? Як їх можна пояснити? Визначте валентність і ступінь окиснення Нітрогену в молекулі азоту N2. 10. Що таке алотропія? Схарактеризуйте найголовніші алотропні форми Фосфору. Розкрийте причину відмінності їхніх властивостей. 11. Як ви гадаєте, чому азот — газ, а фосфор — тверда речовина? 12. Порівняйте алотропію Оксигену і Фосфору. Що тут спільного і в чому відмінність? 13. Розкрийте фізіологічну роль Нітрогену і Фосфору. 14. У якому вигляді Нітроген і Фосфор зустрічаються в природі і чому? 15. Які місця у періодичній системі хімічних елементів займають Карбон і Силіцій? Як це пов'язано з будовою їхніх атомів? 16. Як пояснити з погляду електронної теорії структуру атома Силіцію? Чому неметалічні ознаки виявлені у нього меншою мірою, а металічні ознаки — більшою, ніж у елемента Карбону? 17. Що таке алотропія і чим пояснюється існування різних алотропних форм? 18. Що собою являє озон за звичайних умов? З якою метою він застосовується? 19. Схарактеризуйте відомі вам алотропні форми Сульфуру і зазначте, яка з них найбільш стійка. 20. Внаслідок розкладу бертолетової солі КСlO3 (хлорат калію) за наявності оксиду мангану (ІV) добуто кисень об'ємом 6,72 л (н. у.). Маса витраченої при цьому бертолетової солі становить (а) 24,5 г; (в) 245 г; (б) 2,45 г; (г) 0, 245 г. 21. Кисень виділяється під час термічного розкладання ряду сполук. Якщо взяти по 0,5 моль таких сполук, як оксид мерку-рію (ІІ), перманганат калію, бертолетова сіль, нітрат калію (утворюється нітрит калію KN02), то найбільша кількість речовини кисню виділиться під час розкладання (a) HgO; (в) КСlO3; (б) КМп04; (г) KN03. 22. Максимальна маса озону, яка може утворитися з 16 г кисню, становить (а) 12 г; (в) 24 г; (б) 16 г; (г) 32 г.
Н.М. Буринська, Л.П. Величко, Хімія, 10 клас Вислано читачами з інтернет-сайтів
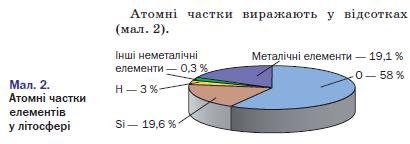
Неметалічні елементи Поширеність у природі. На нашій планеті неметалічні елементи більш поширені, ніж металічні. Атмосфера складається переважно з азоту і кисню — простих речовин Нітрогену й Оксигену. У повітрі є домішки інертних газів, водяної пари, вуглекислого газу, деяких інших сполук неметалічних елементів. Основна речовина гідросфери — вода. У ній розчинені гази, які входять до складу повітря, а також солі хлоридної, карбонатної, сульфатної кислот. У літосфері міститься майже 90 хімічних елементів, однак і в ній більш поширені неметалічні елементи. Вони утворюють велику кількість мінералів (мал. 1).
Мал. 1. Мінерали. У живих організмах переважають органічні речовини і вода, а це — також сполуки неме-талічних елементів. Поширеність хімічних елементів оцінюють, зіставляючи кількості їхніх атомів. Відношення кількості атомів елемента до кількості атомів усіх елементів у певному середовищі називають атомною часткою елемента. Атоми і йони.
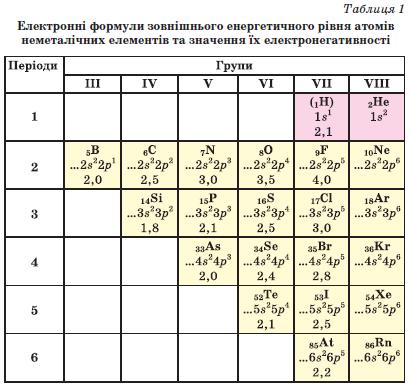
За електронною будовою зовнішнього енергетичного рівня атомів більшість неметалічних елементів є елементами, а Гідроген і Гелій — з-елементами (табл. 1). Атоми неметалічних елементів на зовнішньому енергетичному рівні мають, як правило, від 4 до 8 електронів. Майже всі вони можуть приєднувати певну кількість електронів і перетворюватися на негативно заряджені йони — аніони1. Приклад перетворення атома Сульфуру на сульфід-іон: На зовнішньому енергетичному рівні нової частинки (аніона) перебуває 8 електронів, тобто електронний октет. Проілюструємо розглянуту властивість атомів неметалічних елементів загальною схемою: Отже, такі атоми здатні бути окисниками; під час відповідних хімічних реакцій вони зазнають відновлення. ► Запишіть схему перетворення атома Хлору на йон, використавши електронні формули частинок. Аніони неметалічних елементів разом із катіонами металічних елементів входять до складу бінарних йонних сполук — оксидів (наприклад, Ьі20, ВаО, А1203), солей (КаГ, К28 тощо), деяких інших сполук (наприклад, СаН2, М^). ► Назвіть неметалічний елемент, який утворює не тільки аніон, а й катіон. У молекулах багатьох речовин (Н2, НГ, СО2, Н2804, С2Н5ОН та ін.) містяться атоми немета-лічних елементів, сполучені ковалентними зв'язками. Хімічний зв'язок такого типу реалізується завдяки утворенню спільних електронних пар із неспарених електронів двох атомів. Ділянки перекривання орбіталей можуть бути рівновіддаленими від ядер атомів (наприклад, у молекулі Н : Н) або зміщеними в бік одного з них (Н :Вг). У першому випадку ковалентний зв'язок є неполярним, а в другому — полярним. Зміщення спільної електронної пари позначають стрілкою або записом зарядів над символами елементів: Величину, яка характеризує здатність атома притягувати електрони, називають електронегативністю. Зіставляючи її значення для різних елементів (табл. 1), можна з'ясувати, чи зміщується спільна електронна пара, а якщо зміщується, то до якого атома.
Порівняйте хімічні зв'язки в таких молекулах: а) О2, Н2О і 0Г2; б) Н2, Н28 і РН3. Здатність атомів неметалічних елементів приєднувати електрони або зміщувати їх у свій бік зростає у періоді зліва направо, а в групі — знизу догори1. Тому найтиповіший неметаліч-ний елемент перебуває у правому верхньому куті періодичної системи. Це — Флуор.
Валентність. Значення валентності хімічного елемента визначається кількістю спільних електронних пар, які утворює його атом з іншими атомами. Вам відомо, що валентні можливості елемента можна передбачити за кількістю неспарених електронів в атомі. Наприклад, в атомі Оксигену — два неспарені електрони, тому він має бути двовалентним. За наявності вакантних орбіталей зовнішнього енергетичного рівня атоми можуть переходити у збуджений стан. Його позначають зірочками справа від символу елемента. Для атома Бору існує один збуджений стан, для атома Сульфуру можливі два такі стани, а для атома Хлору — три. Покажемо процес збудження атома Сульфуру за допомогою електронних формул та їх графічних варіантів (у дужках — формули сполук із відповідною валентністю елемента):
Елементи, атоми яких не бувають у збудженому стані, — Флуор, Оксиген (вони мають сталу валентність), Нітроген. Ступені окиснення. Вам відомо, що ступінь окиснення елемента — це умовний цілочи-сельний заряд його атома в речовині. Значення ступенів окиснення неметалічного елемента можна передбачити, враховуючи заряд його простого йона, можливі значення валентності атома і зіставляючи цей елемент з іншими за електронегативністю. При визначенні ступеня окиснення елемента в речовині користуються правилом електронейтральності: сума ступенів окиснення всіх атомів у речовині дорівнює нулю. Значення ступеня окиснення елемента (без урахування знака) в речовині часто збігається зі значенням його валентності:
Існують речовини, у яких ступені окиснення елементів відрізняються від значень валентності. Це — прості речовини (крім інертних газів), деякі неорганічні сполуки, багато органічних сполук. ВИСНОВКИ Неметалічні елементи поширеніші за металічні. Поширеність хімічного елемента визначають за його атомною часткою, тобто відношенням кількості атомів елемента до кількості атомів усіх елементів у певному середовищі. Атоми неметалічних елементів мають на зовнішньому енергетичному рівні від 4 до 8 електронів і здатні приєднувати електрони, перетворюючись на аніони. Ця властивість посилюється в періодах зліва направо, а в групах — знизу догори. Значення валентності неметалічного елемента визначається кількістю неспарених електронів у його атомі, що взяли участь в утворенні ковалентних зв'язків з іншими атомами. Ступені окиснення неметалічних елементів у сполуках можуть бути від'ємними або додатними числами.
П.П. Попель, Л.С. Крикля.Хімія, 10 клас Надіслано читачами інтернет-сайту
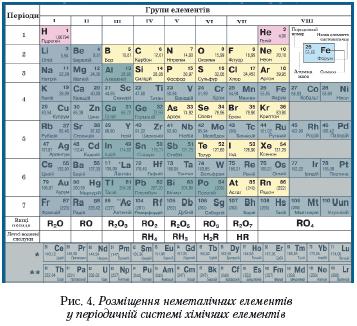
Неметалічні елементи, розташування в періодичній системі, загальна характеристика Скористайтеся фрагментом періодичної системи хімічних елементів Д. І. Менделєєва та ознайомтеся з назвами й символами неметалічних елементів, які зображені на рожевому та жовтому фонах (рис. 4).
Користуючись рисунком 4, установіть: 1. Чи властиве неметалічним елементам розміщення на початку періодів? Який виняток існує? 2. Чи властиве неметалічним елементам розміщення в кінці періодів? Який виняток існує? 3. У головних чи побічних підгрупах розміщені неметалічні елементи? 4. Чи є серед неметалічних елементів хоча б один, розміщений у побічній підгрупі?
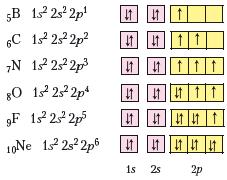
Приклад 1. Неметалічні елементи одного періоду. Неметалічні елементи Бор, Карбон, Нітроген, Оксиген, Флуор і Неон належать до другого періоду періодичної системи хімічних елементів і мають такі електронні та графічні електронні формули атомів:
Приклад 2. Неметалічні елементи однієї підгрупи. Карбон і Силіцій розташовані в IV групі в головній підгрупі періодичної системи хімічних елементів, тобто є елементами однієї групи й підгрупи. Напишемо електронну та графічну електронну формули атома Силіцію: Скористаємося електронною й графічною електронною формулами атома Карбону з прикладу 1 й порівняємо електронні формули атомів цих хімічних елементів. Результати порівняння вказують на те, що електронні оболонки їх атомів відрізняються кількістю енергетичних рівнів, проте на зовнішньому енергетичному рівні в них однакова кількість електронів і вона чисельно дорівнює номеру групи. Електронні формули атомів Карбону і Силіцію свідчать, що неметалічні елементи IV групи головної підгрупи мають однакову будову зовнішнього енергетичного рівня і кількість електронів на ньому дорівнює половині електронів зовнішнього завершеного восьмиелектронного енергетичного рівня.
Приклад 3. Характеристика неметалічного елемента за будовою атома й розміщенням у періодичній системі. Хімічний елемент з протонним числом 52 — Телур Те — розташований у періодичній системі хімічних елементів у п'ятому періоді, сьомому ряді, VI групі, головній підгрупі. Відносна атомна маса 128. Ядро атома має заряд +52 і складається з 52 протонів і 76 нейтронів (128 - 52 = 76). Електронна оболонка атома налічує 52 електрони, які розташовані на п'ятьох енергетичних рівнях. На зовнішньому енергетичному рівні є б електронів, тому максимальна валентність Телуру б, максимальний ступінь окиснення +б. Формула вищого оксиду — ТеО3. Оскільки Телур — аналог (так називають елементи однієї підгрупи) Оксигену і Сульфуру, то це дає змогу записати електронну конфігурацію зовнішнього енергетичного рівня як ...552 5р4 і скласти його графічну електронну формулу: З графічної електронної формули зовнішнього енергетичного рівня бачимо, що для його завершення не вистачає 2 електронів, тому з Гідрогеном Телур утворює сполуку Н2Те.
О. Г. Ярошенко, хімія, 10 клас Надіслано читачами інтернет-сайтів
Онлайн бібліотека з підручниками і книгами з хімії, плани-конспекти уроків по всім предметам, завдання з хімії для 10 класу Зміст уроку Если у вас есть исправления или предложения к данному уроку, напишите нам. Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум. |
Авторські права | Privacy Policy |FAQ | Партнери | Контакти | Кейс-уроки
© Автор системы образования 7W и Гипермаркета Знаний - Владимир Спиваковский
При использовании материалов ресурса
ссылка на edufuture.biz обязательна (для интернет ресурсов -
гиперссылка).
edufuture.biz 2008-© Все права защищены.
Сайт edufuture.biz является порталом, в котором не предусмотрены темы политики, наркомании, алкоголизма, курения и других "взрослых" тем.
Ждем Ваши замечания и предложения на email: 
По вопросам рекламы и спонсорства пишите на email: