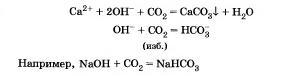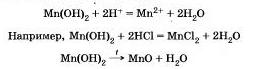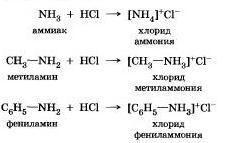|
|
|
| Строка 3: |
Строка 3: |
| | На каждом этапе развития ваших химических знаний основания, как и кислоты, вы определяли по-разному.<br> | | На каждом этапе развития ваших химических знаний основания, как и кислоты, вы определяли по-разному.<br> |
| | | | |
| - | Основания — это сложные вещества, в состав которых входят атомы металла, связанные с одной или несколькими гидроксогруппами (в зависимости от степени окисления металла). | + | [[Основания._Полные_уроки|Основания]] — это сложные вещества, в состав которых входят атомы металла, связанные с одной или несколькими гидроксогруппами (в зависимости от степени окисления металла). |
| | | | |
| - | <br>С точки зрения теории электролитической диссоциации основания — это электролиты, которые при диссоциации образуют в качестве отрицательных ионов только гидроксиданионы. | + | <br>С точки зрения теории электролитической диссоциации основания — это электролиты, которые при диссоциации образуют в качестве отрицательных ионов только гидроксиданионы. |
| | | | |
| - | <br>Наконец, в свете протолитической теории Брёнстеда—Лоури основания — это молекулы или ионы, которые служат акцепторами катионов водорода Н+ (протонов). | + | <br>Наконец, в свете протолитической теории Брёнстеда—Лоури основания — это молекулы или ионы, которые служат акцепторами катионов водорода Н+ (протонов). |
| | | | |
| - | <br>Последнее определение более полное, так как оно позволяет включить в класс оснований фторид-ион, аммиак, амины и другие вещества, которые оказались бы за рамками этого класса, если опираться на первое и второе определения. Классификация осковаиий по различным признакам дана в таблице 19. | + | <br>Последнее определение более полное, так как оно позволяет включить в класс оснований фторид-ион, аммиак, амины и другие вещества, которые оказались бы за рамками этого класса, если опираться на первое и второе определения. Классификация осковаиий по различным признакам дана в таблице 19. |
| | | | |
| - | <br>''Таблица 19 Классификации оснований'' | + | <br>''Таблица 19 Классификации оснований'' |
| | | | |
| - | [[Image:onov58.jpg]]<br> | + | [[Image:Onov58.jpg|Основания органические и неорганические]]<br> |
| | | | |
| - | [[Image:onov59.jpg]] | + | [[Image:Onov59.jpg|Основания органические и неорганические]] |
| | | | |
| | + | <br> |
| | | | |
| | + | Характеризуя свойства оснований, мы рассмотрим отдельно свойства гидроксидов [[Свойства_черных_и_цветных_металлов|металлов]] — кислородсодержащих оснований, причем особо выделим свойства щелочей. |
| | | | |
| - | Характеризуя свойства оснований, мы рассмотрим отдельно свойства гидроксидов металлов — кислородсодержащих оснований, причем особо выделим свойства щелочей.
| + | <br>''Химические свойства оснований''<br>Свойства щелочей — гидроксидов щелочных н щелочноземельных металлов |
| | | | |
| - | <br>''Химические свойства оснований''<br>Свойства щелочей — гидроксидов щелочных н щелочноземельных металлов | + | <br>1. Водные растворы щелочей мылкие на ощупь, разъедают кожу, ткань, изменяют окраску индикаторов: лакмуса — в синий, фенолфталеина — в малиновый. |
| | | | |
| - | <br>1. Водные растворы щелочей мылкие на ощупь, разъедают кожу, ткань, изменяют окраску индикаторов: лакмуса — в синий, фенолфталеина — в малиновый. | + | <br>2. Водные растворы основании (растворимых) диссоциируют. |
| | | | |
| - | <br>2. Водные растворы основании (растворимых) диссоциируют. | + | <br>3. Взаимодействуют с кислотами, вступая с ними в реакцию обмена.<br><br>Многокислотные основании могут в таких реакциях давать как средние, так и основные соли.<br><br>4. Взаимодействуют с кислотными [[Оксиды,_их_классификация_и_свойства|оксидами]], образуя средние и кислые соли а зависимости от основности кислоты, соответствующей этому оксиду: |
| | | | |
| - | <br>3. Взаимодействуют с кислотами, вступая с ними в реакцию обмена.<br><br>Многокислотные основании могут в таких реакциях давать как средние, так и основные соли.<br><br>4. Взаимодействуют с кислотными оксидами, образуя средние и кислые соли а зависимости от основности кислоты, соответствующей этому оксиду:
| + | [[Image:Onov60.jpg|Основания органические и неорганические]] |
| | | | |
| - | [[Image:onov60.jpg]]
| + | <br> |
| | | | |
| | + | 5. Взаимодействуют с амфотерными оксидами и гндроксидами:<br>а) при сплавлении (термическая диссоциация)<br>б) в растворах<br><br>6. Взаимодействуют с растворимыми в воде солями, если образуется осадок или газ. |
| | | | |
| | + | <br>7. Вступают в реакции с некоторыми органическими веществами, например с [[Фенолы_(Химия_10_класс)|фенолом]] — карболовой кислотой.<br><br>Нерастворимые основания взаимодействуют с кислотами и разлагаются при нагревании на основный оксид и воду. |
| | | | |
| - | 5. Взаимодействуют с амфотерными оксидами и гндроксидами:<br>а) при сплавлении (термическая диссоциация)<br>б) в растворах<br><br>6. Взаимодействуют с растворимыми в воде солями, если образуется осадок или газ.
| + | [[Image:Onov61.jpg|Основания органические и неорганические]]<br> |
| | | | |
| - | <br>7. Вступают в реакции с некоторыми органическими веществами, например с фенолом — карболовой кислотой.<br><br>Нерастворимые основания взаимодействуют с кислотами и разлагаются при нагревании на основный оксид и воду. | + | <br> |
| | | | |
| - | [[Image:onov61.jpg]]<br>
| + | ''Свойства бескислородных оснований'' |
| | | | |
| | + | <br>Рассмотрим их на примере аммиака и аминов<br>1. Взаимодействуют с кислотами, образуя соли но донорно-акцепторному механизму: |
| | | | |
| | + | [[Image:Onov62.jpg|Основания органические и неорганические]] |
| | | | |
| - | ''Свойства бескислородных оснований''
| + | <br> |
| | | | |
| - | <br>Рассмотрим их на примере аммиака и аминов<br>1. Взаимодействуют с кислотами, образуя соли но донорно-акцепторному механизму: | + | 2. Взаимодействуют с водой, образуя гидроксиды — слабые и непрочные кислородсодержащие основания<br><br>Основные свойства метиламина выражены более сильно, чем у аммиака, потому что положительный индукционный эффект метального радикала — СН3 увеличивает электронную плотность на атоме азота, обеспечивая тем самым его большую способность к присоединению протона. |
| | | | |
| - | [[Image:onov62.jpg]]
| + | <br>Водные растворы аммиака и аминов имеют щелочную среду и окрашивают фенолфталеин в малиновый цвет. Анилин такого действия не оказывает.<br>Ароматические амины плохо растворяются в воде. Их основные свойства ослаблены влиянием бензольного кольца, которое несколько оттягивает неподеленную электронную пару от атома азота аминогруппы, вследствие чего затрудняется прием протонов Н+. |
| | | | |
| | + | <br>Аммиак, метиламин и анилин можно расположить в следующий ряд в порядке ослабления их основных свойств. |
| | | | |
| | + | На этом примере, одном из многих, мы опять красноречиво подтверждаем универсальное проявление положения теории химического строений о взаимном влиянии атомов в молекулах веществ. |
| | | | |
| - | 2. Взаимодействуют с водой, образуя гидроксиды — слабые и непрочные кислородсодержащие основания<br><br>Основные свойства метиламина выражены более сильно, чем у аммиака, потому что положительный индукционный эффект метального радикала — СН3 увеличивает электронную плотность на атоме азота, обеспечивая тем самым его большую способность к присоединению протона. | + | <br>Влияние аминогруппы на бензольное ядро (радикал фенил) из-за наличия на атоме азота неподеленной электронной пары приводит к нарушению равномерности распределения замкнутой ''п''-электронной системы в бензольном кольце, вследствие чего атомы водорода будут более подвижными в 2. 4, 6-положениях.<br><br>По этой причине реакции замещения в бензольном кольце будут проходить в этих положениях. |
| | | | |
| - | <br>Водные растворы аммиака и аминов имеют щелочную среду и окрашивают фенолфталеин в малиновый цвет. Анилин такого действия не оказывает.<br>Ароматические амины плохо растворяются в воде. Их основные свойства ослаблены влиянием бензольного кольца, которое несколько оттягивает неподеленную электронную пару от атома азота аминогруппы, вследствие чего затрудняется прием протонов Н+. | + | <br>Многие амины с низкой молекулярной массой имеют неприятный запах испорченной рыбы, ведь они и аммиак образуются при разложении мертвых организмов без доступа [[Кислород|кислорода]]. |
| | | | |
| - | <br>Аммиак, метиламин и анилин можно расположить в следующий ряд в порядке ослабления их основных свойств. | + | <br>Некоторые лекарственные препараты (белый стрептоцид, норсульфазол, сульфидин) — производные ароматических аминов. |
| | | | |
| - | На этом примере, одном из многих, мы опять красноречиво подтверждаем универсальное проявление положения теории химического строений о взаимном влиянии атомов в молекулах веществ. | + | <br>1. Почему фенол откосят к кислотам, а анилин — к основаниям? Что общего во влиянии гидроксо- и аминогрупп на фенил? На примере этих веществ рассмотрите положение теории А. М. [[Теорія_хімічної_будови_органічних_сполук_О._М._Бутлерова.|Бутлерова]] о взаимном влиянии атомов в молекулах. |
| | | | |
| - | <br>Влияние аминогруппы на бензольное ядро (радикал фенил) из-за наличия на атоме азота неподеленной электронной пары приводит к нарушению равномерности распределения замкнутой ''п''-электронной системы в бензольном кольце, вследствие чего атомы водорода будут более подвижными в 2. 4, 6-положениях.<br><br>По этой причине реакции замещения в бензольном кольце будут проходить в этих положениях. | + | <br>3. Как изменяются основные свойства летучих водородных соединении в пределах одного периода? Рассмотрите на примере соединений элементов второго периода. Поясните ответ. |
| | | | |
| - | <br>Многие амины с низкой молекулярной массой имеют неприятный запах испорченной рыбы, ведь они и аммиак образуются при разложении мертвых организмов без доступа кислорода. | + | <br>4. Как изменяются основные свойства летучих водородных соединений одной подгруппы? Почему? Рассмотрите на примере соединений элементов главной подгруппы V группы. Поясните ответ. |
| | | | |
| - | <br>Некоторые лекарственные препараты (белый стрептоцид, норсульфазол, сульфидин) — производные ароматических аминов. | + | <br>5. Найдите массовую долю гидроксида натрия в растворе, полученном при взаимодействии 69 г натрия и 130 мл воды. Ответ: 61,2%. |
| | | | |
| - | <br>1. Почему фенол откосят к кислотам, а анилин — к основаниям? Что общего во влиянии гидроксо- и аминогрупп на фенил? На примере этих веществ рассмотрите положение теории А. М. Бутлерова о взаимном влиянии атомов в молекулах. | + | <br> |
| | | | |
| - | <br>3. Как изменяются основные свойства летучих водородных соединении в пределах одного периода? Рассмотрите на примере соединений элементов второго периода. Поясните ответ.
| + | 6. В 400 г 5%-иого раствора гидроксида натрия добавили 92 г натрия. Какой стала массовая доле щелочи в полученном растворе?<br>Ответ: 37.10%. |
| | | | |
| - | <br>4. Как изменяются основные свойства летучих водородных соединений одной подгруппы? Почему? Рассмотрите на примере соединений элементов главной подгруппы V группы. Поясните ответ.
| + | <br>7. Рассчитайте объем метиламина (н. у.), необходимого для получен на 16,2 г хлорида метилакмония. если его выход составил 80% от теоретически возможного. Ответ: 6.72 л. |
| - | | + | |
| - | <br>5. Найдите массовую долю гидроксида натрия в растворе, полученном при взаимодействии 69 г натрия и 130 мл воды. Ответ: 61,2%.
| + | |
| - | | + | |
| - | | + | |
| - | | + | |
| - | 6. В 400 г 5%-иого раствора гидроксида натрия добавили 92 г натрия. Какой стала массовая доле щелочи в полученном растворе?<br>Ответ: 37.10%.
| + | |
| - | | + | |
| - | <br>7. Рассчитайте объем метиламина (н. у.), необходимого для получен на 16,2 г хлорида метилакмония. если его выход составил 80% от теоретически возможного. Ответ: 6.72 л. | + | |
| | | | |
| | <br> | | <br> |
| | | | |
| - | <sub>вопросы [[Химия|по химии]] от учеников, ответы по [[Химия_11_класс|химии 11 класс]], тесты [[Гипермаркет_знаний_-_первый_в_мире!|по всем предметам]]</sub> | + | <sub>вопросы [[Химия|по химии]] от учеников, ответы по [[Химия 11 класс|химии 11 класс]], тесты [[Гипермаркет знаний - первый в мире!|по всем предметам]]</sub> |
| | | | |
| | '''<u>Содержание урока</u>''' | | '''<u>Содержание урока</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] конспект урока ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] конспект урока ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] опорный каркас | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] опорный каркас |
| - | [[Image:1236084776 kr.jpg|10x10px]] презентация урока | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] презентация урока |
| - | [[Image:1236084776 kr.jpg|10x10px]] акселеративные методы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] акселеративные методы |
| - | [[Image:1236084776 kr.jpg|10x10px]] интерактивные технологии | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] интерактивные технологии |
| | | | |
| | '''<u>Практика</u>''' | | '''<u>Практика</u>''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] задачи и упражнения | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] задачи и упражнения |
| - | [[Image:1236084776 kr.jpg|10x10px]] самопроверка | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] самопроверка |
| - | [[Image:1236084776 kr.jpg|10x10px]] практикумы, тренинги, кейсы, квесты | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] практикумы, тренинги, кейсы, квесты |
| - | [[Image:1236084776 kr.jpg|10x10px]] домашние задания | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] домашние задания |
| - | [[Image:1236084776 kr.jpg|10x10px]] дискуссионные вопросы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] дискуссионные вопросы |
| - | [[Image:1236084776 kr.jpg|10x10px]] риторические вопросы от учеников | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] риторические вопросы от учеников |
| - |
| + | |
| | '''<u>Иллюстрации</u>''' | | '''<u>Иллюстрации</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] аудио-, видеоклипы и мультимедиа ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] аудио-, видеоклипы и мультимедиа ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] фотографии, картинки | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фотографии, картинки |
| - | [[Image:1236084776 kr.jpg|10x10px]] графики, таблицы, схемы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] графики, таблицы, схемы |
| - | [[Image:1236084776 kr.jpg|10x10px]] юмор, анекдоты, приколы, комиксы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] юмор, анекдоты, приколы, комиксы |
| - | [[Image:1236084776 kr.jpg|10x10px]] притчи, поговорки, кроссворды, цитаты | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] притчи, поговорки, кроссворды, цитаты |
| | | | |
| | '''<u>Дополнения</u>''' | | '''<u>Дополнения</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] рефераты''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] рефераты''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] статьи | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] статьи |
| - | [[Image:1236084776 kr.jpg|10x10px]] фишки для любознательных | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фишки для любознательных |
| - | [[Image:1236084776 kr.jpg|10x10px]] шпаргалки | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] шпаргалки |
| - | [[Image:1236084776 kr.jpg|10x10px]] учебники основные и дополнительные | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] учебники основные и дополнительные |
| - | [[Image:1236084776 kr.jpg|10x10px]] словарь терминов | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] словарь терминов |
| - | [[Image:1236084776 kr.jpg|10x10px]] прочие | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] прочие |
| | '''<u></u>''' | | '''<u></u>''' |
| | <u>Совершенствование учебников и уроков | | <u>Совершенствование учебников и уроков |
| - | </u>'''[[Image:1236084776 kr.jpg|10x10px]] исправление ошибок в учебнике''' | + | </u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] исправление ошибок в учебнике''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] обновление фрагмента в учебнике | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обновление фрагмента в учебнике |
| - | [[Image:1236084776 kr.jpg|10x10px]] элементы новаторства на уроке | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] элементы новаторства на уроке |
| - | [[Image:1236084776 kr.jpg|10x10px]] замена устаревших знаний новыми | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] замена устаревших знаний новыми |
| - |
| + | |
| | '''<u>Только для учителей</u>''' | | '''<u>Только для учителей</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] идеальные уроки ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] идеальные уроки ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] календарный план на год | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] календарный план на год |
| - | [[Image:1236084776 kr.jpg|10x10px]] методические рекомендации | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] методические рекомендации |
| - | [[Image:1236084776 kr.jpg|10x10px]] программы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] программы |
| - | [[Image:1236084776 kr.jpg|10x10px]] обсуждения | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обсуждения |
| | | | |
| | | | |
Текущая версия на 19:47, 2 июля 2012
Гипермаркет знаний>>Химия>>Химия 11 класс>> Химия: Основания органические и неорганические
На каждом этапе развития ваших химических знаний основания, как и кислоты, вы определяли по-разному.
Основания — это сложные вещества, в состав которых входят атомы металла, связанные с одной или несколькими гидроксогруппами (в зависимости от степени окисления металла).
С точки зрения теории электролитической диссоциации основания — это электролиты, которые при диссоциации образуют в качестве отрицательных ионов только гидроксиданионы.
Наконец, в свете протолитической теории Брёнстеда—Лоури основания — это молекулы или ионы, которые служат акцепторами катионов водорода Н+ (протонов).
Последнее определение более полное, так как оно позволяет включить в класс оснований фторид-ион, аммиак, амины и другие вещества, которые оказались бы за рамками этого класса, если опираться на первое и второе определения. Классификация осковаиий по различным признакам дана в таблице 19.
Таблица 19 Классификации оснований
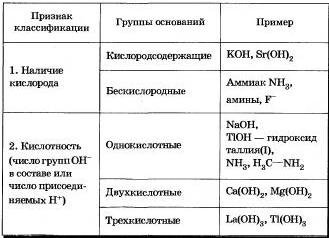

Характеризуя свойства оснований, мы рассмотрим отдельно свойства гидроксидов металлов — кислородсодержащих оснований, причем особо выделим свойства щелочей.
Химические свойства оснований
Свойства щелочей — гидроксидов щелочных н щелочноземельных металлов
1. Водные растворы щелочей мылкие на ощупь, разъедают кожу, ткань, изменяют окраску индикаторов: лакмуса — в синий, фенолфталеина — в малиновый.
2. Водные растворы основании (растворимых) диссоциируют.
3. Взаимодействуют с кислотами, вступая с ними в реакцию обмена.
Многокислотные основании могут в таких реакциях давать как средние, так и основные соли.
4. Взаимодействуют с кислотными оксидами, образуя средние и кислые соли а зависимости от основности кислоты, соответствующей этому оксиду:
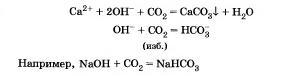
5. Взаимодействуют с амфотерными оксидами и гндроксидами:
а) при сплавлении (термическая диссоциация)
б) в растворах
6. Взаимодействуют с растворимыми в воде солями, если образуется осадок или газ.
7. Вступают в реакции с некоторыми органическими веществами, например с фенолом — карболовой кислотой.
Нерастворимые основания взаимодействуют с кислотами и разлагаются при нагревании на основный оксид и воду.
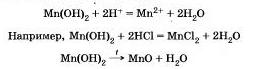
Свойства бескислородных оснований
Рассмотрим их на примере аммиака и аминов
1. Взаимодействуют с кислотами, образуя соли но донорно-акцепторному механизму:
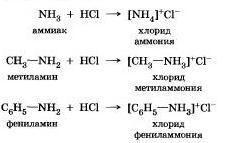
2. Взаимодействуют с водой, образуя гидроксиды — слабые и непрочные кислородсодержащие основания
Основные свойства метиламина выражены более сильно, чем у аммиака, потому что положительный индукционный эффект метального радикала — СН3 увеличивает электронную плотность на атоме азота, обеспечивая тем самым его большую способность к присоединению протона.
Водные растворы аммиака и аминов имеют щелочную среду и окрашивают фенолфталеин в малиновый цвет. Анилин такого действия не оказывает.
Ароматические амины плохо растворяются в воде. Их основные свойства ослаблены влиянием бензольного кольца, которое несколько оттягивает неподеленную электронную пару от атома азота аминогруппы, вследствие чего затрудняется прием протонов Н+.
Аммиак, метиламин и анилин можно расположить в следующий ряд в порядке ослабления их основных свойств.
На этом примере, одном из многих, мы опять красноречиво подтверждаем универсальное проявление положения теории химического строений о взаимном влиянии атомов в молекулах веществ.
Влияние аминогруппы на бензольное ядро (радикал фенил) из-за наличия на атоме азота неподеленной электронной пары приводит к нарушению равномерности распределения замкнутой п-электронной системы в бензольном кольце, вследствие чего атомы водорода будут более подвижными в 2. 4, 6-положениях.
По этой причине реакции замещения в бензольном кольце будут проходить в этих положениях.
Многие амины с низкой молекулярной массой имеют неприятный запах испорченной рыбы, ведь они и аммиак образуются при разложении мертвых организмов без доступа кислорода.
Некоторые лекарственные препараты (белый стрептоцид, норсульфазол, сульфидин) — производные ароматических аминов.
1. Почему фенол откосят к кислотам, а анилин — к основаниям? Что общего во влиянии гидроксо- и аминогрупп на фенил? На примере этих веществ рассмотрите положение теории А. М. Бутлерова о взаимном влиянии атомов в молекулах.
3. Как изменяются основные свойства летучих водородных соединении в пределах одного периода? Рассмотрите на примере соединений элементов второго периода. Поясните ответ.
4. Как изменяются основные свойства летучих водородных соединений одной подгруппы? Почему? Рассмотрите на примере соединений элементов главной подгруппы V группы. Поясните ответ.
5. Найдите массовую долю гидроксида натрия в растворе, полученном при взаимодействии 69 г натрия и 130 мл воды. Ответ: 61,2%.
6. В 400 г 5%-иого раствора гидроксида натрия добавили 92 г натрия. Какой стала массовая доле щелочи в полученном растворе?
Ответ: 37.10%.
7. Рассчитайте объем метиламина (н. у.), необходимого для получен на 16,2 г хлорида метилакмония. если его выход составил 80% от теоретически возможного. Ответ: 6.72 л.
вопросы по химии от учеников, ответы по химии 11 класс, тесты по всем предметам
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|