|
Гіпермаркет Знань>>Хімія>>Хімія 7 клас>> Речовини. Чисті речовини і суміші
Ми живемо у світі речовин. Подивись навколо, тебе оточує безліч предметів — фізичних тіл. Наприклад, цинк — речовина, а цинкове відро — фізичне тіло. Вода — речовина, а крапля води — фізичне тіло.
Речовини, які використовуються для виготовлення предметів, фізичних тіл, прийнято називати матеріалами.
Залізний цвях, мідна пластинка, алюмінієвий дріт — це фізичні тіла, а речовини, з яких вони зроблені — залізо, мідь, алюміній — це матеріали. Тут назви речовин і матеріалів збігаються.
Але так буває не завжди. Наприклад, дерев'яний штатив, дерев'яна лопата — це фізичні тіла, що зроблені з одного й того самого матеріалу — деревини, а основна речовина, що утворює деревину, — це клітковина, або целюлоза.
Нині відомо майже 20 000 000 різних речовин. Одні з них — природні, наприклад вода, кисень, вуглекислий газ. Інші — добуті штучно, наприклад капрон, поліетилен, синтетичний каучук.
Як же розібратися в цій безлічі речовин? Виявляється, кожна речовина має певну сукупність властивостей, які визначають її індивідуальність.
Властивості речовини — це певні ознаки, за якими різні речовини подібні між собою або відрізняються одна від одної.
Розрізняють фізичні й хімічні властивості речовин. До фізичних властивостей належать колір, блиск, запах, смак. Ці властивості можна виявити при безпосередньому спостереженні. Наприклад, золото можна відрізнити від інших речовин за його блиском і кольором. Цукор і кухонну сіль можна розрізнити за смаком.
УВАГА! Завжди пам'ятай, що куштувати невідомі речовини не можна, оскільки багато з них отруйні!
Деякі речовини можна впізнати за запахом.
* Назви речовини, які ти можеш упізнати за запахом, і пригадай, як треба нюхати, наприклад, невідомий газ або розчин (див. мал. 17).
Але не всі фізичні властивості виявляються за допомогою органів чуття. Так, щоб дізнатися про густину рідини, потрібно скористатися ареометром (мал. 35), а про температуру її кипіння — термометром, тобто є фізичні властивості, які вимірюють за допомогою приладів.
А чи належить агрегатний стан речовини до її фізичних властивостей?
З курсу фізики ти знаєш, що речовини існують у різних агрегатних станах. Лід, вода і водяна пара — це твердий, рідкий і газуватий стани однієї й тієї самої речовини — води. Отже, тверда, рідка й газу вата форми не є індивідуальними характеристиками води. Вони відповідають різним станам існування води за певних умов. Тому не можна приписувати воді лише ознаку рідини, кисню — ознаку газу, а залізу — ознаку твердої речовини. Будь-яка речовина в разі зміни умов може перейти в інший агрегатний стан.
Агрегатний стан — це не фізична властивість речовини, а лише стан, у якому вона перебуває за певних умов.
Інша річ, що під час переліку фізичних властивостей якоїсь речовини прийнято зазначати і її агрегатний стан, у якому вона перебуває за стандартних умов (за температури 298,15 К, або 25 °С, і тиску 100 кПа, або 760 мм рт. ст. (1 атм).
Аби переконатися, як ти розумієш фізичні властивості речовин, виконай такі досліди.
Зверни увагу, що для засвоєння знань тобі треба бути обізнаним із науковими методами пізнання. Вони єдині для всіх наук про природу. Передусім — це експеримент і спостереження.
Хімічний експеримент, який ти зараз будеш виконувати, — це найголовніший метод добування хімічних знань. Одночасно він є і видом практики, що підтверджує істинність знань. Під час виконання лабораторного експерименту уважно спостерігай зовнішній вигляд речовин та інші фізичні властивості.
Спостереження як метод наукового пізнання в хімії посідає особливе місце. У цьому ти переконаєшся в процесі подальшого навчання.
ЛАБОРАТОРНІ ДОСЛІДИ
Виявлення фізичних властивостей речовин
Завдання: зазнач агрегатний стан і схарактеризуй фізичні властивості двох речовин із числа запропонованих: а) натрій хлорид (кухонна сіль) і алюміній; б) вода і залізо; в) вода й олія; г) мідь і натрій карбонат (сода) за таким планом:
1) агрегатний стан речовини за стандартних умов;
2) колір, блиск;
3) запах;
4) розчинність у воді.
Щоб визначити розчинність, наприклад соди, треба за допомогою ложки або шпателя насипати трохи соди у пробірку (тільки вкрити дно!) і долити 1 мл води. Розчинення прискорюється в разі перемішування.
• Пригадай, як треба перемішувати рідину з твердою речовиною. У разі потреби звернись до мал. 28.
УВАГА! Не закривай пробірку пальцем і сильно не збовтуй рідину — це може спричини викидання рідини і пошкодження шкіри
Свої спостереження запиши у зошит.
Інші фізичні властивості — температуру кипіння або плавлення, твердість, густину, електричну провідність тощо можна з'ясувати, якщо потрібно, за хімічним довідником.
Аби вивчити фізичні властивості якоїсь речовини, необхідно очистити її від сторонніх домішок. У житті нам майже не трапляються чисті речовини, найчастіше ми маємо справу з сумішами речовин.
А як дізнатися про хімічні властивості речовини? Хімічні властивості вивчатимуться пізніше, оскільки вони виявляються лише в процесі перетворення одних речовин на інші. Так, здатність кисню підтримувати горіння і дихання, а заліза — іржавіти і є хімічними властивостями речовин кисню й заліза.
Як тобі здається, для чого потрібно вивчати властивості речовин? Властивості речовин вивчають для того, аби знати, як дану речовину з якомога більшою користю використовувати, як правильно з нею поводитися, як її розпізнати серед інших речовин. Адже є багато речовин з небезпечними для людини властивостями: одні легко спалахують і можуть спричинити пожежу, другі — отруйні і можуть викликати хворобу і навіть загибель людини, треті — здатні вибухати і можуть завдати непоправної шкоди. Однак усі ці небезпечні властивості можна спрямувати на користь людині. Як саме? Поміркуй і спробуй висловити з цього приводу свою думку.
Щоб робота з речовинами не спричинила нещасного випадку, треба знати властивості речовин, дотримуватися техніки безпеки й правил поведінки в кабінеті хімії.
КОРОТКІ висновки
Різні фізичні тіла й матеріали складаються з речовин. Кожна речовина характеризується певними фізичними й хімічними властивостями.
Сукупність властивостей речовини є тією ознакою, яка дає змогу відрізнити речовини одну від одної або встановити подібність між ними.
Завдання для самоконтролю
1. Як ти розумієш поняття "речовина", "матеріал", "матеріал"? Наведи приклади.
2. З наведенего переліку випиши окремо речовини й тіла: залізо, цвях, крохмаль, спирт, вода, сніжинка, краплина роси, сірник.
3. Порівняй фізичні властивості (ознаки схожості й відмінності) води й нашатирного спирту, взятих за стандартних умов.
4. Обгрунтуй, чому потрібно зазначити агрегатний стан, якщо йдеться про фізичні властивості речовини, хоча він не є фізичною властивістю.
Додаткові завдання
5. Тільки речовини (на відміну від фізичних тіл) містяться в ряду
(а) глюкоза, повітря, крохмаль;
(б) туман, вода, пісок;
(в) вуглекислий газ, кисень, мідь;
(г) залізо, молоко, жир.
6. Заповни таблицю:

Таблиця 1. Речовини.
7. Чому цвяхи виготовляють з заліза, а не з свинцю?
ЧИСТІ РЕЧОВИНИ І СУМІШІ
Ти вже знаєш, що кожна речовина має характерні для неї властивості. Однак ці властивості будуть цілком певні лише для окремо взятої речовини, не змішаної з іншими речовинами. Такі речовини називають чистими.
Чиста речовина — це речовина індивідуальна, яка не містить домішок інших речовин.
Від чистих речовин слід відрізняти суміші.
Суміш — це сукупність різних речовин, яка становить одне фізичне тіло.
Суміш може складатися з двох або більшої кількості чистих речовин. Оці складові частини суміші називаються компонентами. Речовини, що входять до складу сумішей, зберігають притаманні їм властивості.
Дослід 1. Якщо змішати порошок сірки з ошурками заліза, то речовини — залізо й сірка — зберігатимуть у суміші свої властивості. Так, залізо притягуватиметься магнітом, тонутиме у воді, якщо цю суміш всипати у воду, а сірка спливатиме, оскільки вона не змочується водою. Це використовують, щоб таку суміш розділити на окремі речовини.

Мал. 37. Порох - суміш речовин.
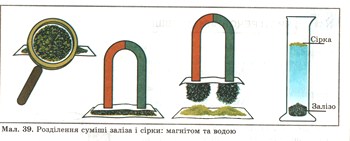
Мал. 39. Розділення суміши заліза і сірки: магнітом та водою.
Суміші речовин поділяють на однорідні й неоднорідні. В однорідних сумішах компоненти не можна помітити або виявити за допомогою оптичних приладів, оскільки речовини перебувають у дуже подрібненому стані. Наприклад, повітря — однорідна суміш кисню, азоту та інших газів; однорідною сумішшю є також розчин цукру у воді.
У неоднорідних сумішах неозброєним оком або за допомогою оптичних приладів можна помітити частинки речовин, з яких складається суміш. Наприклад, скаламучена у воді крейда, молоко — неоднорідні суміші.
• Пригадай, які природні суміші речовин ти знаєш.
• Поясни, на підставі яких ознак суміші поділяють на однорідні й неоднорідні. Наведи приклади.
За допомогою фізичних методів суміші можна розділити на складові частини. Нижче наведено способи розділення сумішей, деякі з них ти вже знаєш з курсу природознавства.
1. Відстоювання
Цим способом можна розділити тверді речовини, не розчинні у воді, або рідини, не розчинні одна в одній, якщо вони мають різну густину.
Дослід 2. Щоб розділити суміш залізних ошурків з тирсою, треба всипати суміш у воду і дати їй відстоятись. Ошурки осядуть на дно посудини, а тирса спливе. Воду над осадом зливають (декантація, мал. 40).
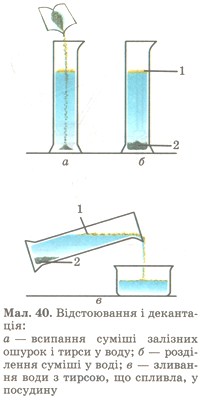
Мал. 40. Відстоювання і декантація.
У промисловості, якщо речовини значно відрізняються одна від одної за густиною, для їх розділення використовують проточну воду. Прикладом може бути добування золота із золотоносного піску. Пісок, що містить часточки золота, промивають проточною водою в похилому жолобі. Пісок виноситься водою, а важкі часточки золота осідають на дно жолоба. Так само відокремлюють подрібнене кам'яне вугілля від пустої породи.
Для розділення нерозчинних або малорозчинних одна в одній рідин з різними густинами використовують ділильну лійку (мал. 41). Суміш рідин, наприклад бензину з водою, наливають у лійку й відстоюють доти, доки між ними з'явиться досить чітка межа поділу. Після цього з лійки виймають корок, повертають кран і випускають воду, залишаючи бензин у лійці.
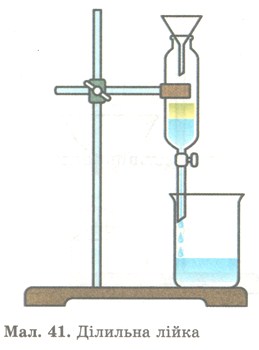
Мал. 41. Ділильна лійка.
2. Фільтрування
Цей спосіб застосовують для розділення суміші розчинних і не розчинних у воді речовин. Він ґрунтується на тому, що під дією води на суміш відбувається дуже сильне подрібнення розчинної речовини. Внаслідок збовтування суміші у воді утворюється каламутна рідина, в якій є такі дрібні часточки розчинної речовини, які разом з молекулами води проходять крізь пористий матеріал, а часточки нерозчинної речовини залишаються на його поверхні.
Такий спосіб розділення сумішей називають фільтруванням. Матеріал, крізь який фільтрують рідину, називають фільтром. Нерозчинні речовини, що залишилися на фільтрі, називають осадом, а розчин, що пройшов крізь фільтр,— фільтратом (мал. 42).

Мал. 42, 43. Фільтрування та випарювання.
У побуті й на виробництві як фільтрувальний матеріал використовують тканини різної щільності. На водоочисних станціях воду фільтрують крізь шар чистого піску.
3. Випарювання і кристалізація
Якщо з фільтрату треба виділити розчинну тверду речовину, наприклад кухонну сіль, то розчин випарюють (мал. 43). Вода випаровується, а сіль залишається на дні чашки для випарювання. Іноді воду випарюють не повністю. Часткове випарювання води називають упарюванням. В результаті утворюється концентрований розчин, під час охолодження якого розчинна речовина кристалізується, тобто виділяється у вигляді кристалів.
4. Дистиляція
Щоб розділити рідини, розчинні одна в одній, використовують різницю їхніх температур кипіння. Наприклад, щоб відокремити спирт від води, цю суміш наливають у колбу 1 (мал. 44), нагрівають до кипіння і спостерігають за показами термометра 2. При температурі близько 78 °С виходить пара майже чистого спирту. Вона потрапляє у внутрішню трубку 4 холодильника б, охолоджується водою 5, конденсується і переходить у рідкий стан. Рідкий спирт стікає у склянку-збірник 7. Дистиляція, або перегонка, широко використовується у промисловості, наприклад, під час переробки нафти, яка є сумішшю речовин, подібних за багатьма властивостями, але відмінних за температурами кипіння.
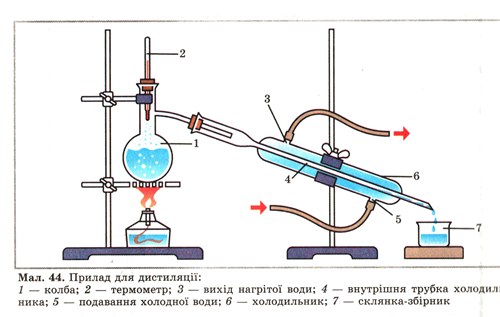
Мал. 44. Прилад для дистиляції.
КОРОТКІ висновки
Речовини поділяють на чисті, тобто без домішок, і змішані одна з одною, тобто суміші.
У сумішах речовини можуть перебувати у будь-якому агрегатному стані. Речовини, що входять до складу сумішей — компоненти, зберігають свої властивості. Суміші поділяють на однорідні та неоднорідні. Однорідні суміші, в яких навіть за допомогою мікроскопу не можна виявити часточок інших речовин, розділяють випарюванням або дистиляцією.
Неоднорідні суміші, в яких неозброєним оком або за допо могою мікроскопу можна виявити часточки інших речовин, розділяють відстоюванням, декантацією, фільтруванням.
Завдання для самоконтролю
1. Яка речовина називається чистою?
2. За якими ознаками можна відрізнити чисту речовину від суміші?
3. Які способи розділення сумішей ти знаєш?
4. Як практично можна довести, що нафта є сумішшю, а не чистою речовиною?
5. Як очистити порошок крейди, якщо він засмічений тирсою?
6. Індивідуальні речовини (на відміну від сумішей) — це
(а) молоко; (в) повітря;
(б) вода; (г) вуглекислий газ.
7. Суміші (на відміну від індивідуальних речовин) — це
(а) кисень; (в) граніт;
(б) ґрунт; (г) натрій хлорид.
8. Склади план роботи по розділенню суміші, що містить річний пісок і кухонну сіль.
Додаткові завдання
9. Як ти вважаєш, суміш яких речовин могли розділяти стародавні люди за допомогою посудини, що показана на мал. 45.
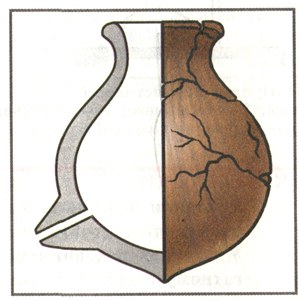
Мал. 45. Завдання.
10. Перед переробкою побутового сміття і паперової макулатури потрібно позбутися від залізних предметів. Як, на твій погляд, найпростіше це зробити?
11. Поясни, чому пилосос всмоктує повітря, яке містить пил, а випускає чисте.
12. Поясни, чи можна проводити розділення сумішей шляхом фільтрування або декантації в умовах космічної станції. Чому?
Хімія 7. Підручник для загальноосвітніх навчальних закладів. Н. М. Буринська
Планування уроків з хімії , відповіді на тести, завдання та відповіді по класам , домашнє завадання та робота з хімії 7 класу
Зміст уроку
 конспект уроку і опорний каркас конспект уроку і опорний каркас
 презентація уроку презентація уроку
 акселеративні методи та інтерактивні технології акселеративні методи та інтерактивні технології
 закриті вправи (тільки для використання вчителями) закриті вправи (тільки для використання вчителями)
 оцінювання
Практика оцінювання
Практика
 задачі та вправи,самоперевірка задачі та вправи,самоперевірка
 практикуми, лабораторні, кейси практикуми, лабораторні, кейси
 рівень складності задач: звичайний, високий, олімпійський рівень складності задач: звичайний, високий, олімпійський
 домашнє завдання
Ілюстрації домашнє завдання
Ілюстрації
 ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа ілюстрації: відеокліпи, аудіо, фотографії, графіки, таблиці, комікси, мультимедіа
 реферати реферати
 фішки для допитливих фішки для допитливих
 шпаргалки шпаргалки
 гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення гумор, притчі, приколи, приказки, кросворди, цитати
Доповнення
 зовнішнє незалежне тестування (ЗНТ) зовнішнє незалежне тестування (ЗНТ)
 підручники основні і допоміжні підручники основні і допоміжні
 тематичні свята, девізи тематичні свята, девізи
 статті статті
 національні особливості національні особливості
 словник термінів словник термінів
 інше
Тільки для вчителів інше
Тільки для вчителів
 ідеальні уроки ідеальні уроки
 календарний план на рік календарний план на рік
 методичні рекомендації методичні рекомендації
 програми програми
 обговорення обговорення
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|


















