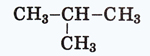|
Гіпермаркет Знань>>Хімія>>Хімія 11 клас>>Явище ізомерії. Структурна ізомерія, номенклатура насичених вуглеводнів.
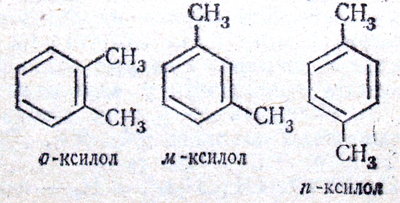
Ізомерія Ізомерія – явище, при якому різні сполуки, що мають однаковий якісний і кількісний склад, відрізняються своїми властивостями. Ізомерія пояснюється різною будовою молекул таких сполук (ізомерів). Відомо два основні типи ізомерії: структурна і просторова (стереоізомерія). Молекули структурних ізомерів різняться порядком зв’язку атомів і молекул, тобто хімічною будовою. В молекулах стереоізомерів хімічна будова однакова, але атоми по-різному розміщені в просторі. В гомологічному ряду вуглеводнів структурна ізомерія можлива з C4H10 : н-бутан CH3CH2CH2CH3 та ізобутан (CH3)2СН-СН3. Із збільшенням кількості атомів карбону число ізомерів швидко зростає. В ряду ароматичних вуглеводнів існує ізомерія положення відносно замісника та ізомерія в бензольному кільці:
Ізомери можуть відрізнятися не тільки будовою карбонового ланцюга, а й характером функціональних груп: наприклад, ізомерами є етиловий спирт CH3CH2OH і дим етиловий етер CH3 – O – CH3. До просторової ізомерії відносять геометричну (цис – транс - ізомерія) і оптичну ізомерію. Просторова ізомерія можлива для сполук, що містять подвійні зв’язки. Приклад геометричних ізомерів:
Оптична ізомерія виникає при наявності просторової асиметрії молекул, найчастіше завдяки асиметричним атомам карбону, наприклад молочна кислота CH3 – C*H(OH) – COOH(асиметричний атом позначено *). Ізомерія є однією з причин, що зумовлює величезну кількість органічних сполук.
Номенклатура алканів Насичені вуглеводні, молекули яких мають відкритий карбоновий ланцюг, називають алканами. У ХХ ст. було запропоновано систему назв(систематичну номенклатуру) органічних сполук. Згідно з нею, назви усіх алканів мають суфікс –ан. Для перших чотирьох сполук гомологічного ряду використовують такі назви: CH4 – метан; С2Н6 – етан; С3Н8 – пропан; С4Н10 – бутан.
Основу решти алканів становлять грецькі числівники, які відповідають кількості атомів Карбону в молекулах сполук. Приклади: С5Н12 – пентан, С6Н14 – гексан, С7Н16 – гептан, С8Н18 – октан, С9Н20 – нонан, С10Н22 – декан (5 – «пента», 6 – «гекса» і т.д.). Якщо молекула вуглеводню має лінійну будову, то перед назвою алкану додають літеру н (тобто, «нормальна будова»). Наприклад, сполуку із формулою CH3 - CH2 - CH2 - CH3 називають н – бутаном. Другий ізомер бутану має назву «ізобутан». Якщо для вуглеводню існує кілька ізомерів, то їх назви повинні відрізнятися. Для цього у правилах складання назв використовують поняття замісник. Замісник – це атом або група атомів, яка є відгалуженням від лінійного або замкненого карбонового ланцюга молекули. Замісники часто позначають літерою R. Якщо замісник складається з атомів Карбону і Гідрогену, то його називають вуглеводневим залишком. Формулу вуглеводневого залишку можна отримати, віднявши від формули алкану атом Гідрогену. Назва такого замісника походить від назви алкану і має суфікс -ил(-іл): CH3 – метил; С2Н5 – етил; С3Н7 – пропіл; С4Н9 – бутил.
Ці замісники мають загальну назву алкіли. Їх загальна формула – СnH2n+1. Замісником у молекулі ізобутану є група атомів СН3 , а молекула містить три замісники – групу атомів С2Н5 і дві групи СН3.
Правила складання назв алканів: 1. У молекулі знаходять найдовший (головний) карбоновий ланцюг і нумерують у ньому атоми Карбону. Нумерацію починають із того кінця ланцюга, до якого ближче знаходиться замісник. 2. Визначають назву кожного замісника. 3. Назви замісників розміщують на початку назви сполуки (за алфавітом). Перед назвою кожного замісника через дефіс указують номер атома карбону, з яким сполучений замісник. Останньою записують назву алкану нерозгалуженої будови, молекула якого містить стільки атомів Карбону, скільки їх у головному ланцюзі. 4. При наявності кількох однакових замісників їх кількість указують, добавляючи до назви замісника числовий префікс (ди-, три-, тетра- тощо), а перед ним указують номери відповідних атомів Карбону, розділені комами.
Зміст уроку Если у вас есть исправления или предложения к данному уроку, напишите нам. Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум. |
Авторські права | Privacy Policy |FAQ | Партнери | Контакти | Кейс-уроки
© Автор системы образования 7W и Гипермаркета Знаний - Владимир Спиваковский
При использовании материалов ресурса
ссылка на edufuture.biz обязательна (для интернет ресурсов -
гиперссылка).
edufuture.biz 2008-© Все права защищены.
Сайт edufuture.biz является порталом, в котором не предусмотрены темы политики, наркомании, алкоголизма, курения и других "взрослых" тем.
Ждем Ваши замечания и предложения на email: 
По вопросам рекламы и спонсорства пишите на email: