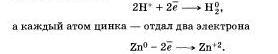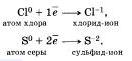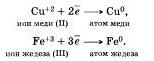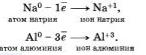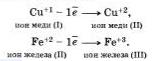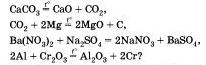|
|
|
| Строка 1: |
Строка 1: |
| - | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 8 класс|Химия 8 класс]]>> Химия: Окислительно-восстановительные реакции<metakeywords>химия, 8 класс, класс, урок химии, на тему, урок на тему, урок для 8 класса, Окислительно-восстановительные реакции</metakeywords>''' | + | '''[[Гипермаркет знаний - первый в мире!|Гипермаркет знаний]]>>[[Химия|Химия]]>>[[Химия 8 класс|Химия 8 класс]]>> Химия: Окислительно-восстановительные реакции<metakeywords>химия, 8 класс, класс, урок химии, на тему, урок на тему, урок для 8 класса, Окислительно-восстановительные реакции</metakeywords>''' Многообразие классификаций [[Скорость_химических_реакций|химических реакций]] по различным признакам (фазе, направлению, числу и характеру реагирующих и образующих веществ, использованию катализатора, тепловому эффекту) можно дополнить еще одним признаком. Этот признак — изменение степени окисления атомов химических элементов, образующих реагирующие вещества. Например, в реакции<br> |
| - | Многообразие классификаций химических реакций по различным признакам (фазе, направлению, числу и характеру реагирующих и образующих веществ, использованию катализатора, тепловому эффекту) можно дополнить еще одним признаком. Этот признак — изменение степени окисления атомов химических элементов, образующих реагирующие вещества. Например, в реакции<br> | + | |
| | | | |
| - | [[Image:him8-157.jpg]]<br> | + | [[Image:Him8-157.jpg|химия 8 класс]]<br> |
| | | | |
| - | <br> | + | <br> |
| | | | |
| - | степени окисления атомов химических элементов после реакции не изменились. А вот в другой реакции — взаимодействие соляной кислоты с цинком<br> | + | степени окисления атомов химических элементов после реакции не изменились. А вот в другой реакции — взаимодействие соляной [[Кислоты._Полные_уроки|кислоты]] с цинком<br> |
| | | | |
| - | <br> | + | <br> |
| | | | |
| - | [[Image:him8-158.jpg]]<br> | + | [[Image:Him8-158.jpg|химия 8 класс]]<br> |
| | | | |
| - | <br> | + | <br> |
| | | | |
| - | атомы двух элементов, водорода и цинка, изменили свои степени окисления: водород с +1 на 0, а цинк с 0 на +2. Следовательно, в этой реакции каждый атом водорода получил по одному электрону:<br> | + | атомы двух элементов, водорода и цинка, изменили свои степени окисления: водород с +1 на 0, а цинк с 0 на +2. Следовательно, в этой реакции каждый атом водорода получил по одному электрону:<br> |
| | | | |
| - | <br> | + | <br> |
| | | | |
| - | [[Image:him8-159.jpg]]<br> | + | [[Image:Him8-159.jpg|химия 8 класс]]<br> |
| | | | |
| - | <br> | + | <br> |
| | | | |
| - | <br> | + | <br> |
| | | | |
| | ---- | | ---- |
| | | | |
| - | Химические реакции, в результате которых происходит изменение степеней окисления атомов химических элементов или ионов, образующих реагирующие вещества, называют окислительно-восстановительными реакциями.<br> | + | Химические реакции, в результате которых происходит изменение степеней окисления атомов химических элементов или ионов, образующих реагирующие вещества, называют окислительно-восстановительными реакциями.<br> |
| | | | |
| | ---- | | ---- |
| | | | |
| - | <br><u>''Под восстановлением''</u> понимают процесс присоединения электронов атомами, ионами или молекулами. Степень окисления ири этом понижается.<br> <br>Например, атомы неметаллов могут присоединять электроны, превращаясь при этом в отрицательные ионы, то есть восстанавливаясь: | + | <br><u>''Под восстановлением''</u> понимают процесс присоединения электронов атомами, ионами или [[Взаимодействие_молекул._Полные_уроки|молекулами]]. Степень окисления ири этом понижается.<br> <br>Например, атомы неметаллов могут присоединять электроны, превращаясь при этом в отрицательные ионы, то есть восстанавливаясь: |
| | | | |
| - | <br> | + | <br> |
| | | | |
| - | [[Image:him8-160.jpg]]<br> | + | [[Image:Him8-160.jpg|химия 8 класс]]<br> |
| | | | |
| - | <br> | + | <br> |
| | | | |
| - | Электроны могут присоединяться и к положительным ионам, превращая их при этом в атомы:<br> | + | Электроны могут присоединяться и к положительным ионам, превращая их при этом в атомы:<br> |
| | | | |
| - | <br> | + | <br> |
| | | | |
| - | [[Image:him8-161.jpg]]<br> | + | [[Image:Him8-161.jpg|химия 8 класс]]<br> |
| | | | |
| - | <br> | + | <br> |
| | | | |
| - | Принимать электроны могут и положительные ионы, у которых при этом степень окисления понижается.<br> | + | Принимать электроны могут и положительные ионы, у которых при этом степень окисления понижается.<br> |
| | | | |
| - | <br> | + | <br> |
| | | | |
| | ---- | | ---- |
| | | | |
| - | Атомы, ионы или молекулы, принимающие электроны, называются окислителями.<br> | + | Атомы, ионы или молекулы, принимающие электроны, называются окислителями.<br> |
| | | | |
| | ---- | | ---- |
| | | | |
| - | <br><u>''Под окислением''</u> понимают процесс отдачи электронов атомами, ионами или молекулами. Например, атомы металлов, теряя электроны, превращаются в положительные ионы, то есть окисляются:<br><br> | + | <br><u>''Под окислением''</u> понимают процесс отдачи электронов атомами, ионами или молекулами. Например, атомы металлов, теряя [[Состояние_электронов_в_атоме|электроны]], превращаются в положительные ионы, то есть окисляются:<br><br> |
| | | | |
| - | [[Image:him8-162.jpg]]<br> | + | [[Image:Him8-162.jpg|химия 8 класс]]<br> |
| | | | |
| - | <br> | + | <br> |
| | | | |
| - | Отдавать свои электроны могут отрицательные ионы.<br> | + | Отдавать свои электроны могут отрицательные ионы.<br> |
| | | | |
| - | <br> | + | <br> |
| | | | |
| - | Терять электроны могут и некоторые положительные ионыс низшими степенями окисления.<br> | + | Терять электроны могут и некоторые положительные ионыс низшими степенями окисления.<br> |
| | | | |
| - | [[Image:him8-163.jpg]]<br> | + | [[Image:Him8-163.jpg|химия 8 класс]]<br> |
| | | | |
| - | <br> | + | <br> |
| | | | |
| - | Можно отметить, что при этом степень окисления повышается.<br> | + | Можно отметить, что при этом степень окисления повышается.<br> |
| | | | |
| - | Атомы, ионы или молекулы, отдающие электроны, называются ''восстановителями.''<br> | + | Атомы, ионы или молекулы, отдающие электроны, называются ''восстановителями.''<br> |
| | | | |
| - | Окисление всегда сопровождается восстановлением и наоборот, то есть окислительно-восстановительные реакции представляют собой единство двух противоположных процессов — окисления н восстановления. Схема взаимосвязи изменения степеней окисления с процессами окисления и восстановления может быть представлена так, как это изображено на схеме ниже. | + | Окисление всегда сопровождается восстановлением и наоборот, то есть окислительно-восстановительные реакции представляют собой единство двух противоположных процессов — окисления н восстановления. Схема взаимосвязи изменения степеней окисления с процессами окисления и восстановления может быть представлена так, как это изображено на схеме ниже. |
| | | | |
| - | <br>В окислительно-восстановитольных реакциях число электронов, отдаваемых восстановителем, равно числу электронов, принимаемых окислителем, то есть соблюдается электронный баланс. Метод электронного баланса применяют для записей электронных уравнений процессов окисления и восстановления.<br>[[Image:him8-164.jpg]]<br> | + | <br>В окислительно-восстановитольных реакциях число электронов, отдаваемых восстановителем, равно числу электронов, принимаемых окислителем, то есть соблюдается электронный баланс. Метод электронного баланса применяют для записей электронных уравнений процессов [[Степень_окисления._Полные_уроки|окисления]] и восстановления.<br>[[Image:Him8-164.jpg|химия 8 класс]]<br> |
| | | | |
| | + | <br> |
| | | | |
| | + | Молекулярное уравнение этой реакции написать уже несложно, так как коэффициенты для него будут взяты из электронных уравнений.<br><br>Покажем, как с помощью метода электронного баланса можно расставить коэффициенты в уравнении сложной окислительно-восстановительной реакции. Как вы помните, первое правило ряда напряжений металлов о взаимодействии металлов с растворами кислот не распространялось на серную кислоту концентрированную и азотную кислоту любой концентрации. |
| | | | |
| - | Молекулярное уравнение этой реакции написать уже несложно, так как коэффициенты для него будут взяты из электронных уравнений.<br><br>Покажем, как с помощью метода электронного баланса можно расставить коэффициенты в уравнении сложной окислительно-восстановительной реакции. Как вы помните, первое правило ряда напряжений металлов о взаимодействии металлов с растворами кислот не распространялось на серную кислоту концентрированную и азотную кислоту любой концентрации.
| + | <br>В отличие от соляной кислоты, в которой окислителем атомов металла были катионы водорода, в серной и азотной кислотах окислителями являются атомы серы и азота из сульфат-ионов и нитрат-ионов. Поэтому H2S04 (конц.) и HNO3, (любой конц.) взаимодействуют с металлами, стоящими в ряду напряжений как до водорода, так и после него, восстанавливаясь при атом до S02, NO и т. д. Например, при взаимодействии разбавленной азотной кислоты с медью получается нитрат меди (II), оксид азота (II) и вода. Запишем формулы исходных и конечных веществ с указанием степеней окисления: |
| | | | |
| - | <br>В отличие от соляной кислоты, в которой окислителем атомов металла были катионы водорода, в серной и азотной кислотах окислителями являются атомы серы и азота из сульфат-ионов и нитрат-ионов. Поэтому H2S04 (конц.) и HNO3, (любой конц.) взаимодействуют с металлами, стоящими в ряду напряжений как до водорода, так и после него, восстанавливаясь при атом до S02, NO и т. д. Например, при взаимодействии разбавленной азотной кислоты с медью получается нитрат меди (II), оксид азота (II) и вода. Запишем формулы исходных и конечных веществ с указанием степеней окисления:
| + | [[Image:Him8-165.jpg|химия 8 класс]] |
| | | | |
| - | [[Image:him8-165.jpg]]
| + | <br> |
| | | | |
| | + | Подчеркнем знаки химических элементов, изменивших свои степени окисления. |
| | | | |
| | + | <br> |
| | | | |
| - | Подчеркнем знаки химических элементов, изменивших свои степени окисления.
| + | Составим электронные уравнения, то есть отразим процессы отдачи и присоединения электронов: |
| | | | |
| | + | [[Image:Him8-166.jpg|химия 8 класс]] |
| | | | |
| | + | <br> |
| | | | |
| - | Составим электронные уравнения, то есть отразим процессы отдачи и присоединения электронов:
| + | Ставим коэфициент 3 перед Cu и перед формулой нитрата меди, в котором Cu +2, так как с такими значениями степеней окисления медь встречается по одному разу.<br> |
| | | | |
| - | [[Image:him8-166.jpg]] | + | [[Image:Him8-167.jpg|химия 8 класс]] |
| | | | |
| | + | <br> |
| | | | |
| | + | Проверим правильность расстановки коэффициентов, подсчитав число атомов кислорода до и после реакции: до реакции — 24 атома и после реакции — 24 атома. Коэффициенты расставлены правильно, поэтому заменим в уравнении стрелку на знак равенства:<br> <br>[[Image:Him8-168.jpg|химия 8 класс]] |
| | | | |
| - | Ставим коэфициент 3 перед Cu и перед формулой нитрата меди, в котором Cu +2, так как с такими значениями степеней окисления медь встречается по одному разу.<br>
| + | <br> |
| | | | |
| - | [[Image:him8-167.jpg]]
| + | Зная формулу вещества и определив степени окисления атомов химических элементов в нем. нетрудно предсказать, какие свойства будет проявлять каждый элемент и вещество в целом: окислительные или восстановительные. Например, [[Азот_(Химия_9_класс)|азот]] в азотной кислоте имеет максимальное значение степени окисления +5, то есть он "потерял" все электроны, поэтому азот и азотная кислота будут проявлять только окислительные свойства. |
| | | | |
| | + | <br>Азот в аммиаке NH3, имеет минимальное значение степени окисления -3. то есть он не сможет принять больше ни одного электрона, и поэтому аммиак будет проявлять только восстановительные свойства. |
| | | | |
| | + | <br>Другой пример — оксид азота (II) N0. Азот в этом соединении имеет промежуточное значение степени окисления и поэтому может проявлять как окислительные, так и восстановительные свойства.<br> <br>Приведем примеры важнейших восстановителей и окислителей. |
| | | | |
| - | Проверим правильность расстановки коэффициентов, подсчитав число атомов кислорода до и после реакции: до реакции — 24 атома и после реакции — 24 атома. Коэффициенты расставлены правильно, поэтому заменим в уравнении стрелку на знак равенства:<br> <br>[[Image:him8-168.jpg]]
| + | <br> |
| - | | + | |
| - | | + | |
| - | | + | |
| - | Зная формулу вещества и определив степени окисления атомов химических элементов в нем. нетрудно предсказать, какие свойства будет проявлять каждый элемент и вещество в целом: окислительные или восстановительные. Например, азот в азотной кислоте имеет максимальное значение степени окисления +5, то есть он "потерял" все электроны, поэтому азот и азотная кислота будут проявлять только окислительные свойства.
| + | |
| - | | + | |
| - | <br>Азот в аммиаке NH3, имеет минимальное значение степени окисления -3. то есть он не сможет принять больше ни одного электрона, и поэтому аммиак будет проявлять только восстановительные свойства.
| + | |
| - | | + | |
| - | <br>Другой пример — оксид азота (II) N0. Азот в этом соединении имеет промежуточное значение степени окисления и поэтому может проявлять как окислительные, так и восстановительные свойства.<br> <br>Приведем примеры важнейших восстановителей и окислителей.
| + | |
| - | | + | |
| - | | + | |
| - | | + | |
| - | [[Image:him8-169.jpg]]
| + | |
| | | | |
| | + | [[Image:Him8-169.jpg|химия 8 класс]] |
| | | | |
| | + | <br> |
| | | | |
| | 1. Окислительно-восстановнтельные реакции. | | 1. Окислительно-восстановнтельные реакции. |
| Строка 126: |
Строка 125: |
| | 2. Окислитель и восстановитель; окисление и восстановление. | | 2. Окислитель и восстановитель; окисление и восстановление. |
| | | | |
| - | 3. Метод электронного баланса.<br> | + | 3. Метод электронного баланса.<br> |
| | | | |
| - | Какие из реакций, уравнения которых записаны ниже, относятся к окислительно-восстановительным: | + | Какие из реакций, уравнения которых записаны ниже, относятся к окислительно-восстановительным: |
| | | | |
| - | [[Image:him8-170.jpg]] | + | [[Image:Him8-170.jpg|химия 8 класс]] |
| | | | |
| | + | <br> |
| | | | |
| | + | Для окислительно-восстановительных реакций укажите окислитель и восстановитель, процессы окисления и восстановления, составьте электронные уравнения. |
| | | | |
| - | Для окислительно-восстановительных реакций укажите окислитель и восстановитель, процессы окисления и восстановления, составьте электронные уравнения.
| + | <br>Дайте характеристику реакции синтеза аммиака по всем известным вам признакам классификации. |
| | | | |
| - | <br>Дайте характеристику реакции синтеза аммиака по всем известным вам признакам классификации. | + | <br>Из следующих утверждений отберите истинные:<br>а) к окислительно-восстановительным будут относиться все реакции ионного обмена;<br>б) все реакции ионного обмена не будут являться окисли-тельно- восстановительными;<br>в) все [[Типы_химических_реакций_в_органической_химии|реакции замещения]] являются окислительно-восстановительными;<br>г) только некоторые реакции замещения являются окислительио-восстановительными реакциями;<br>д) к окислительно-восстановительным реакциям относятся те реакции соединения и разложения, в которых участвует хотя бы одно простое вещество;<br>е) все реакции разложения и соединения не являются окислительно - восстановительными |
| | | | |
| - | <br>Из следующих утверждений отберите истинные:<br>а) к окислительно-восстановительным будут относиться все реакции ионного обмена;<br>б) все реакции ионного обмена не будут являться окисли-тельно- восстановительными;<br>в) все реакции замещения являются окислительно-восстановительными;<br>г) только некоторые реакции замещения являются окислительио-восстановительными реакциями;<br>д) к окислительно-восстановительным реакциям относятся те реакции соединения и разложения, в которых участвует хотя бы одно простое вещество;<br>е) все реакции разложения и соединения не являются окислительно - восстановительными | + | <br>Обоснуйте свою точку зрения, докажите ее примерами уравнений реакций.<br> |
| | | | |
| - | <br>Обоснуйте свою точку зрения, докажите ее примерами уравнений реакций.<br>
| + | [[Image:Him8-171.jpg|химия 8 класс]] |
| | | | |
| - | [[Image:him8-171.jpg]]
| + | <br> |
| | | | |
| | + | Назовите окислитель в реакциях взаимодействия цинка с соляной и азотной кислотами. |
| | | | |
| - | | + | <br> <sub>конспекты уроков [[Химия 8 класс|химии 8 класса]], материал для использования [[Гипермаркет знаний - первый в мире!|учителями химии]], кроссворды к [[Химия|уроку химии]]</sub> |
| - | Назовите окислитель в реакциях взаимодействия цинка с соляной и азотной кислотами.
| + | |
| - | | + | |
| - | <br> <sub>конспекты уроков [[Химия_8_класс|химии 8 класса]], материал для использования [[Гипермаркет_знаний_-_первый_в_мире!|учителями химии]], кроссворды к [[Химия|уроку химии]]</sub> | + | |
| | | | |
| | '''<u>Содержание урока</u>''' | | '''<u>Содержание урока</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] конспект урока ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] конспект урока ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] опорный каркас | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] опорный каркас |
| - | [[Image:1236084776 kr.jpg|10x10px]] презентация урока | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] презентация урока |
| - | [[Image:1236084776 kr.jpg|10x10px]] акселеративные методы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] акселеративные методы |
| - | [[Image:1236084776 kr.jpg|10x10px]] интерактивные технологии | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] интерактивные технологии |
| | | | |
| | '''<u>Практика</u>''' | | '''<u>Практика</u>''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] задачи и упражнения | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] задачи и упражнения |
| - | [[Image:1236084776 kr.jpg|10x10px]] самопроверка | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] самопроверка |
| - | [[Image:1236084776 kr.jpg|10x10px]] практикумы, тренинги, кейсы, квесты | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] практикумы, тренинги, кейсы, квесты |
| - | [[Image:1236084776 kr.jpg|10x10px]] домашние задания | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] домашние задания |
| - | [[Image:1236084776 kr.jpg|10x10px]] дискуссионные вопросы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] дискуссионные вопросы |
| - | [[Image:1236084776 kr.jpg|10x10px]] риторические вопросы от учеников | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] риторические вопросы от учеников |
| - |
| + | |
| | '''<u>Иллюстрации</u>''' | | '''<u>Иллюстрации</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] аудио-, видеоклипы и мультимедиа ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] аудио-, видеоклипы и мультимедиа ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] фотографии, картинки | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фотографии, картинки |
| - | [[Image:1236084776 kr.jpg|10x10px]] графики, таблицы, схемы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] графики, таблицы, схемы |
| - | [[Image:1236084776 kr.jpg|10x10px]] юмор, анекдоты, приколы, комиксы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] юмор, анекдоты, приколы, комиксы |
| - | [[Image:1236084776 kr.jpg|10x10px]] притчи, поговорки, кроссворды, цитаты | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] притчи, поговорки, кроссворды, цитаты |
| | | | |
| | '''<u>Дополнения</u>''' | | '''<u>Дополнения</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] рефераты''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] рефераты''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] статьи | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] статьи |
| - | [[Image:1236084776 kr.jpg|10x10px]] фишки для любознательных | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] фишки для любознательных |
| - | [[Image:1236084776 kr.jpg|10x10px]] шпаргалки | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] шпаргалки |
| - | [[Image:1236084776 kr.jpg|10x10px]] учебники основные и дополнительные | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] учебники основные и дополнительные |
| - | [[Image:1236084776 kr.jpg|10x10px]] словарь терминов | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] словарь терминов |
| - | [[Image:1236084776 kr.jpg|10x10px]] прочие | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] прочие |
| | '''<u></u>''' | | '''<u></u>''' |
| | <u>Совершенствование учебников и уроков | | <u>Совершенствование учебников и уроков |
| - | </u>'''[[Image:1236084776 kr.jpg|10x10px]] исправление ошибок в учебнике''' | + | </u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] исправление ошибок в учебнике''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] обновление фрагмента в учебнике | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обновление фрагмента в учебнике |
| - | [[Image:1236084776 kr.jpg|10x10px]] элементы новаторства на уроке | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] элементы новаторства на уроке |
| - | [[Image:1236084776 kr.jpg|10x10px]] замена устаревших знаний новыми | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] замена устаревших знаний новыми |
| - |
| + | |
| | '''<u>Только для учителей</u>''' | | '''<u>Только для учителей</u>''' |
| - | <u></u>'''[[Image:1236084776 kr.jpg|10x10px]] идеальные уроки ''' | + | <u></u>'''[[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] идеальные уроки ''' |
| - | [[Image:1236084776 kr.jpg|10x10px]] календарный план на год | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] календарный план на год |
| - | [[Image:1236084776 kr.jpg|10x10px]] методические рекомендации | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] методические рекомендации |
| - | [[Image:1236084776 kr.jpg|10x10px]] программы | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] программы |
| - | [[Image:1236084776 kr.jpg|10x10px]] обсуждения | + | [[Image:1236084776 kr.jpg|10x10px|1236084776 kr.jpg]] обсуждения |
| | | | |
| | | | |
Текущая версия на 06:30, 29 июня 2012
Гипермаркет знаний>>Химия>>Химия 8 класс>> Химия: Окислительно-восстановительные реакции Многообразие классификаций химических реакций по различным признакам (фазе, направлению, числу и характеру реагирующих и образующих веществ, использованию катализатора, тепловому эффекту) можно дополнить еще одним признаком. Этот признак — изменение степени окисления атомов химических элементов, образующих реагирующие вещества. Например, в реакции
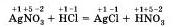
степени окисления атомов химических элементов после реакции не изменились. А вот в другой реакции — взаимодействие соляной кислоты с цинком
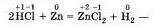
атомы двух элементов, водорода и цинка, изменили свои степени окисления: водород с +1 на 0, а цинк с 0 на +2. Следовательно, в этой реакции каждый атом водорода получил по одному электрону:
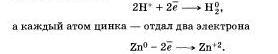
Химические реакции, в результате которых происходит изменение степеней окисления атомов химических элементов или ионов, образующих реагирующие вещества, называют окислительно-восстановительными реакциями.
Под восстановлением понимают процесс присоединения электронов атомами, ионами или молекулами. Степень окисления ири этом понижается.
Например, атомы неметаллов могут присоединять электроны, превращаясь при этом в отрицательные ионы, то есть восстанавливаясь:
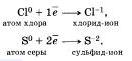
Электроны могут присоединяться и к положительным ионам, превращая их при этом в атомы:
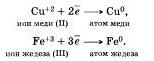
Принимать электроны могут и положительные ионы, у которых при этом степень окисления понижается.
Атомы, ионы или молекулы, принимающие электроны, называются окислителями.
Под окислением понимают процесс отдачи электронов атомами, ионами или молекулами. Например, атомы металлов, теряя электроны, превращаются в положительные ионы, то есть окисляются:
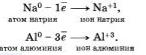
Отдавать свои электроны могут отрицательные ионы.
Терять электроны могут и некоторые положительные ионыс низшими степенями окисления.
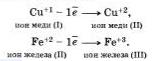
Можно отметить, что при этом степень окисления повышается.
Атомы, ионы или молекулы, отдающие электроны, называются восстановителями.
Окисление всегда сопровождается восстановлением и наоборот, то есть окислительно-восстановительные реакции представляют собой единство двух противоположных процессов — окисления н восстановления. Схема взаимосвязи изменения степеней окисления с процессами окисления и восстановления может быть представлена так, как это изображено на схеме ниже.
В окислительно-восстановитольных реакциях число электронов, отдаваемых восстановителем, равно числу электронов, принимаемых окислителем, то есть соблюдается электронный баланс. Метод электронного баланса применяют для записей электронных уравнений процессов окисления и восстановления.

Молекулярное уравнение этой реакции написать уже несложно, так как коэффициенты для него будут взяты из электронных уравнений.
Покажем, как с помощью метода электронного баланса можно расставить коэффициенты в уравнении сложной окислительно-восстановительной реакции. Как вы помните, первое правило ряда напряжений металлов о взаимодействии металлов с растворами кислот не распространялось на серную кислоту концентрированную и азотную кислоту любой концентрации.
В отличие от соляной кислоты, в которой окислителем атомов металла были катионы водорода, в серной и азотной кислотах окислителями являются атомы серы и азота из сульфат-ионов и нитрат-ионов. Поэтому H2S04 (конц.) и HNO3, (любой конц.) взаимодействуют с металлами, стоящими в ряду напряжений как до водорода, так и после него, восстанавливаясь при атом до S02, NO и т. д. Например, при взаимодействии разбавленной азотной кислоты с медью получается нитрат меди (II), оксид азота (II) и вода. Запишем формулы исходных и конечных веществ с указанием степеней окисления:
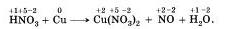
Подчеркнем знаки химических элементов, изменивших свои степени окисления.
Составим электронные уравнения, то есть отразим процессы отдачи и присоединения электронов:

Ставим коэфициент 3 перед Cu и перед формулой нитрата меди, в котором Cu +2, так как с такими значениями степеней окисления медь встречается по одному разу.

Проверим правильность расстановки коэффициентов, подсчитав число атомов кислорода до и после реакции: до реакции — 24 атома и после реакции — 24 атома. Коэффициенты расставлены правильно, поэтому заменим в уравнении стрелку на знак равенства:
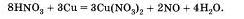
Зная формулу вещества и определив степени окисления атомов химических элементов в нем. нетрудно предсказать, какие свойства будет проявлять каждый элемент и вещество в целом: окислительные или восстановительные. Например, азот в азотной кислоте имеет максимальное значение степени окисления +5, то есть он "потерял" все электроны, поэтому азот и азотная кислота будут проявлять только окислительные свойства.
Азот в аммиаке NH3, имеет минимальное значение степени окисления -3. то есть он не сможет принять больше ни одного электрона, и поэтому аммиак будет проявлять только восстановительные свойства.
Другой пример — оксид азота (II) N0. Азот в этом соединении имеет промежуточное значение степени окисления и поэтому может проявлять как окислительные, так и восстановительные свойства.
Приведем примеры важнейших восстановителей и окислителей.

1. Окислительно-восстановнтельные реакции.
2. Окислитель и восстановитель; окисление и восстановление.
3. Метод электронного баланса.
Какие из реакций, уравнения которых записаны ниже, относятся к окислительно-восстановительным:
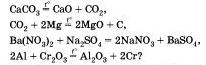
Для окислительно-восстановительных реакций укажите окислитель и восстановитель, процессы окисления и восстановления, составьте электронные уравнения.
Дайте характеристику реакции синтеза аммиака по всем известным вам признакам классификации.
Из следующих утверждений отберите истинные:
а) к окислительно-восстановительным будут относиться все реакции ионного обмена;
б) все реакции ионного обмена не будут являться окисли-тельно- восстановительными;
в) все реакции замещения являются окислительно-восстановительными;
г) только некоторые реакции замещения являются окислительио-восстановительными реакциями;
д) к окислительно-восстановительным реакциям относятся те реакции соединения и разложения, в которых участвует хотя бы одно простое вещество;
е) все реакции разложения и соединения не являются окислительно - восстановительными
Обоснуйте свою точку зрения, докажите ее примерами уравнений реакций.

Назовите окислитель в реакциях взаимодействия цинка с соляной и азотной кислотами.
конспекты уроков химии 8 класса, материал для использования учителями химии, кроссворды к уроку химии
Содержание урока
 конспект урока конспект урока
 опорный каркас опорный каркас
 презентация урока презентация урока
 акселеративные методы акселеративные методы
 интерактивные технологии
Практика интерактивные технологии
Практика
 задачи и упражнения задачи и упражнения
 самопроверка самопроверка
 практикумы, тренинги, кейсы, квесты практикумы, тренинги, кейсы, квесты
 домашние задания домашние задания
 дискуссионные вопросы дискуссионные вопросы
 риторические вопросы от учеников
Иллюстрации риторические вопросы от учеников
Иллюстрации
 аудио-, видеоклипы и мультимедиа аудио-, видеоклипы и мультимедиа
 фотографии, картинки фотографии, картинки
 графики, таблицы, схемы графики, таблицы, схемы
 юмор, анекдоты, приколы, комиксы юмор, анекдоты, приколы, комиксы
 притчи, поговорки, кроссворды, цитаты
Дополнения притчи, поговорки, кроссворды, цитаты
Дополнения
 рефераты рефераты
 статьи статьи
 фишки для любознательных фишки для любознательных
 шпаргалки шпаргалки
 учебники основные и дополнительные учебники основные и дополнительные
 словарь терминов словарь терминов
 прочие
Совершенствование учебников и уроков прочие
Совершенствование учебников и уроков
 исправление ошибок в учебнике исправление ошибок в учебнике
 обновление фрагмента в учебнике обновление фрагмента в учебнике
 элементы новаторства на уроке элементы новаторства на уроке
 замена устаревших знаний новыми
Только для учителей замена устаревших знаний новыми
Только для учителей
 идеальные уроки идеальные уроки
 календарный план на год календарный план на год
 методические рекомендации методические рекомендации
 программы программы
 обсуждения
Интегрированные уроки обсуждения
Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь - Образовательный форум.
|